
À Hong Kong, le processus d'approbation des médicaments orphelins pour maladies rares, en particulier ceux contenant de nouvelles entités chimiques ou biologiques (NCEs) pour les maladies potentiellement mortelles ou gravement débilitantes, est géré par le Conseil de la pharmacie et des poisons de Hong Kong. Vous trouverez ci-dessous un guide étape par étape pour naviguer dans le processus :
Guide étape par étape pour l'autorisation des médicaments orphelins destinés au traitement des maladies rares
Préparation et soumission
Préparez votre dossier de candidature en joignant les documents essentiels :
- Rapports d'évaluation d'experts et documents CTD sur la sécurité, l'efficacité et la qualité
- Plans de gestion des risques (PGR)
- Étiquettes des produits et notices d'information
- Rapports d'évaluation des risques liés aux impuretés élémentaires
- Record mondial d'inscriptions
Soumettez votre demande d'enregistrement via le Système d'enregistrement des produits pharmaceutiques 2.0 (PRS 2.0) sur le site web du Bureau des médicaments. Il s'agit d'une première étape cruciale pour ceux qui enregistrent des médicaments orphelins pour maladies rares à Hong Kong.
Paiement des frais
Payez les frais de demande via :
- PRS 2.0 (en ligne) – par carte de crédit ou PPS
- En personne – en espèces ou par chèque au Bureau des médicaments
- Examen et évaluation
- Le Bureau des médicaments examine tous les documents soumis avant d'accepter la demande pour évaluation.
- Si les documents sont incomplets, une lettre de carence sera émise.
- Mécanisme de refus d'enregistrement (RTF)
- À compter du 1er juillet 2024, le mécanisme RTF garantit que seules les demandes complètes et dûment documentées seront soumises à l'évaluation. Un délai de 60 jours est accordé aux demandeurs pour remédier aux lacunes constatées lors de l'examen préliminaire.
- Les demandes incomplètes seront rejetées dès la phase de présélection. L'absence de réponse dans un délai de 60 jours entraînera le rejet automatique de la demande.
Procédures améliorées pour les produits NCE
Pour NCE relevant du «mécanisme 1+ »(destinés au traitement de maladies mortelles ou gravement invalidantes), le Conseil a approuvé des améliorations visant à faciliter et à accélérer le processus d'enregistrement, ce qui est particulièrement bénéfique pour les médicaments destinés au traitement des maladies orphelines.
- Exigences après l'approbation
- Une fois le produit enregistré :
- Se conformer aux exigences de pharmacovigilance
- Signaler les effets indésirables graves des médicaments (EIG)
- Mettre en œuvre et maintenir les plans de gestion des risques
- Une fois le produit enregistré :
Recours
En cas de contestation d'une décision du comité, le demandeur peut faire appel devant le Tribunal d'appel des pharmacies et des poisons.
Délais
Le ministère de la Santé vise à achever le processus d'enregistrement environ 9 mois après la soumission, à condition que tous les documents soient complets. Cela contribue à commercialiser efficacement les médicaments pour maladies rares.
Consultation et retours
Le Conseil peut mener des consultations avec les parties prenantes et les experts de l'industrie pendant les phases d'évaluation et de mise en œuvre des politiques.
Mises à jour continues
Restez informé en consultant régulièrement :
- Le site officiel du Conseil
- Annonces du Bureau des médicaments
Organigramme
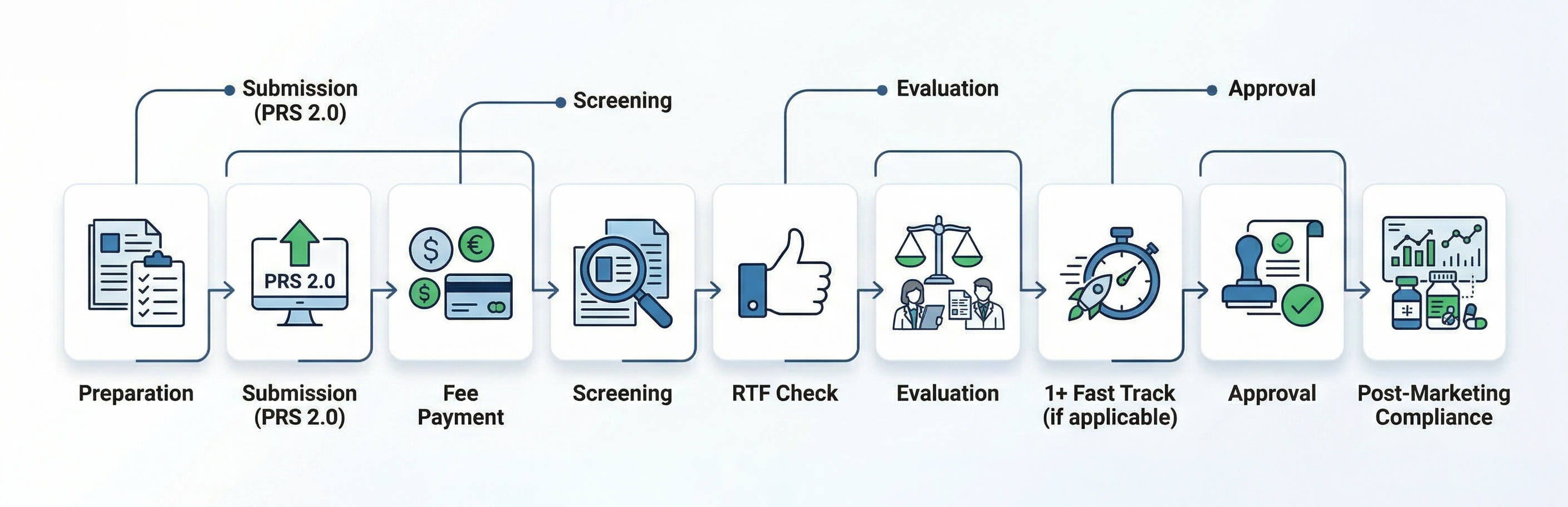
Comment Freyr peut vous aider
Freyr offre un accompagnement End-to-End pour l'enregistrement des médicaments orphelins à Hong Kong, y compris la préparation des dossiers, la navigation dans PRS 2.0 et la conformité après approbation. Grâce à notre expertise locale et à une approche stratégique, nous contribuons à assurer une mise sur le marché plus rapide et conforme des médicaments orphelins pour les maladies rares.









