
Dans l'industrie pharmaceutique, la sécurité des patients repose sur un facteur essentiel : la constance de la qualité des produits. Chaque comprimé, flacon ou injection remis à un patient doit agir exactement comme prévu. Cette constance est le fruit d'une validation rigoureuse des procédés (PV), encadrée par un dispositif solide d'assurance qualité (QA).
La validation des procédés est une approche axée sur la qualité qui garantit que les procédés de fabrication sont bien compris, maîtrisés et capables de fournir de manière constante des produits conformes aux spécifications prédéfinies. Du QA , la validation des procédés passe d'une simple formalité de conformité à une mesure préventive visant à préserver à la fois l'intégrité des produits et la santé des patients.
Qu'est-ce que la validation des procédés ?
Selon les directives FDA ICH , la validation des procédés consiste en « la collecte et l'évaluation de données, depuis la phase de conception du procédé jusqu'à la production commerciale, qui permettent d'établir scientifiquement qu'un procédé est capable de fournir de manière constante des produits de qualité ».
Le cycle de vie de la validation comprend généralement trois (3) étapes essentielles :
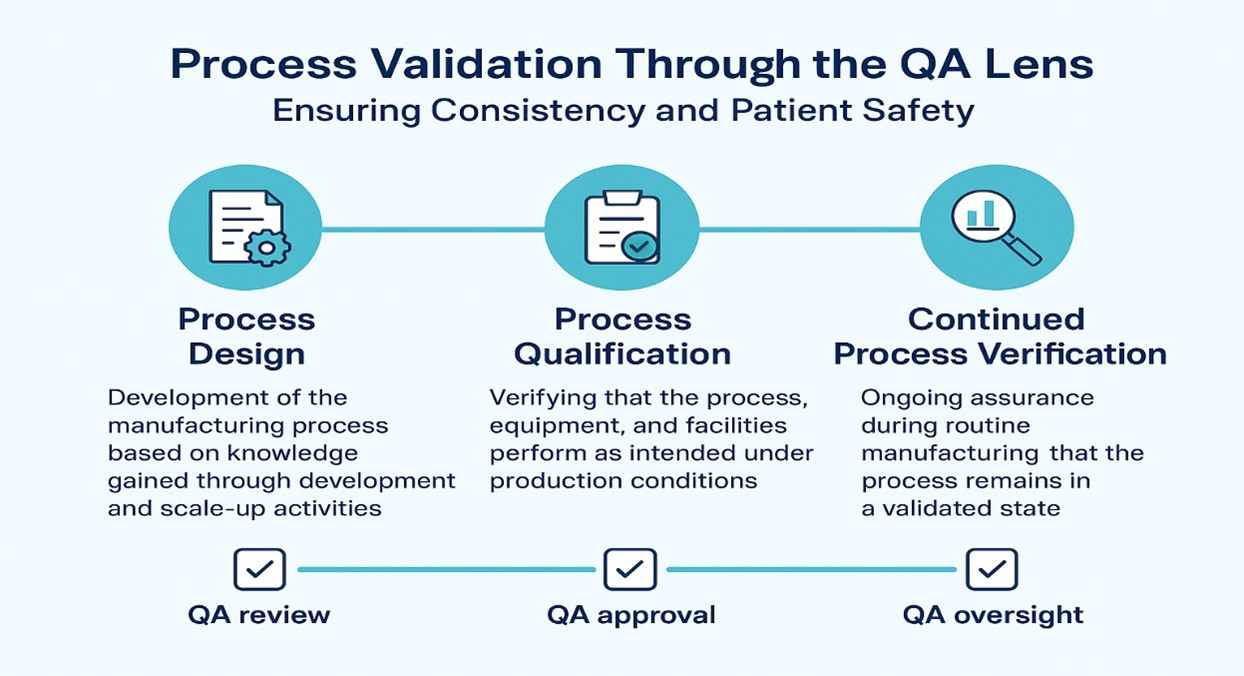
- Étape 1 – Conception du processus :
Élaboration du processus de fabrication sur la base des connaissances acquises lors des activités de développement et de mise à l'échelle.
QARôleQA: veiller à ce que les évaluations des risques, les contrôles de conception et les principes de la qualité par la conception (QbD) soient appliqués. - Étape 2 – Qualification des procédés :
Vérification que les procédés, les équipements et les installations fonctionnent comme prévu dans les conditions de production.
QARôleQA: approuver les protocoles de qualification, examiner les écarts et garantir l'intégrité des données lors de la mise en œuvre. - Étape 3 – Vérification continue du processus (CPV) :
Garantie permanente, tout au long de la fabrication courante, que le processus reste dans un état validé.
QARôleQA: mettre en œuvre des analyses de tendances, des indicateurs de qualité et des systèmes CAPA afin de maintenir le contrôle.
QA : au-delà de la documentation
Si la validation des procédés implique des évaluations techniques et statistiques, la QA veille à ce qu'elle soit menée avec une rigueur scientifique et dans le respect de la réglementation. La responsabilité QAs'étend à toutes les phases, de la planification et de l'approbation du protocole à la gestion des changements et à la vérification continue.
- Approche fondée sur les risques
QA un rôle central dans l'adoption d'une approche fondée sur les risques, telle que définie par ICH . Les paramètres critiques de processus (CPP) et les attributs critiques de qualité (CQA) sont identifiés, évalués et surveillés afin de minimiser les risques. QA ce que les protocoles de validation soient statistiquement valables et QA que des plans d'atténuation des risques soient intégrés dès la conception.
- Intégrité et traçabilité des données
À era la transformation numérique, l'intégrité des données reste une priorité absolue pour QA. Les principes ALCOA+ (Attribuable, Lisible, Contemporain, Original, Exact, ainsi que Complet, Cohérent, Durable et Disponible) guident chaque saisie et chaque vérification des données. QA ce que les données de validation — de la qualification des équipements aux dossiers de lots — soient traçables, vérifiées et conformes aux 21 CFR Part 11 .
- Amélioration continue grâce au CPV
Une fois la validation terminée, QA les performances des processus à l'aide d'outils de contrôle statistique des processus (SPC) et d'analyse des tendances. Tout écart ou résultat s'écartant de la tendance déclenche la mise en œuvre de mesures correctives et préventives (CAPA) visant à améliorer en permanence la capacité des processus. Ce système en boucle fermée renforce la conformité à long terme et réduit la variabilité des produits.
Exigences réglementaires et normes internationales
Les autorités de réglementation du monde entier, notamment laFDA US , EMA, MHRA et WHO, attendent des laboratoires pharmaceutiques qu'ils démontrent la validation de leurs processus selon une approche couvrant l'ensemble du cycle de vie. QA la conformité avec ces lignes directrices en constante évolution, notamment :
- FDA à l'intention de l'industrie – Validation des procédés : principes généraux et pratiques
- ICH (Développement pharmaceutique), Q9 (Gestion des risques liés à la qualité) et Q10 (Système de qualité pharmaceutique)
- Annexe 15 de l'UE – Qualification et validation
En assurant l'harmonisation de la documentation et la traçabilité, QA la préparation aux inspections et la conformité réglementaire à l'échelle mondiale, quelles que soient les variations régionales.
Les défis de la validation des processus et QA
Défi | Solution QA |
|---|---|
Données incohérentes d'un lot à l'autre | Mettre en place des dossiers de lot électroniques (EBR) et des points de contrôle pour la vérification QA |
Absence de justification statistique dans l'échantillonnage | QA l'alignement des protocoles sur les niveaux de confiance statistique (par exemple, les intervalles de confiance à 95 %) |
Documentation insuffisante | QA des systèmes de contrôle des documents et à la traçabilité SOP |
Écarts constatés lors de la validation | QA la gestion des écarts, l'analyse des causes profondes et la mise en œuvre des mesures correctives et préventives |
Gestion du cycle de vie | QA les programmes CPV et les critères de revalidation sont clairement définis |
La transformation numérique dans le domaine de QA la validation des processus
QA modernes ont recours à l'automatisation et aux plateformes de validation numériques pour améliorer leur efficacité et leur précision. Des outils tels que les systèmes de gestion du cycle de vie de la validation (VLMS) permettent une collaboration en temps réel entre les équipes QA, de fabrication et de validation.
Grâce à son expertise en matière de validation des systèmes informatiques (CSV) et d'assurance qualité des logiciels (CSA), Freyr aide ses clients à mettre en place des stratégies de validation numérique conformes, évolutives et prêtes pour les audits. Cela garantit non seulement la conformité, mais aussi l'excellence opérationnelle et des délais de mise sur le marché plus courts.
Instaurer la confiance grâce à la qualité
La validation des processus est un engagement permanent en faveur de la qualité, de la sécurité et de la confiance des patients. Grâce à QA , les laboratoires pharmaceutiques peuvent s'assurer que leurs processus sont non seulement validés, mais aussi améliorés en permanence afin de répondre aux normes internationales les plus strictes.
En intégrant QA chaque étape de la validation des processus, les organisations renforcent leur système de gestion de la qualité (SGQ), réduisent les risques réglementaires et tiennent leur promesse fondamentale : offrir des produits sûrs et efficaces aux patients du monde entier.
Chez Freyr, notre équipe d'experts QA en validation collabore avec des laboratoires pharmaceutiques internationaux afin de mettre en place des cadres de validation solides, conformes et prêts pour les inspections. De la mise en conformité des systèmes de gestion de la qualité (SGQ) à l'élaboration de stratégies de validation des processus, en passant par QA numérique QA , Freyr garantit une conformité réglementaire sans faille et l'excellence opérationnelle.
Découvrez comment Freyr peut vous aider à atteindre l'excellence en matière de validation.










