
La publicité pharmaceutique, y compris la publicité destinée directement aux consommateurs, est réglementée respectivement par l’Office of Prescription Drug Promotion (OPDP) de la Food and Drug Administration (FDAUS , la Advertising and Promotional Labeling Branch (APLB) du Center for Drug Evaluation and Research (CDER) et le Center for Biologics Evaluation and Research (CBER). Les informations soumises à l'OPDP et à APLB être exactes, éthiques et non trompeuses. Des informations supplémentaires sur les avantages et les risques du produit doivent être incluses dans la soumission. Ces services examinent également les supports promotionnels soumis à l'Agence.
En avril 2022, laFDA US FDA des lignes directrices concernant les soumissions relatives à l'étiquetage promotionnel et aux supports publicitaires. Ces lignes directrices aident à comprendre la soumission électronique dans le module 1 de l'eCTD, en utilisant la version 3.3 ou une version ultérieure du fichier « US ». Le document mentionne les types de supports promotionnels qui ne sont pas soumis à l'obligation de soumission électronique prévue à l'article 745A. Les copies papier de tous les types de soumissions promotionnelles seront acceptées jusqu'à vingt-quatre (24) mois après la publication des lignes directrices.
Exception
Le document précise que les demandes présentées en vertu des sections 505(b), (i) ou (j) de la loi fédérale sur les aliments, les médicaments et les cosmétiques (FD&C Act) et celles présentées en vertu des sections 47 351(a) ou (k) de la loi sur les services de santé publique (PHS Act) doivent être soumises sous un format électronique tel que défini par la FDA. Le présent document n'est pas soumis aux restrictions habituelles prévues par les règlements FDArelatifs aux bonnes pratiques en matière de lignes directrices, car il n'établit pas de responsabilités juridiquement contraignantes. Par conséquent, la partie de la présente ligne directrice qui établit l'obligation de soumettre les demandes par voie électronique en vertu de l'article 745A(a) de la FD&C Act a un effet contraignant, comme l'indique l'utilisation des termes « doit », « sera » ou « requis ».
La FDA les projets de documents promotionnels dans un délai de quarante-cinq (45) jours à compter de leur soumission volontaire par les promoteurs. Pour toute question relative au produit soulevée par les professionnels de santé, les consommateurs, les promoteurs de médicaments ou les cabinets d'avocats, l'OPDP accorde aux promoteurs un délai de trente (30) jours civils pour y répondre.
Définition des supports promotionnels
L'expression « matériel promotionnel » désigne les étiquettes promotionnelles et les supports publicitaires, quels que soient leur format, leur mode de diffusion ou le support utilisé. La FDA supervise FDA deux (02) types d'étiquetage pour les médicaments :
- Étiquetage FDA
- Étiquetage promotionnel
Conformément à l'article 201(m) FDA, l'étiquetage est défini comme « toutes les étiquettes, qu'elles soient écrites, imprimées ou graphiques, apposées sur un récipient, un emballage ou sur tout article, ou accompagnant un tel article ». L'expression « accompagnant un tel article » est considérée comme une interprétation ou une explication du matériel promotionnel, comme l'a déclaré la Cour US .
Critères pour la soumission de matériel promotionnel pour examen
- Inclusion des numéros NDA, ANDA ou BLA appropriés
- Dans les cas où les demandeurs nécessitent un examen immédiat, adressez les soumissions au chef de projet de l'OPDP
- À partir du formulaire FDA , sélectionnez la catégorie la plus précise pour désigner le matériel promotionnel
- Les différents types de documents doivent être soumis séparément.
- Ne mélangez pas d'autres dossiers avec du matériel promotionnel.
- Le matériel promotionnel destiné aux professionnels de la santé doit être soumis séparément de celui destiné aux consommateurs
Les métriques ci-dessous clarifient le nombre de formulaires 2253 soumis et les documents inclus dans ces soumissions.
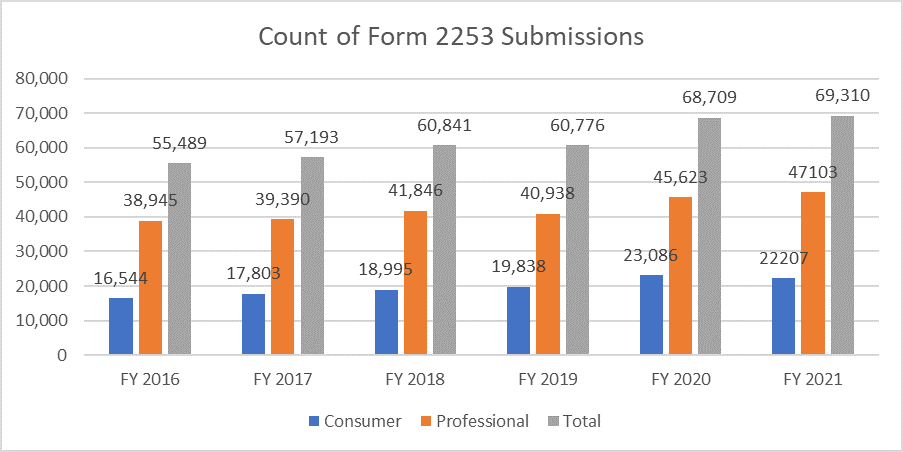
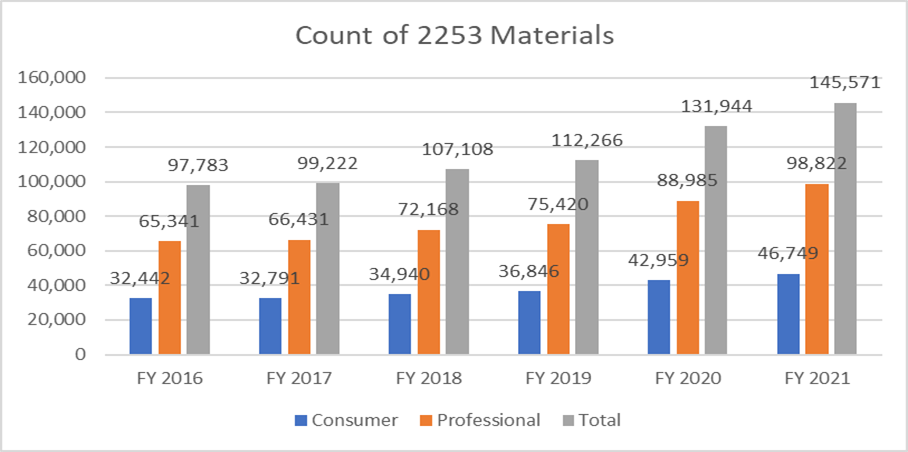
Il est primordial que les promoteurs rédigent leurs supports promotionnels conformément aux directives de la FDA éviter de multiples cycles d'examen, compte tenu du coût de la procédure. Le fait de disposer de ressources capables de faciliter le processus de soumission des supports promotionnels en toute fluidité permet aux promoteurs d'atteindre leurs objectifs commerciaux tout en respectant les exigences réglementaires. Un partenaire réglementaire expérimenté tel que Freyr peut garantir un examen complet des supports promotionnels et non promotionnels avant leur soumission, qu'ils soient sous forme électronique ou non. Contactez Freyr dès aujourd'hui pour rédiger des supports promotionnels clairs, concis et conformes dès la première fois.










