
La plupart des organisations des sciences de la vie ont du mal à rationaliser leur processus de soumissions réglementaires en raison des changements fréquents dans les directives de soumission. Selon une analyse récente menée par la United States Food and Drug Administration (USFDA), 32 % des soumissions avec données d'étude présentaient des problèmes critiques de conformité des données. Le processus nécessite une compréhension approfondie de la collaboration entre les parties prenantes internes et externes. Au sein de l'organisation, les départements de fabrication, de recherche et développement, de recherche clinique/non clinique, de QA/QC, de marketing et de ventes doivent travailler en harmonie pour accélérer le processus d'approbation, du développement initial jusqu'à la mise sur le marché du médicament. Le département des Affaires Réglementaires et les Autorités de Santé (AS) sont en correspondance constante pour assurer et évaluer la sécurité et l'efficacité des médicaments à usage humain. Voyons quelles mesures préliminaires les organisations pharmaceutiques doivent prendre pour atteindre l'excellence en matière de soumissions réglementaires :
Allouer et déployer des ressources pour rationaliser, standardiser et accélérer les processus de soumission désorganisés.
Un spécialiste des soumissions intervient sur une base contractuelle et peut maîtriser plus d'un (01) type de soumission tout en étant associé à des programmes de développement au fil des ans, aidant ainsi à élaborer des récits convaincants pour le dossier. Cela facilite la tâche des organisations pour :
- Éliminer les erreurs en équilibrant la collaboration des parties prenantes internes et externes
- Réduire le cycle d'examen par l'autorité de santé du processus de rédaction et d'approbation des documents
- Établir des soumissions complètes et conformes pour suivre l'évolution des exigences réglementaires pour les différents marchés
- Accuser réception des soumissions affectées par une Autorité Réglementaire
- Être informé de l'état de la rédaction, de l'examen et des approbations des soumissions
- Amélioration du protocole de soumission actuel
Simplifier la méthodologie de soumission des dossiers.
La rédaction d'un dossier est primordiale lors de la préparation des soumissions. Il est observé que les demandes de licence de produits biologiques (BLA) et les demandes d'autorisation de mise sur le marché de nouveaux médicaments (NDA) comprennent un très grand nombre de pages, ce qui rend difficile pour les régulateurs de saisir le contenu du dossier. Une représentation structurée d'une idée générale peut considérablement améliorer la capacité de l'équipe à préparer les soumissions et celle des agences à les examiner.
L'utilisation de modules pour simplifier les soumissions permet aux experts d'analyser ce qui doit être inclus dans chaque section ou module du dossier. Une telle pratique facilite :
- Lancement anticipé de la rédaction des documents en accélérant la préparation des dossiers de soumission de l'organisation.
- Utilisation des données pertinentes nécessaires à la rédaction des soumissions.
- Utilisation de ressources appropriées sans avoir à rédiger de nombreux documents à partir de zéro pour chaque soumission.
Travailler en collaboration avec les autorités de réglementation
Chaque organisation doit organiser des réunions régulières avec les autorités de santé (HAs) dès le début du développement d'un produit. Cette pratique assure un examen et des retours rapides, ce qui accélère la résolution des commentaires par les HAs et, par conséquent, le processus d'approbation. Cela permet non seulement d'établir de bonnes relations entre les organisations et les HAs, mais aussi d'obtenir des éclaircissements dès les premières étapes de la planification des soumissions.
Rationaliser le contenu et les données dans le Système de Gestion Documentaire (SGD)
Un référentiel de contenu robuste est censé gérer toutes les données de tous les domaines fonctionnels, y compris la documentation et les informations créées précédemment. Un référentiel de contenu et de données structuré offre un accès fluide aux documents de divers domaines fonctionnels sans effort supplémentaire ni besoin de duplication. Les documents stockés dans le DMS deviennent la source unique d'information pour toutes les parties prenantes internes (science clinique, CMC, non clinique, pharmacocinétique, pharmacodynamique, rédaction médicale et opérations cliniques). Ce contenu et ces données peuvent être utilisés pour créer du contenu local en fonction des exigences régionales. Optimisation des soumissions réglementaires grâce à la gestion structurée du contenu et des données
L'adoption de la technologie et de l'automatisation pour réduire les tâches répétitives et les erreurs
Les organisations peuvent tirer parti de la technologie en utilisant sa fonction de mise à jour automatique et de contrôle qualité des Tableaux, Listes et Figures (TLF) intégrés au texte par rapport aux données sources, afin d'accélérer le processus de documentation. Ainsi, chaque fois que des modifications sont apportées aux tableaux sources existants, une mise à jour est effectuée en conséquence dans les TLF intégrés au texte. Cela permet d'éliminer les heures de travail globales, de gagner du temps sur le chemin critique et d'améliorer la précision des données.
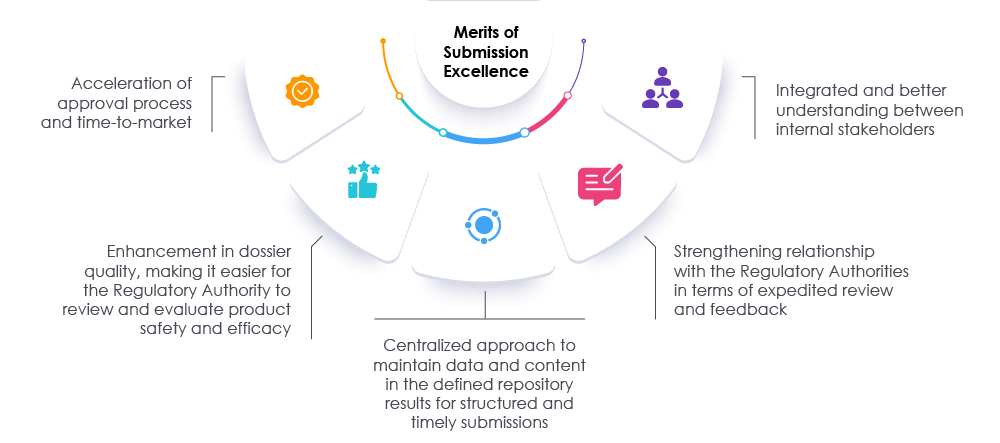
L'adoption de mesures appropriées, associée à des examens opportuns des dossiers et des données, peut aider les régulateurs et les organisations à accélérer le processus de soumission. Cette approche accélère la mise sur le marché afin de répondre aux besoins des patients et de l'industrie. Un partenaire réglementaire éprouvé peut aider les organisations à repenser, réévaluer et modifier les approches actuelles de préparation des soumissions. Nos experts chez Freyr peuvent faciliter l'atteinte de l'excellence en matière de soumissions réglementaires en augmentant la visibilité au sein de l'organisation et en promouvant la conformité globale, permettant ainsi à l'organisation de réussir sur le marché actuel des sciences de la vie. Consultez Freyr.










