POURQUOI FREYR ?
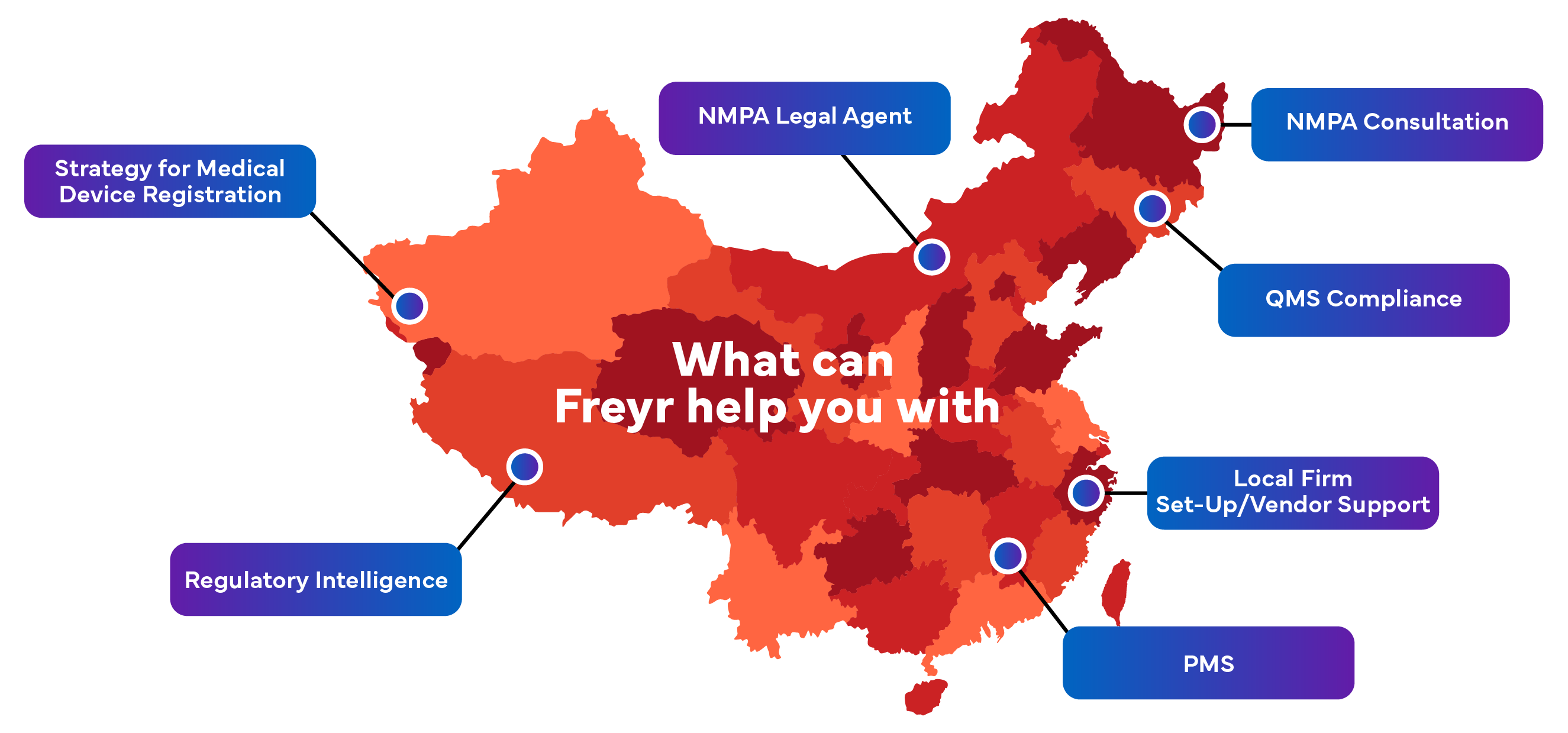
Obtenez un accès au marché sans heurts avec Freyr comme votre agent NMPA en Chine. Freyr représente de nombreuses entreprises mondiales de dispositifs médicaux en tant qu'agent chinois pour l'enregistrement NMPA.
Rencontrez nos experts en réglementation
Prenez rendez-vous
avec nos experts en réglementation dès aujourd'hui pour assurer une conformité rapide avec toutes les réglementations chinoises relatives aux dispositifs médicaux.
Foire aux questions (FAQ)
- Autorité de réglementation : NMPA (National Medical Products Administration) (anciennement CFDA)
- Réglementation : Ordonnance n° 739 du Conseil d'État
- Représentant autorisé : Agent légal NMPA requis
- Exigence du SMQ : YY/T0287-2017, ISO 13485:2016
- Évaluation des données techniques : Centre d'évaluation des dispositifs médicaux (CMDE)
- Exigences en matière de Labelling : Décret n° 6 de la CFDA
- Format de soumission : eRPS
- Langue : Anglais et chinois
La classification des dispositifs est définie dans le Catalogue de classification des dispositifs médicaux de l'Administration nationale des produits médicaux (NMPA) (Annonce n° 104/2017), ou/et les règles de l'Arrêté n° 15 pour les dispositifs médicaux. Les dispositifs sont classés en trois (03) catégories selon les critères de risque. Les dispositifs de classe I sont à faible risque et les dispositifs de classe III sont à haut risque.
| Classe de dispositif | Risque |
| I | Faible risque |
| II | Risque moyen |
| III | Haut risque |
Pour l'enregistrement des dispositifs médicaux en Chine, un dépôt de dossier auprès de la NMPA est requis pour les dispositifs médicaux de classe I, et des certificats d'enregistrement de la NMPA doivent être obtenus pour les classes II et III. Les dispositifs de classe I sont soumis à un examen administratif, tandis que les dispositifs de classe II et III sont soumis à un processus d'examen approfondi. Les exigences en matière de données et de tests varient en fonction de la disponibilité de dispositifs de référence. Par conséquent, les fabricants de dispositifs de classe II et III devraient également identifier des dispositifs de référence pour déterminer les exigences en matière de données cliniques pour leurs dispositifs. La NMPA délivre des certificats de dépôt de dossier et d'enregistrement pour les dispositifs de classe I et de classe II/III, respectivement.
En résumé, pour l'enregistrement NMPA -
Classe I - Dossier d'enregistrement et examen administratif
Classe II - Dossier d'enregistrement complet et examen complet de la demande (y compris technique)
Classe III - Dossier d'enregistrement complet et examen complet de la demande (y compris technique)
La réglementation chinoise sur les dispositifs médicaux définit le processus d'enregistrement suivant pour l'approbation des dispositifs médicaux en Chine -












