Conformité en matière d'enregistrement et de réglementation des dispositifs médicaux dans l'Union européenne
L'Union européenne représente l'un des marchés des dispositifs médicaux les plus réglementés et les plus attractifs au monde sur le plan commercial. Avec ses 27 member states, EEA 3 EEA et la Turquie, le marché de l'Union fonctionne selon un cadre réglementaire harmonisé défini par EU MDR 2017/745) pour les dispositifs médicaux et le RDI (2017/746) pour les dispositifs de diagnostic in vitro ; la région garantit ainsi des normes uniformes de sécurité et de performance pour toutes les catégories de produits. Pour commercialiser légalement un dispositif sur le marché de l'Union européenne, les fabricants doivent obtenir le marquage CE, qui confirme la conformité à la réglementation applicable en fonction de la classification des risques du dispositif et de la voie d'évaluation de la conformité. Le non-respect de ces exigences peut entraîner de graves conséquences, notamment le rappel du produit, la saisie en douane, la suspension de la certification ou la perte totale de l'accès au marché.
Dans le cadre du régime réglementaire actuel :
- Le marquage CE est obligatoire pour tous les dispositifs médicaux et les dispositifs de diagnostic in vitro avant leur mise sur le marché.
- L'enregistrement des dispositifs médicaux dans EUDAMED se déroule par étapes, et plusieurs modules sont déjà opérationnels et obligatoires.
- La désignation d'un représentant autorisé européen (EAR) est obligatoire pour tout fabricant établi en dehors de l'UE, deEEA ou deEEA.
- Les règles de classification plus strictes prévues par les directives MDR et IVDR exigent une documentation technique solide, des données cliniques ou des preuves de performance, ainsi qu'un suivi continu tout au long du cycle de vie.
Freyr accompagne les fabricants tout au long de ce processus en leur permettant d'accéder au marché de l'Union européenne en toute conformité et sans difficulté. De l'élaboration d'une stratégie de marquage CE et de la constitution du dossier technique à la gestion des demandes auprès des organismes notifiés et à la fonction de représentant autorisé dans l'UE, Freyr garantit une conformité totale aux règlements MDR et IVDR ainsi qu'un accès sans entrave à tous member states de l'UE,EEA et à la Turquie.
Processus de mise en conformité avec la réglementation européenne, étape par étape
La mise sur le marché d'un dispositif médical ou d'un dispositif de diagnostic in vitro (IVD) dans l'Union européenne (UE) comporte plusieurs étapes bien définies. Voici comment Freyr gère l'ensemble du processus pour vous :
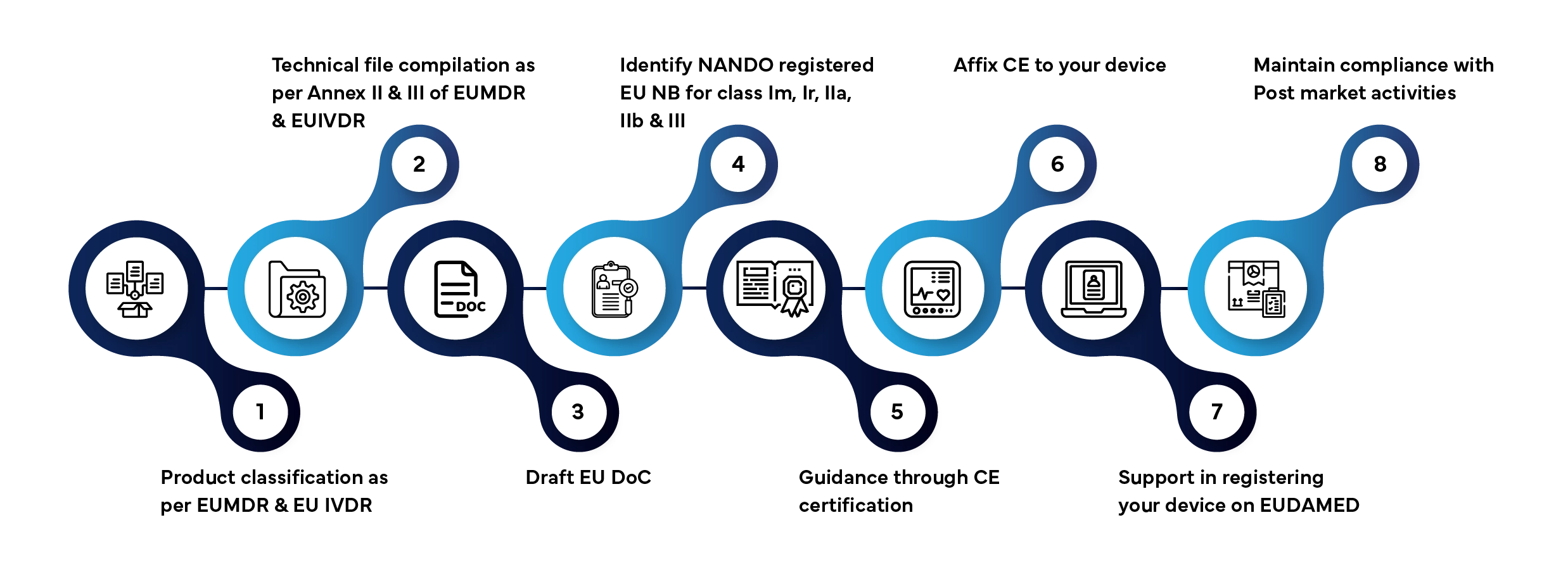
Délai de traitement habituel : 3 à 12 mois, selon la catégorie de dispositif et l'état d'avancement du dossier.
Principales offres de Freyr Medical Device dans l'Union européenne
- Stratégie réglementaire et transition vers le MDR et l'IVDR – Nous élaborons des feuilles de route end-to-end , adaptées au EU MDR à l'IVDR EU MDR , afin de garantir une transition en douceur depuis les régimes fondés sur les directives et la conformité avec les exigences actuelles de l'UE.
- Documentation technique et évaluation de la conformité – Notre équipe vous accompagne dans l'élaboration, la révision et la soumission de vos dossiers techniques / dossiers de conception, vous aide dans vos démarches auprès des organismes notifiés et gère le marquage CE, les essais de sécurité et de performance des dispositifs médicaux ainsi que les procédures de conformité.
- Évaluation clinique et de performance : Freyr assure la rédaction par des experts de rapports d'évaluation clinique (CER), de rapports d'évaluation de la performance (PER), de plans PMCF, de rapports de sécurité périodiques (PSUR), de rapports de surveillance de la sécurité (SVR), de rapports de conformité (CPR) pour les dispositifs de diagnostic in vitro (IVD), de documentation relative aux risques et de contenu d'évaluation biologique, garantissant ainsi la clarté technique et la conformité réglementaire pour toutes les classes de dispositifs.
- Assistance à l'enregistrement UDI et EUDAMED – Nous veillons à la conformité de votre système d'identification unique des dispositifs médicaux (UDI) et vous accompagnons dans l'enregistrement au sein de la base de données européenne des dispositifs médicaux EUDAMED ainsi que dans la gestion du cycle de vie associée.
- Représentant autorisé européen (EAR) et représentation locale – Pour les fabricants situés en dehors de l'UE, deEEA, nous agissons en tant que votre représentant autorisé européen (EAR) mandaté et vous apportons notre soutien en matière de conformité locale dans tous member states l'UE.
- Surveillance post-commercialisation (PMS) – Freyr vous aide à mettre en place, à mettre en œuvre et à maintenir des systèmes de surveillance post-commercialisation, notamment le plan de surveillance post-commercialisation (PMSP), le rapport de surveillance post-commercialisation (PMSR), le rapport périodique de mise à jour de sécurité (PSUR), les plans de suivi clinique et de performance post-commercialisation (PMCF), les rapports de vigilance, les FSCAs, les FSNs et les CAPAs, garantissant ainsi le maintien continu du marquage CE et un accès durable au marché, dans le respect de la conformité tout au long du cycle de vie du produit.
- Enregistrement des dispositifs médicaux au titre du marquage CE : Freyr gère l'ensemble du processus d'enregistrement au titre du marquage CE dans l'UE en assurant l'évaluation de la conformité, en préparant les dossiers de conformité, en collaborant avec les organismes notifiés et en garantissant l'obtention rapide des autorisations pour toutes les catégories de dispositifs médicaux et de dispositifs de diagnostic in vitro.
- Assistance en matière de systèmes de gestion de la qualité : nous vous accompagnons dans la mise en place et la maintenance de systèmes de gestion de la qualité ISO 13485, en adéquation avec les exigences de qualité et de sécurité EU MDR et les attentes des organismes notifiés.
- Conformité de l'étiquetage : notre équipe veille à ce que vos étiquettes, notices d'utilisation, emballages et symboles soient conformes aux exigences du règlement MDR/IVDR et aux règles linguistiques multilingues de l'UE, garantissant ainsi la cohérence et la conformité dans member states 27 member states de l'UE.
Offres de services du représentant autorisé de l'UE (EAR)
Enregistrement des dispositifs auprès des autorités de l'UE
Pour les fabricants hors UE, Freyr agit en tant que représentant autorisé désigné (EAR) au sein de l'UE, conformément aux exigences du RDM/RDIV. En tant qu'entité établie en Allemagne, Freyr accompagne les activités d'enregistrement des dispositifs auprès de l'autorité compétente allemande concernée et tient à jour les dossiers réglementaires requis. Pour Member States autres Member States de l'UE, Freyr fournit, le cas échéant, un soutien réglementaire afin de garantir la conformité des dispositifs et de faciliter leur mise sur le marché de l'Union.
Documentation et assurance de la conformité
Nos experts en réglementation vérifient que votre déclaration de conformité (DoC), vos certificats CE et vos dossiers techniques sont complets, à jour et conformes au RDM/RDIV. Freyr garantit que tout est prêt pour l'évaluation de la conformité et les demandes de marquage CE.
Réponse aux demandes des autorités compétentes
Si nécessaire, Freyr gère en votre nom toutes les communications directes et les demandes de clarification émanant des autorités compétentes de l'UE ou des organismes notifiés, en garantissant des réponses rapides et précises et en contribuant à éviter tout retard dans les procédures d'autorisation ou les contrôles réglementaires post-commercialisation.
Vigilance et communication en cas d'incident
En tant que votre EAR, Freyr assure la liaison principale pour toutes les communications relatives à la sécurité. Si nécessaire, nous coordonnons les notifications d'incidents, les mesures correctives de sécurité sur le terrain (FSCA) et les rapports de vigilance entre le fabricant, les professionnels de santé et les autorités, afin de garantir une réponse adéquate et la conformité réglementaire.
Préparation aux inspections et aux audits
Freyr conserve l'ensemble de la documentation, de la correspondance et des registres obligatoires en vue des audits et inspections des autorités. Notre équipe veille à ce que la documentation technique, l'étiquetage et les registres post-commercialisation soient facilement accessibles et pleinement conformes aux exigences du RDM et du RIDV.
Pourquoi collaborer avec Freyr ?
- Une expertise End-to-end , allant de l'enregistrement préalable à la mise sur le marché à la vigilance post-commercialisation, couvrant toutes les étapes de la conformité.
- Une expérience éprouvée, avec plus de 2 000 enregistrements d'appareils menés à bien dans diverses catégories.
- Une forte présence européenne implantée en Allemagne (EAR), complétée par des spécialistes de la réglementation sur place à Reading et soutenue par les équipes opérationnelles mondiales de Freyr.
- Une planification de transition sur mesure qui apporte un soutien stratégique pour obtenir la certification CE en toute fluidité et à moindre coût.
- Des équipes de livraison présentes dans plusieurs régions, bénéficiant d'un soutien sur le terrain grâce aux activités européennes de Freyr basées en Allemagne.
- Une expérience avérée dans la mise en conformité avec les règlements MDR et IVDR et la transition des dispositifs existants
- Une gouvernance transparente du projet grâce à une communication directe avec l'organisme notifié











