KGMP signifie « Korea Good Manufacturing Practice » (bonnes pratiques de fabrication coréennes) et s'appuie sur ISO 13485:2016. Il s'agit de la norme internationalement reconnue pour les systèmes de gestion de la qualité (SGQ) des dispositifs médicaux. Tous les fabricants de dispositifs médicaux commercialisant leurs produits en Corée du Sud doivent se conformer aux normes KGMP.
Le certificat KGMP est-il obligatoire pour tous les dispositifs ?
Les dispositifs médicaux et les diagnostics in vitro (DIV) relevant des Classes II, III et IV doivent se conformer aux réglementations KGMP et obtenir le certificat KGMP. Les dispositifs de Classe I sont exemptés de la certification KGMP mais doivent adhérer aux réglementations BPF (Bonnes Pratiques de Fabrication) des dispositifs médicaux du MFDS. Les fabricants de Classe I peuvent volontairement opter pour la « reconnaissance de conformité BPF des dispositifs médicaux de Classe I ».
Quels sont les organismes statutaires impliqués dans l'inspection KGMP ?
Les dispositifs de classe II sont soumis à un examen par des organismes d'audit accrédités par le MFDS, tandis que les dispositifs de classe III et IV nécessitent une inspection combinée par l'organisme d'examen tiers et le MFDS.
Qui peut demander le certificat KGMP ?
Les fabricants nationaux peuvent soumettre directement leurs demandes à l'organisme d'audit tiers. Pour les fabricants étrangers, le représentant local autorisé du fabricant étranger est tenu d'obtenir une licence.
Quelle est la procédure pour obtenir un certificat KGMP ?
Pour la première fois, la demande (déposée par les demandeurs – le représentant local du fabricant étranger et les fabricants nationaux) doit être soumise à des évaluateurs tiers accrédités par le MFDS. Le processus d'obtention d'un certificat KGMP est décrit ci-dessous :
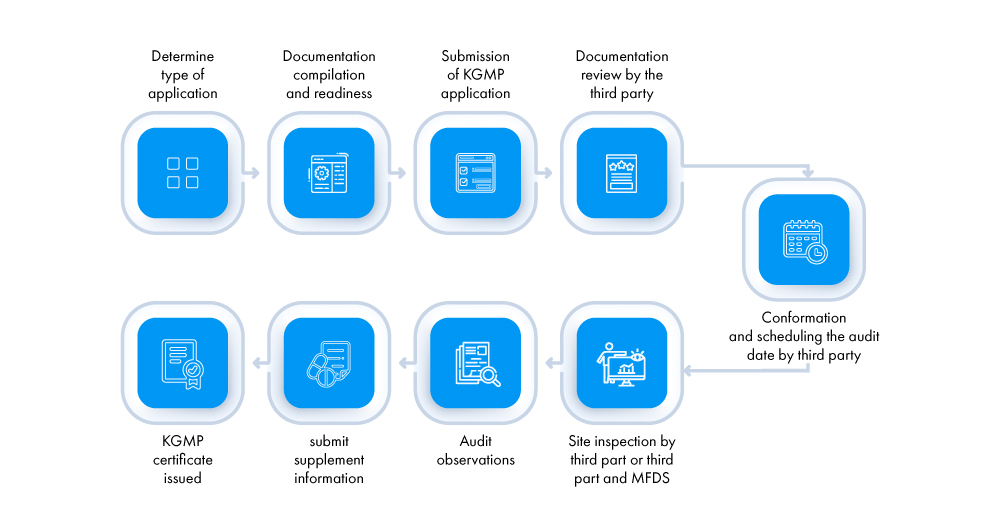
Quels sont les différents types d'inspections pour l'obtention d'un certificat KGMP ?
Selon la classe de risque du dispositif et le type de demande (nouvelle, régulière ou modification), il peut s'agir d'une inspection sur site ou d'un examen de la documentation. Avant de demander la certification KGMP, les fabricants doivent comprendre les types d'inspections possibles et le type applicable à leur situation. Les facteurs clés à prendre en compte sont :
- Si des dispositifs fabriqués sur le site sont déjà enregistrés et commercialisés en Corée ou si le dispositif concerné est le premier à être lancé sur le marché coréen
- Si un nouveau dispositif (d'une autre catégorie) est introduit dans l'établissement de fabrication déjà certifié KGMP
- Si le site de fabrication du dispositif est modifié
Inspection initiale : Une inspection initiale est effectuée lorsqu'un dispositif lancé est fabriqué dans une installation non certifiée KGMP ou si le certificat KGMP existant a expiré avant son renouvellement.
Inspection régulière : Une inspection régulière est effectuée tous les trois (03) ans pour une évaluation périodique afin de s'assurer que les fabricants continuent de se conformer aux normes BPF.
Inspection supplémentaire : Si un fabricant certifié BPF ajoute et fabrique un dispositif médical correspondant à une nouvelle catégorie, il devra subir une inspection supplémentaire pour cette nouvelle catégorie de produits. Selon le résultat de l'inspection régulière, une inspection supplémentaire peut être partielle ou complète. La validité du certificat délivré suite à une inspection supplémentaire sera alignée sur celle du certificat KGMP initialement délivré.
Évaluation des changements : Une évaluation est effectuée lorsque le site de fabrication est modifié. Une exception est faite pour le stockage et les laboratoires, qui ont un impact insignifiant sur la qualité du produit.
Comment l'évaluation KGMP est-elle réalisée ?
Le site de fabrication fera l'objet d'un examen documentaire ou d'une inspection sur site par des examinateurs tiers ou par le MFDS.
Examen des documents : L'examen des documents est effectué lorsque le fabricant possède un certificat QMS valide ou lorsqu'un rapport d'inspection de site valide délivré par des agences certifiées est disponible. Il est également effectué lorsqu'un autre importateur souhaite obtenir un certificat KGMP pour un fabricant qui possède déjà un certificat KGMP valide d'une autre importation.
Inspection sur site : Une inspection sur site est effectuée pour les dispositifs médicaux de Classe II, III et IV. L'inspection sur site peut être réalisée par des évaluateurs tiers ou conjointement par les évaluateurs tiers et la MFDS.
Quels sont les délais pour l'obtention d'un certificat KGMP ?
Selon l'exactitude du document soumis et la préparation du fabricant à l'inspection sur site, le MFDS délivre le certificat KGMP dans les deux à trois (02-03) mois suivant la soumission de la demande. Le délai pourrait être prolongé si les auditeurs soulèvent des questions pendant l'inspection, et les fabricants pourraient également prendre plus de temps pour y répondre.
Quelle est la validité du certificat KGMP ?
Après une inspection approfondie, le MFDS délivre un certificat KGMP qui est valable trois (03) ans et doit être renouvelé à l'expiration de cette période.
Quelle est la procédure pour le renouvellement d'un certificat KGMP ?
Si le certificat KGMP est sur le point d'expirer, le titulaire de la licence peut importer les dispositifs mais ne doit pas les distribuer tant que le certificat KGMP n'est pas renouvelé. Le demandeur doit soumettre la demande de renouvellement 90 jours avant l'expiration du certificat KGMP. La demande sera traitée par des auditeurs accrédités par le MFDS, et la documentation présentée pendant les trois (03) années de validité du certificat original sera examinée. Une fois l'inspection terminée, le certificat KGMP est renouvelé. L'évaluation pour le renouvellement du certificat KGMP dépend de la classe des dispositifs.
Type d'inspection | Classe II | Classe III | Classe IV |
Inspection initiale | Inspection sur site par un examinateur tiers | Inspection conjointe sur site (tiers et MFDS) | Inspection conjointe sur site (Tiers et MFDS) |
Inspection régulière | Inspection sur site par un examinateur tiers* | Inspection sur site par un examinateur tiers* | Inspection conjointe sur site (tiers et MFDS) |
Inspection supplémentaire | Examen des documents par un tiers | Examen des documents par un tiers | Examen des documents par un tiers |
Évaluation des changements | Examen des documents par un tiers | Examen des documents par un tiers | Examen des documents par un tiers |
* Soumis à une inspection conjointe en cas de préoccupations concernant la sécurité et l'efficacité pendant la période de trois ans
Les fabricants souhaitant pénétrer le marché sud-coréen doivent comprendre en profondeur les exigences KGMP établies par le MFDS. Les fabricants sont tenus de toujours maintenir les documents détaillés et le site de fabrication en conformité avec les normes KGMP. L'obtention de la certification KGMP peut être difficile pour les fabricants en raison du cadre réglementaire strict mis en place par le MFDS. Les fabricants peuvent opter pour un partenaire réglementaire expérimenté afin d'élaborer une stratégie appropriée et d'obtenir un certificat KGMP.
Pour en savoir plus sur les Bonnes Pratiques de Fabrication coréennes, contactez notre expert en réglementation.
