Les dispositifs médicaux innovants sont essentiels pour améliorer les résultats en matière de soins de santé, répondre aux besoins médicaux en constante évolution et offrir des solutions rentables aux patients et aux prestataires de soins. La stratégie SAKIGAKE est un processus d'examen et d'approbation accéléré pour les dispositifs médicaux innovants au Japon. Cette stratégie a été lancée par le ministère japonais de la Santé, du Travail et des Affaires sociales (MHLW) en 2015, dans le but d'accélérer le développement et la commercialisation des dispositifs médicaux innovants au Japon.
Dans le cadre de la stratégie SAKIGAKE, les dispositifs médicaux qui répondent à certains critères d'innovation peuvent bénéficier d'un examen et d'une approbation prioritaires de la part de l'Agence des produits pharmaceutiques et des dispositifs médicaux (PMDA), l'agence de réglementation responsable des approbations de dispositifs médicaux au Japon. Les critères de désignation pour l'innovation comprennent les éléments suivants :
- Dispositifs d'efficacité remarquable ; le dispositif est censé apporter un bénéfice clinique significatif grâce à un nouveau mécanisme d'action et une amélioration radicale pour les patients par rapport aux dispositifs médicaux existants.
- Premièrement, l'appareil peut être approuvé au Japon ou simultanément au Japon et dans d'autres pays.
- Le dispositif a le potentiel de répondre à des besoins médicaux non satisfaits au Japon. L'affection médicale ciblée doit être grave, potentiellement mortelle ou présenter des symptômes persistants.
Dans le cadre de la stratégie SAKIGAKE, les fabricants de dispositifs médicaux peuvent bénéficier d'une série d'avantages, notamment :
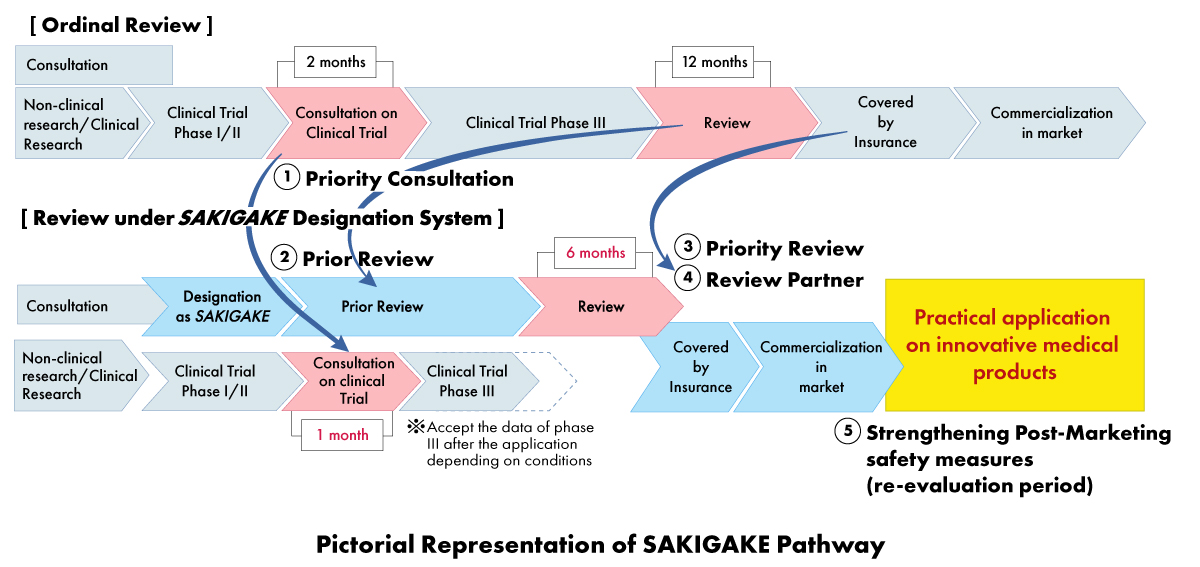
- Consultation prioritaire : Réduire le délai d'attente pour la consultation des essais cliniques à un (01) mois.
- Examen prioritaire : Les produits désignés SAKIGAKE bénéficient d'un examen prioritaire, l'objectif étant de finaliser le processus d'examen dans un délai de six (06) mois au lieu de 12 mois.
- Examen efficace avant la demande : Encourager la consultation et l'acceptation des documents en anglais.
- Partenaire d'examen dédié : Chaque produit désigné SAKIGAKE se voit attribuer un responsable d'examen dédié pour l'ensemble du processus d'approbation.
- Renforcement des mesures de sécurité post-commercialisation : Extension de la période de réexamen et facilitation de la connexion avec les sociétés scientifiques.
Comment postuler ?
- Par le demandeur : Le demandeur soumet la demande à la Division d'évaluation et d'autorisation de la PMDA (ELD).
- Par la PMDA-ELD : L'ELD approche un demandeur potentiel.
P.C- PMDA, Japon.
Dans l'ensemble, le système SAKIGAKE offre une voie accélérée pour le développement et l'approbation des dispositifs médicaux innovants au Japon. Il vise à améliorer les résultats pour les patients et à promouvoir l'innovation dans l'industrie des dispositifs médicaux. Le fabricant doit consulter la PMDA tôt dans le processus de développement pour discuter des exigences réglementaires et recevoir des commentaires sur ses plans de développement de produits.
Pour en savoir plus sur les voies d'enregistrement des dispositifs médicaux au Japon, contactez dès maintenant un expert en réglementation ! Restez informé. Restez conforme.
