
Une communication efficace a toujours garanti la sécurité et la qualité des soins pour les patients. Au fil des ans, le besoin de fournir des traductions d'étiquettes aux personnes ne maîtrisant pas l'anglais reste insatisfait. La demande d'étiquettes de produits dans plusieurs langues régionales a augmenté de manière exponentielle, les fabricants pharmaceutiques souhaitant favoriser la localisation et une meilleure communication.
Répondre à ces exigences améliorera la sécurité des patients tout en permettant la conformité aux exigences réglementaires spécifiques à chaque pays. L'absence d'informations médicales importantes dans les documents régionaux impose une charge supplémentaire aux pharmaciens et aux professionnels de la santé pour surmonter la barrière linguistique.
L'Autorité de Réglementation des Produits de Santé (HPRA) supervise la conformité réglementaire en Irlande. La HPRA facilite et collabore avec les parties prenantes en adhérant aux meilleures pratiques en matière d'étiquetage multilingue publiées par le Groupe de coordination pour la reconnaissance mutuelle et les procédures décentralisées – Humain (CMDh). En outre, la HPRA a également assoupli certaines conditions d'étiquetage, notamment :
- Utilisation de mL en Irlande (IE) par rapport à ml dans les autres États de l'UE.
- Utilisation des points décimaux dans le volume ou la concentration du produit et un point en IE par opposition à une virgule dans l'UE. Les fabricants de médicaments peuvent surmonter cette divergence en regroupant le nom inventé, la concentration et la forme pharmaceutique comme une seule unité dans chaque langue.
- Utilisation d'un séparateur pour la concentration ou le volume du produit - Un point dans l'UE contre une virgule en IE. L'utilisation de virgules comme séparateur est autorisée sur l'emballage extérieur immédiat afin d'éviter tout risque de confusion au sein de la population de patients irlandaise.
- Les petites unités de conditionnement primaire, c'est-à-dire les récipients d'une taille inférieure ou égale à 50 ml, ont une contrainte d'espace et peuvent contenir les informations minimales requises, lorsque cela est justifié, pour plus de deux (02) langues.
- Informations sur les pays tiers – lorsque les conditions d'information sur les produits sont similaires au Royaume-Uni et en Irlande, les emballages multi-pays sont acceptables. Des exigences supplémentaires spécifiques à chaque pays sont placées dans une « boîte bleue ».
- Coordination de l'évaluation avec les autres Member States - Les évaluations de maquettes réalisées par les Member States garantissent la conformité du labelling. Les demandeurs peuvent coordonner avec les Member States pour obtenir des éclaircissements sur les changements requis avant les soumissions à la HPRA.
- Noms conjoints - La mise en évidence de la proposition de nom inventé aux Member States doit être communiquée à la HPRA.
La HPRA émet les suggestions supplémentaires suivantes pour l'étiquetage multilingue :
- Les informations mentionnées en anglais doivent être regroupées dans un bloc.
- Mentionner les exigences de la « boîte bleue » pour tous les pays sur le même panneau lorsque plusieurs pays partagent un même emballage.
- Les informations destinées aux patients irlandais doivent être clairement indiquées dans un code ovale.
- Les demandeurs peuvent inclure une section perforée sur l'emballage, à condition que les données amovibles ne soient pas en anglais. Ceci doit être mentionné dans la soumission.
- Les demandeurs doivent soumettre un PDF de la notice à la HPRA à la fin du processus pour sa mise à jour sur le site web.
Critères pour un conditionnement multilingue :
- Le nom du produit et sa concentration doivent être identiques dans toutes les langues.
- Les informations figurant sur l'étiquetage et la notice doivent être conformes aux Résumés des Caractéristiques du Produit (SmPC).
- Les informations imprimées sur l'étiquetage et la notice doivent être exactes et lisibles.
- Le statut légal du médicament doit être similaire dans les deux pays.
Un exemple d'emballage multilingue serait :
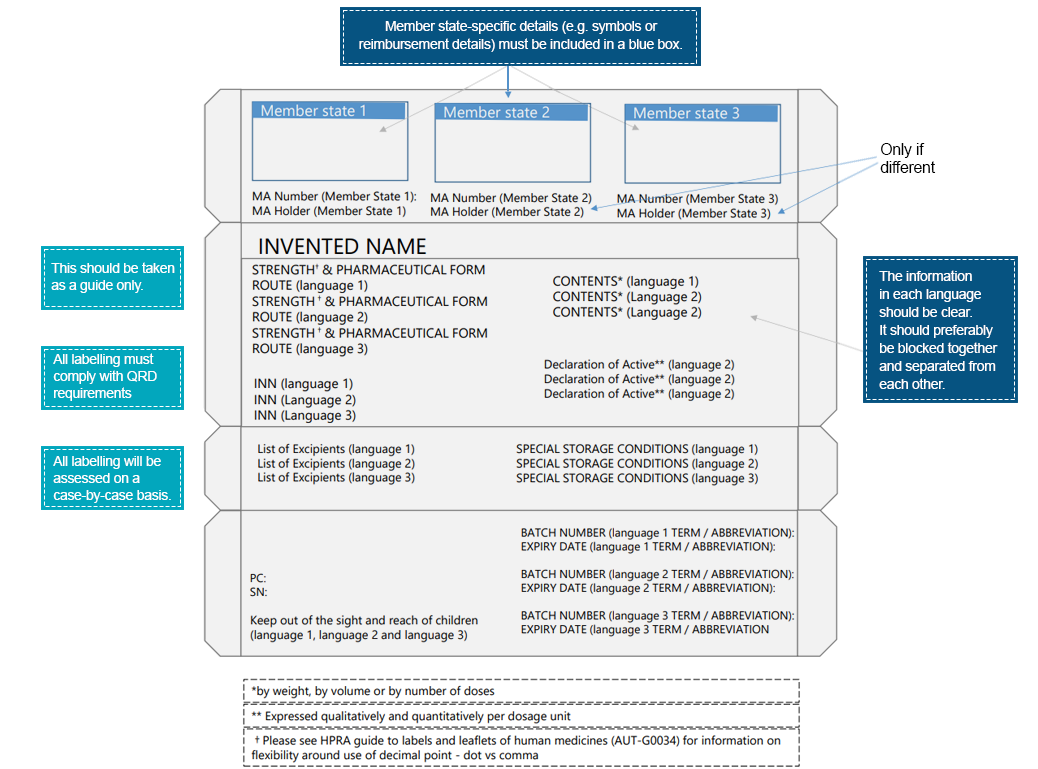
Les patients interagissent avec les étiquettes des médicaments bien avant d'interagir avec le produit médicamenteux lui-même. Ces interactions soulignent l'importance de transmettre des informations essentielles à travers les différents éléments de l'étiquette du médicament. Pour assurer une meilleure lisibilité et une amélioration des éléments de l'étiquette, les entreprises pharmaceutiques doivent prendre les mesures nécessaires. Les langues régionales offrent un moyen de transmettre des instructions médicales pertinentes pour le produit médicamenteux, garantissant ainsi une utilisation sûre et efficace du produit prescrit. Des experts en réglementation spécifiques à chaque pays peuvent aider à traduire les informations d'étiquetage conformément aux réglementations locales/régionales. Les experts de Freyr sont bien équipés pour aider à combler les lacunes entre l'information médicale et la langue. Contactez-nous pour une voie d'étiquetage conforme.










