
Le développement et l'approbation des médicaments pour enfants sont un aspect essentiel des soins de santé pédiatriques. Cependant, en raison de considérations éthiques et pratiques, les essais cliniques impliquant des enfants sont souvent limités. Par conséquent, l'étiquetage des médicaments pédiatriques joue un rôle crucial pour garantir l'utilisation sûre et appropriée des médicaments chez cette population vulnérable. Dans ce blog, nous comparerons les exigences en matière d'étiquetage des médicaments pédiatriques dans l'Union européenne (UE) et aux US afin de mieux comprendre les similitudes et les différences entre ces deux (02) cadres réglementaires.
Exigences d'étiquetage pédiatrique de l'UE
L'UE a des exigences spécifiques pour l'étiquetage pédiatrique des Produits médicaux. Ces exigences garantissent que les médicaments destinés aux enfants sont testés, autorisés et étiquetés de manière appropriée afin d'offrir des options de traitement sûres et efficaces aux patients pédiatriques.
Assurer la sécurité des médicaments pédiatriques. Contactez-nous
Assurer la sécurité des médicaments pédiatriques dès maintenant
Voici quelques aspects des exigences d'étiquetage pédiatrique de l'UE :
- Plans d'investigation pédiatrique (PIP) : Un PIP doit être soumis à l'Agence européenne des médicaments (EMA) avant qu'un médicament ne puisse être approuvé pour les enfants. Il décrit les études et les données nécessaires pour évaluer la sécurité, l'efficacité et la posologie du médicament chez les populations pédiatriques.
- Autorisation de mise sur le marché pour usage pédiatrique (PUMA) : Si un médicament a été étudié chez les enfants et répond aux exigences, il peut recevoir une PUMA. Cette autorisation permet de commercialiser le médicament pour un usage pédiatrique.
- Formulations adaptées à l'âge : Les médicaments à usage pédiatrique doivent être disponibles sous des formulations adaptées aux différentes tranches d'âge, telles que des liquides, des comprimés à croquer ou des dispositifs de dosage adaptés à l'âge.
- Résumé des Caractéristiques du Produit (SmPC) spécifique à la pédiatrie : Le SmPC est un document qui fournit des informations détaillées sur un médicament. Pour les produits pédiatriques, il doit inclure des détails spécifiques sur la posologie, l'administration et les considérations de sécurité pour les différents groupes d'âge.
- Avertissements et précautions pédiatriques : L'étiquetage doit inclure tout avertissement ou toute précaution spécifique liés à l'utilisation du médicament chez les enfants, tels que les effets secondaires potentiels ou les interactions avec d'autres médicaments couramment utilisés chez les patients pédiatriques.
- Surveillance continue et mises à jour : Une fois qu'un médicament est approuvé pour un usage pédiatrique, des études post-autorisation peuvent être nécessaires pour recueillir des données supplémentaires sur sa sécurité et son efficacité. Celles-ci peuvent entraîner des mises à jour de l'étiquetage si nécessaire.
Exigences en matière d'étiquetage pédiatrique US
Aux US, la Food and Drug Administration (FDA) a mis en œuvre la loi sur l'équité en matière de recherche pédiatrique (PREA) et la loi sur les meilleurs médicaments pour les enfants (BPCA) afin de promouvoir la recherche et l'étiquetage des médicaments pédiatriques. La PREA impose aux laboratoires pharmaceutiques de mener des études pédiatriques pour certains médicaments susceptibles d'être utilisés chez les enfants. La BPCA accorde six (06) mois supplémentaires d'exclusivité commerciale aux entreprises qui mènent ces études.
La FDA les directives supplémentaires suivantes afin de garantir la sécurité, l'efficacité et la posologie adéquate des médicaments pédiatriques :
- Plans d'études pédiatriques (PSP) : Les fabricants doivent soumettre des plans décrivant les études pédiatriques pour l'évaluation de la sécurité et de l'efficacité des médicaments.
- Informations spécifiques à l'âge : Les étiquettes doivent inclure des informations sur la posologie, les indications et les considérations de sécurité spécifiques à l'âge.
- Dosage en fonction du poids: Les recommandations de dosage dépendant du poids garantissent une administration précise.
- Réactions indésirables : Fournir des données sur les réactions indésirables et la sécurité spécifiques à la pédiatrie.
- Formulations pédiatriques spécifiques : Les médicaments peuvent nécessiter des formes posologiques spécifiques aux enfants (par exemple, des liquides et des comprimés à croquer).
- Ingénierie des facteurs humains : Les étiquettes doivent tenir compte de la facilité d'administration pour les soignants.
- Notices patient : Des instructions claires concernant l'administration, la posologie et les effets secondaires sont requises.
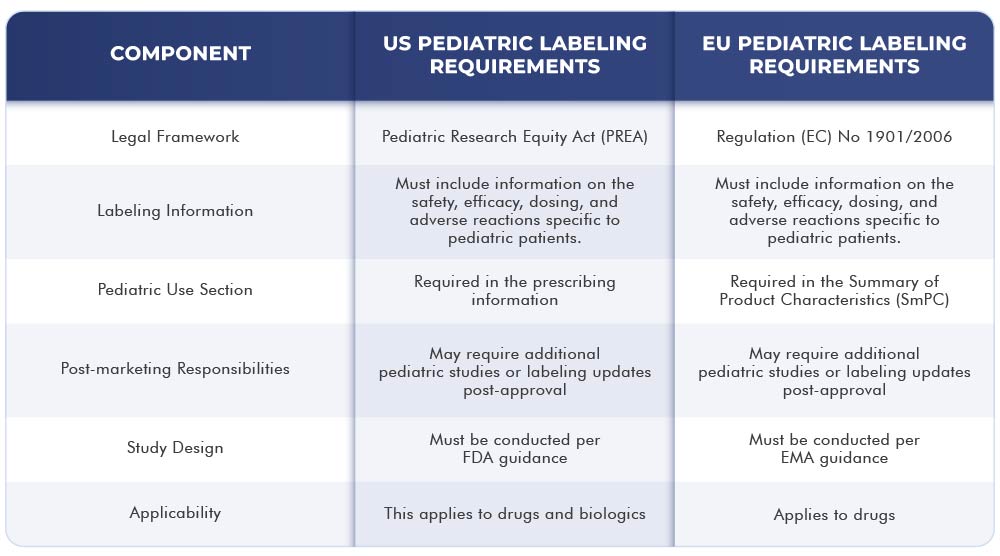
Le tableau ci-dessous présente les différences et les similitudes entre les exigences d'étiquetage US et UE :
Conclusion
Les exigences en matière d'étiquetage des médicaments pédiatriques dans l'UE et aux US visent à garantir l'utilisation sûre et appropriée des médicaments chez les enfants. Bien qu'il existe des similitudes entre les deux cadres réglementaires, telles que la nécessité d'études pédiatriques et l'inclusion d'informations spécifiques aux enfants dans l'étiquetage des médicaments, il existe également des différences notables. Comprendre ces similitudes et ces différences est crucial pour les entreprises pharmaceutiques, les professionnels de la santé et les régulateurs afin de garantir que les enfants aient accès à des médicaments sûrs et efficaces.
Consultez un expert en étiquetage confirmé comme Freyr pour la conformité aux exigences d'étiquetage spécifiques à chaque pays.










