
Étant donné que l'utilisation de produits pharmaceutiques peut avoir un impact significatif sur la santé et le bien-être d'un patient, les informations figurant sur l'étiquette doivent être claires et correctes. Cela est particulièrement vrai pour les instructions d'utilisation, les dates de péremption et les listes de composants. Ainsi, un audit des opérations d'étiquetage pharmaceutique est nécessaire.
En tant qu'aspect important de la conformité réglementaire, la précision des données est l'un des critères les plus critiques dans l'étiquetage des médicaments. Selon les études de la FDA et de la MHRA, environ 51 % des problèmes d'audit sont liés aux documents d'étiquetage.
Les cinq (05) problèmes d'audit les plus courants mis en évidence par les principales conclusions d'audit d'étiquetage des autorités sanitaires sont les suivants :
- Écart par rapport aux SOPs
- Informations CCDS & CSI
- Gestion des versions
- Suivi inefficace
- Décentralisation
Les problèmes énumérés ci-dessus peuvent survenir lors de fusions et acquisitions, de l'approbation de produits multiples dans plusieurs pays et de modifications de l'étiquetage local.
Principales raisons des problèmes d'audit de l'étiquetage pharmaceutique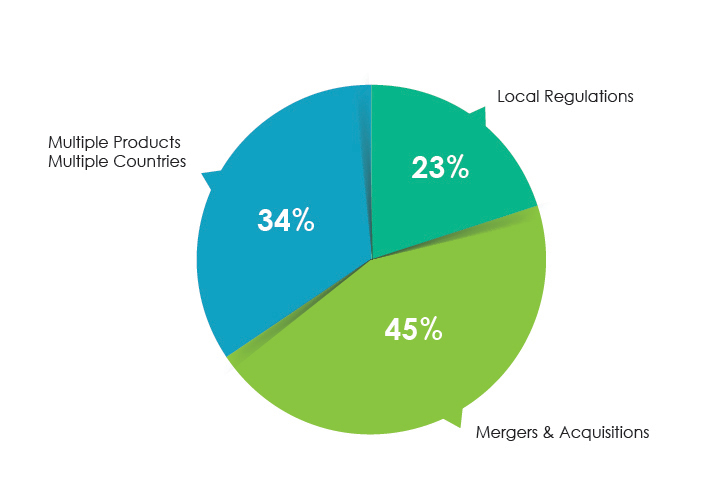
Le non-respect des exigences des normes réglementaires pour divulguer les informations de sécurité des produits, ou le partage de telles informations peut :
- Mettre en danger la sécurité du patient : Toute inexactitude dans l'étiquetage pourrait entraîner une mauvaise utilisation d'un médicament, provoquant des effets négatifs et, dans certains cas, pouvant être fatale.
- Être coûteux pour les organisations : Le rappel d'un produit en raison d'une erreur d'un élément labelling est un processus coûteux qui peut nuire aux résultats financiers d'une entreprise, que ce soit sa rentabilité ou son image de marque.
- Être chronophage : Lorsqu'il y a un manque d'informations sur un élément labelling, l'enquête sur un problème d'un élément labelling peut être chronophage pour l'autorité sanitaire.
- Nuire à la réputation : Une fois le produit retiré du marché, cela peut affecter l'image de marque et, par conséquent, nuire gravement à la réputation d'une organisation.
Dans de tels scénarios, comment vous assurez-vous que votre procédure d'étiquetage des produits pharmaceutiques répondra aux critères requis ?
Adopter l'automatisation pour la Conformité du labelling
L'automatisation, comme dans de nombreux autres domaines, est essentielle pour assurer la Conformité du labelling mondiale. De plus, l'automatisation réduit l'intervention humaine et assure le développement de livrables de haute qualité qui réduisent considérablement les coûts opérationnels globaux et améliorent le délai de mise sur le marché des gammes de produits de l'organisation.
Aujourd'hui, la meilleure méthode pour réussir à atteindre la conformité réglementaire du labelling est d'investir dans un outil complet de gestion du cycle de vie du labelling. En externalisant les opérations mondiales de labelling à des fournisseurs de logiciels spécialisés de gestion de labelling de bout en bout, les fabricants pharmaceutiques peuvent compter sur une gestion du labelling efficace et rationalisée.










