
Introduction
L'essor des produits biopharmaceutiques a véritablement révolutionné le domaine des sciences de la vie. Ces médicaments complexes à base de grosses molécules ont transformé le paysage des soins de santé, en proposant des traitements ciblés et efficaces pour toute une série de maladies. Alors que les produits biopharmaceutiques continuent de se développer, l'Agence américaine des produits alimentaires et médicamenteux (FDA) joue un rôle essentiel pour garantir leur sécurité et leur efficacité.
Dans cet article, nous nous penchons sur l'essor remarquable du secteur biopharmaceutique et examinons le point de vueFDA US sur ce domaine en pleine mutation. Nous abordons également le rôle crucial que jouent les prestataires de services réglementaires pour aider les entreprises à s'y retrouver dans les méandres de la réglementation biopharmaceutique.
Révolution des produits biopharmaceutiques
En raison de l'essor de la recherche et du développement, l'industrie biopharmaceutique a connu une croissance remarquable. Contrairement aux médicaments traditionnels à petites molécules, les produits biopharmaceutiques sont dérivés d'organismes vivants ou de processus biologiques, incluant les protéines, les acides nucléiques et les cellules. Ces molécules larges et complexes offrent plusieurs avantages, tels qu'une spécificité élevée et des effets secondaires réduits, ce qui les rend idéales pour traiter une variété de maladies, du cancer aux troubles auto-immuns.
L'évolution du rôle FDA
Face à l'essor de l'industrie biopharmaceutique, laFDA US FDA adapté son approche réglementaire afin de prendre en compte ces thérapies innovantes. La position de l'agence témoigne de sa volonté de favoriser l'innovation tout en garantissant les normes les plus strictes en matière de sécurité des patients.
- Équilibrer innovation et sécurité :
L'un des principaux défis auxquels la FDA dans la réglementation des produits biopharmaceutiques consiste à trouver le juste équilibre entre la promotion de l'innovation et la protection du bien-être des patients. Le développement de produits biopharmaceutiques peut être long et coûteux, et les procédures réglementaires doivent faire preuve de souplesse pour suivre le rythme des avancées scientifiques.
- Voies réglementaires pour les produits biopharmaceutiques :
La FDA différentes procédures réglementaires adaptées aux caractéristiques propres aux produits biopharmaceutiques. Cela comprend des procédures pour les biosimilaires, qui sont similaires mais non identiques à des produits biopharmaceutiques déjà autorisés, ainsi que des programmes d'examen accéléré pour les traitements innovants qui se révèlent très prometteurs dans le traitement de maladies graves.
- Assurer la qualité et l'efficacité :
La mission FDA en matière de produits biopharmaceutiques consiste notamment à garantir la qualité et l'efficacité de ces traitements. La fabrication de produits biopharmaceutiques est extrêmement complexe et exige un contrôle qualité rigoureux. La FDA étroitement avec les fabricants afin d'établir et de maintenir des normes élevées, notamment des processus et des contrôles rigoureux visant à réduire au minimum les variations dans les produits pharmaceutiques.
- Surveillance de la sécurité et surveillance après commercialisation :
Au-delà de l'autorisation initiale, FDA continue, après la mise sur le marché, à jouer un rôle dans la surveillance de la sécurité et de l'efficacité des produits biopharmaceutiques. Cela comprend la notification des effets indésirables, les inspections et les évaluations continues de la sécurité visant à identifier et à traiter les risques potentiels. La position de l'agence repose fermement sur son engagement à garantir que les bénéfices des produits biopharmaceutiques continuent de l'emporter sur les risques éventuels.
- Promouvoir les approches centrées sur le patient :
La positionFDA US s'inscrit dans la tendance du secteur vers des soins de santé centrés sur le patient. Elle encourage la participation des communautés de patients et des parties prenantes au processus réglementaire, garantissant ainsi que la voix des patients soit entendue et que leurs besoins soient pris en compte dans l'évaluation des produits biopharmaceutiques.
- Favoriser la collaboration mondiale :
L'essor des produits biopharmaceutiques a dépassé les frontières nationales. La FDA collabore FDA avec les agences réglementaires internationales afin d'établir des lignes directrices harmonisées pour le développement et l'autorisation de mise sur le marché de ces traitements. Ces collaborations contribuent à rationaliser le développement mondial des produits biopharmaceutiques, rendant ainsi ces traitements innovants accessibles à un plus grand nombre de patients.
Rôle des fournisseurs réglementaires
Les fournisseurs de services réglementaires peuvent agir comme des partenaires stratégiques à l'ère des produits biopharmaceutiques en aidant les entreprises pharmaceutiques à naviguer dans ce paysage complexe :
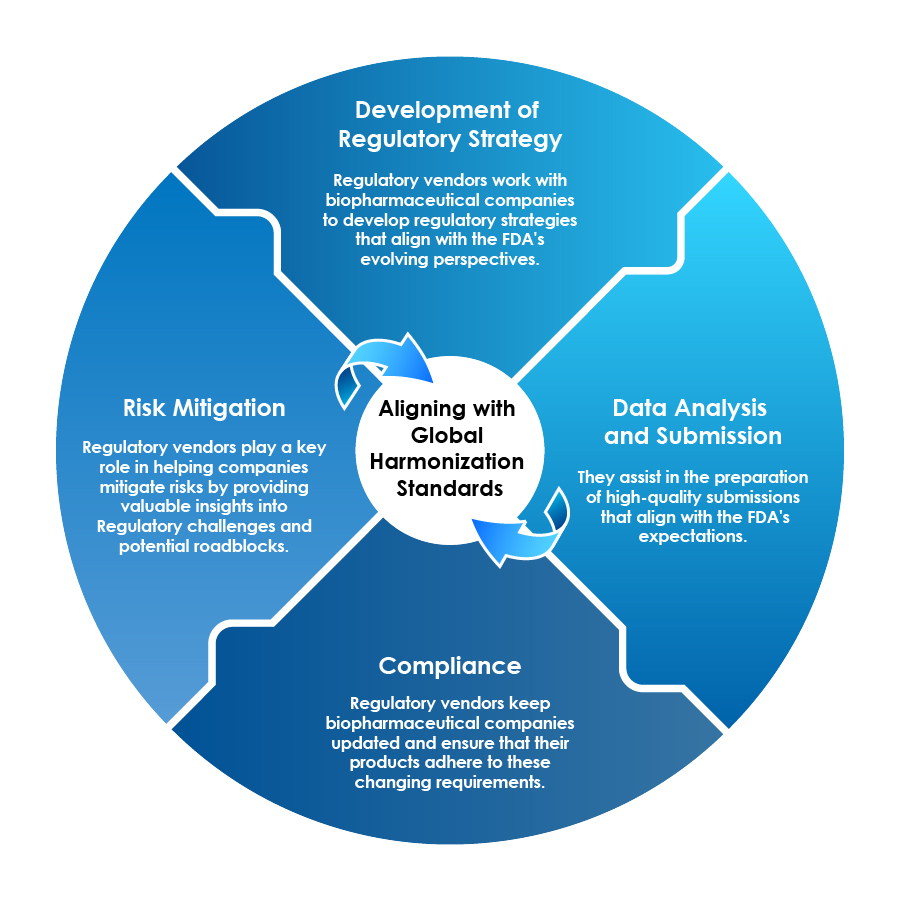
Les fournisseurs de services réglementaires assurent l'alignement avec les normes mondiales
Conclusion
L'essor des produits biopharmaceutiques marque un tournant majeur dans le domaine de la santé, en proposant des traitements ciblés et efficaces pour diverses maladies. La position FDA témoigne d'une adaptation et d'une innovation constantes dans les approches réglementaires relatives au développement biopharmaceutique. De plus, les prestataires de services réglementaires, en tant que partenaires essentiels, veillent à ce que les entreprises biopharmaceutiques parviennent à s'y retrouver dans ce paysage complexe, en facilitant le parcours menant de l'innovation à la mise sur le marché.
La synergie entre la FDA les prestataires spécialisés dans la réglementation permet au secteur de répondre aux exigences en constante évolution des soins aux patients et de tracer la voie vers un avenir marqué par des innovations biopharmaceutiques révolutionnaires. Chez Freyr, nos experts maîtrisent parfaitement ces enjeux réglementaires ; n'hésitez pas à nous contacter pour en savoir plus.










