
Les étiquettes des médicaments servent de guide direct pour les utilisateurs et contribuent à une utilisation qualitative des produits. Il est donc primordial que les informations figurant sur les étiquettes soient cohérentes, faciles à lire, exemptes d'erreurs et conformes aux normes mondiales. Afin de s'y aligner, la Therapeutic Goods Administration (TGA) a apporté quelques modifications à la manière dont les informations d'étiquetage sont présentées sur les produits. L'objectif de ces changements est d'améliorer la clarté et la cohérence des informations fournies aux professionnels de la santé.
Quels sont les nouveaux changements d'étiquetage ?
Bien que les nouvelles informations soient déjà prises en compte et mises en œuvre par les fabricants, il est judicieux de les connaître en détail pour une présentation complète. Voici quelques-unes d'entre elles sur lesquelles les fabricants doivent travailler lors de la définition de leurs étiquettes de médicaments.
1. Informations sur la substance active
Selon la nouvelle règle, les ingrédients actifs devraient être :
- Placé de manière plus visible sur la face avant de l'emballage du médicament
- Devrait être placé en dessous ou à côté du nom du médicament sur le devant de l'emballage du médicament
- Doit être facilement comparable entre les médicaments
2. Informations sur les médicaments
Pour s'assurer que les utilisateurs et les professionnels de la santé prennent une décision éclairée, les informations sur le médicament devraient être plus claires en termes de :
- Informations de santé essentielles sur des étiquettes distinctives
- Toutes les informations obligatoires doivent être présentées de manière plus claire et plus reconnaissable sur le fond, afin d'améliorer leur lisibilité.
- Les substances à déclarer, telles que les allergènes, doivent être mentionnées sur l'étiquette
3. Informations de santé essentielles
Les informations de santé essentielles aident les consommateurs à utiliser le médicament en toute sécurité en fournissant des renseignements importants. Les informations figurant dans le tableau des informations de santé essentielles seront toujours dans le même ordre, bien qu'il puisse y avoir une légère différence dans la présentation de ces informations. Les informations de santé essentielles comportent les titres et informations suivants, dans le même ordre :
- Principes actifs : Nom du principe actif et sa quantité
- Indications : Utilisation du médicament.
- Avertissements : Comprend des déclarations d'avertissement, des déclarations consultatives et des avertissements supplémentaires concernant l'utilisation du médicament sous la rubrique « Mode d'emploi ».
- Mode d'emploi : Comprend des informations sur l'utilisation sûre du médicament.
- Autres informations : Comprend des informations telles que les détails de stockage, les dispositifs de protection contre l'altération, les coordonnées du promoteur, la liste des ingrédients, etc. Cette partie peut ne pas figurer sur tous les médicaments.
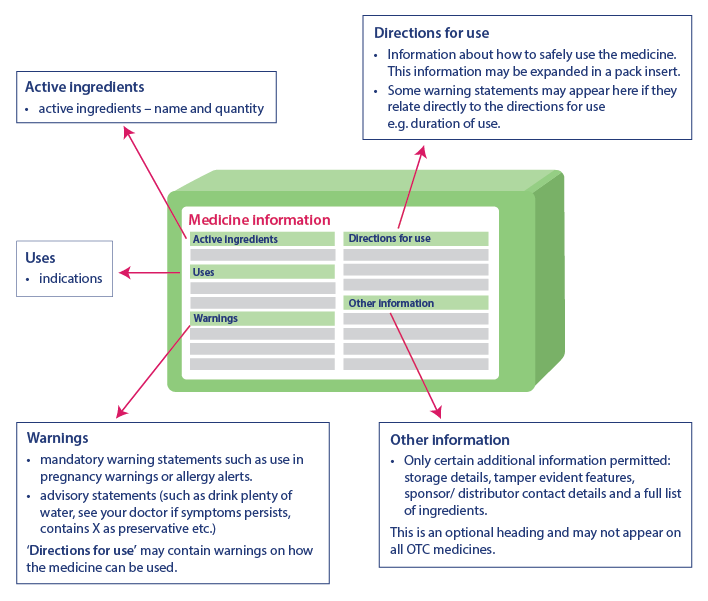
Source : TGA
4. Délivrance en pharmacie
Selon la nouvelle règle, les changements suivants sont apportés aux distributeurs de médicaments :
- Pour améliorer l'identification des médicaments, les boîtes de médicaments sur ordonnance doivent afficher leur nom sur les trois côtés non opposés.
- Les étiquettes des médicaments sur ordonnance doivent disposer d'un espace dédié de 70x30 millimètres, sauf s'ils sont fournis dans un emballage primaire ou un kit de démarrage.
5. Informations sur les allergènes
Les médicaments doivent indiquer les informations suivantes sur les étiquettes :
- Si présentes dans le médicament, toutes les substances doivent être déclarées sur l'étiquette.
- Des substances supplémentaires, telles que les crustacés, le poisson, les œufs, le soja, le lait et les fruits à coque, doivent être déclarées sur l'étiquette
- Dans le cas de nouveaux allergènes, les fabricants ne peuvent pas les inclure avant la fin de la période de transition de 4 ans.
Bien que la TGA ait publié ces informations pour les professionnels de la santé, nous considérons cela comme une exigence essentielle pour les fabricants également, afin d'étiqueter leurs produits de manière exhaustive. Ainsi, les professionnels de la santé peuvent consulter les informations mises à jour sans confusion et guider les patients pour une consommation sûre. Il est bien connu que la TGA a accordé aux fabricants une période de transition de quatre ans pour mettre en œuvre ces changements. Après la date définie, les étiquettes des médicaments doivent être conformes aux nouvelles exigences d'étiquetage. Restez informé. Restez conforme.










