Le Shonin (autorisation de mise sur le marché) est la voie réglementaire pour l'enregistrement des dispositifs médicaux au Japon. La voie Shonin est principalement destinée à l'enregistrement des dispositifs médicaux de classe II et III pour lesquels les normes de classification de la PMDA ne sont pas disponibles. Pour les dispositifs de classe IV à haut risque également, les fabricants doivent soumettre la demande Shonin. La PMDA est responsable de l'examen et de l'approbation de la demande Shonin.
Quelles sont les autres voies d'enregistrement des dispositifs au Japon ?
Outre Shonin, les voies Todokede et Ninsho sont également utilisées pour les approbations de dispositifs médicaux au Japon. Les fabricants de dispositifs médicaux peuvent choisir l'une d'entre elles en fonction de la classe de risque du dispositif et de la disponibilité de dispositifs prédicats au Japon. Le fabricant doit identifier la classification du dispositif et rechercher la disponibilité de la norme industrielle japonaise (JIS) avant de déterminer la voie d'enregistrement applicable.
- Todokede (Soumission avant commercialisation) – Elle s'applique aux dispositifs de Classe I et exige des fabricants qu'ils soumettent une notification avant commercialisation à la PMDA pour approbation.
- Ninsho (Certification avant commercialisation) – Elle est applicable aux dispositifs génériques de classe II et III disposant de normes de certification (normes JIS). L'organisme de certification enregistré (RCB) est responsable de l'examen et de l'approbation de la demande.
Quels sont les prérequis pour l'enregistrement Shonin ?
Les fabricants qui enregistrent leurs dispositifs par la voie Shonin doivent planifier méticuleusement les soumissions. Ils doivent s'assurer des éléments suivants :
- Soumission de données générales sur les dispositifs, telles que la catégorie de dispositif médical, l'utilisation prévue, les données d'analyse des risques d'efficacité, les données cliniques, etc.
- Fournir le Résumé de la Documentation Technique (STED)
- Fourniture des documents uniquement en japonais
- Les fabricants étrangers sont tenus de désigner un titulaire de l'autorisation de mise sur le marché (MAH) ou un titulaire désigné de l'autorisation de mise sur le marché (TDAMM)
- Les fabricants étrangers doivent obtenir un certificat d'enregistrement de fabricant étranger (FMR) pour leurs établissements de fabrication.
Quelles sont les exigences SGC pour l'enregistrement des dispositifs selon la voie Shonin ?
Les fabricants doivent se conformer à toutes les exigences relatives au système de gestion de la qualité (SGQ) définies dans l'ordonnance n° 169. Le promoteur, le DMAH ou MAH introduire une demande auprès de la PMDA. La PMDA à une inspection approfondie du SGQ dans les locaux du fabricant et délivre le certificat dès lors que la mise en œuvre du SGQ est jugée satisfaisante.
Quel est le processus d'enregistrement pour l'approbation des dispositifs selon la voie Shonin ?
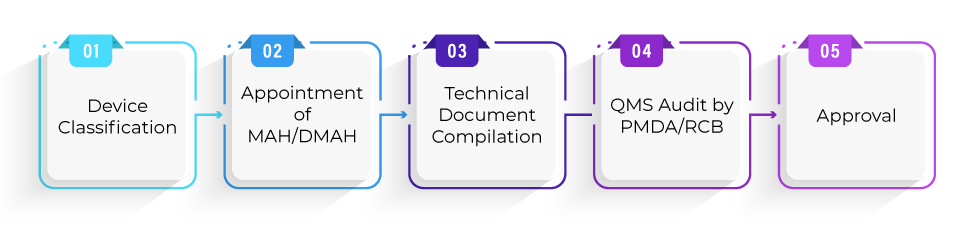
Quel est le délai moyen requis pour l'approbation des dispositifs dans le cadre de la procédure Shonin ?
La PMDA exige généralement 12 mois pour l'évaluation technique à compter de la date de réception de la demande de Shonin. Le fabricant doit prendre en compte le temps nécessaire à la préparation des documents de soumission ou à la réalisation des études cliniques dans le calendrier de son projet.
Y a-t-il un délai d'expiration pour l'enregistrement des dispositifs selon la voie Shonin ?
L'enregistrement des dispositifs médicaux n'expire pas, mais le promoteur doit renouveler les certificats QMS tous les cinq (05) ans.
Le Japon est un marché lucratif, mais il présente intrinsèquement des complexités réglementaires et des barrières linguistiques. Les fabricants doivent prendre en compte ces facteurs et planifier de manière proactive leur stratégie de mise sur le marché (GTM) pour le Japon. Les fabricants de dispositifs médicaux et de DIV peuvent choisir d'externaliser toutes les subtilités réglementaires à un partenaire réglementaire fiable et d'utiliser leurs ressources pour se concentrer sur d'autres éléments essentiels.
Pour en savoir plus sur l'approbation des dispositifs médicaux Shonin au Japon ou sur toute autre réglementation de la PMDA Japon, contactez dès aujourd'hui les experts en réglementation de Freyr.
