L'application des technologies logicielles dans diverses gestions de soins de santé, y compris le diagnostic ou le traitement d'une maladie, s'accélère à un rythme sans précédent. Les autorités mondiales des dispositifs médicaux révisent leurs réglementations et directives pour faire face à ces technologies de dispositifs en plein essor. En Australie, la Therapeutic Goods Administration (TGA) est l'autorité réglementaire responsable de la surveillance des dispositifs médicaux, y compris les logiciels et les applications mobiles. En janvier 2021, la TGA a publié le projet initial de réglementation des logiciels de dispositifs médicaux, qui a été révisé en février 2021. Le 27 juillet 2021, la TGA a publié un organigramme détaillé abordant les ambiguïtés courantes que les fabricants de dispositifs et les professionnels de la réglementation peuvent avoir concernant la classification des logiciels de dispositifs médicaux.
La TGA identifie les logiciels utilisés dans le domaine des dispositifs médicaux comme étant des Logiciels en tant que dispositif médical (SaMD), des Logiciels intégrés à un dispositif médical (SiMD) et des Logiciels qui contrôlent les dispositifs médicaux. Selon la TGA, le terme Logiciel en tant que dispositif médical (ou SaMD) désigne tout logiciel pouvant fonctionner sur un ordinateur portable, un smartphone ou une tablette dont la finalité prévue relève des normes d'un dispositif médical. En revanche, le SiMD est un logiciel qui fait partie intégrante d'un dispositif et est généralement important pour le bon fonctionnement de celui-ci. Certains logiciels contrôlent les dispositifs médicaux soit physiquement, soit via des connexions sans fil comme le Bluetooth, le Wi-Fi, etc. La TGA réglemente les trois (03) types de logiciels.
Peu de logiciels de dispositifs médicaux sont exclus ou exemptés de la réglementation de la TGA sur les logiciels en tant que dispositifs médicaux, sur la base des principes d'alignement de la réglementation avec les normes internationales et de réduction de la charge par la non-réglementation des produits, lorsqu'il n'y a pas de risque majeur pour la sécurité et que des structures ou cadres appropriés pour les contrôles du produit ou du système sont déjà en place.
| Dispositifs logiciels exemptés | Dispositifs logiciels exclus |
|---|---|
Par exemple, Peu de systèmes d'aide à la décision clinique qui répondent à trois critères principaux : 1. Si le logiciel n'est pas destiné à analyser ou traiter une image médicale. 2. Le logiciel est uniquement destiné à fournir un soutien/une recommandation au professionnel de la santé. 3. Le logiciel n'est pas destiné à remplacer le jugement clinique du professionnel. | Les produits qui ne relèvent pas de la catégorie des dispositifs médicaux et ne sont soumis à aucune exigence réglementaire de la TGA sont appelés dispositifs logiciels exclus. Par exemple,
|
La TGA a révisé la réglementation des dispositifs médicaux comprenant des logiciels qui contrôlent ou interagissent avec d'autres dispositifs médicaux, que ce soit en externe ou en interne, ainsi que les logiciels qui fonctionnent comme un dispositif médical (à part entière). Les changements majeurs incluent l'introduction de nouvelles règles de classification, clarifiant la délimitation des produits logiciels réglementés, et les principes essentiels ont été mis à jour pour clarifier les exigences relatives aux dispositifs médicaux basés sur des logiciels.
Avec l'introduction de nouvelles règles de classification, certains dispositifs médicaux basés sur des logiciels sont reclassés dans des classes de risque plus élevées et doivent subir des procédures d'évaluation de la conformité pertinentes. Les promoteurs et fabricants de ces dispositifs reclassés doivent être inscrits à l'ARTG (Australian Register of Therapeutic Goods) avant le 25 février 2021. Les fabricants et promoteurs qui ont déjà soumis une demande à la TGA avant le 25 février 2021, doivent soumettre un formulaire de notification à la TGA.
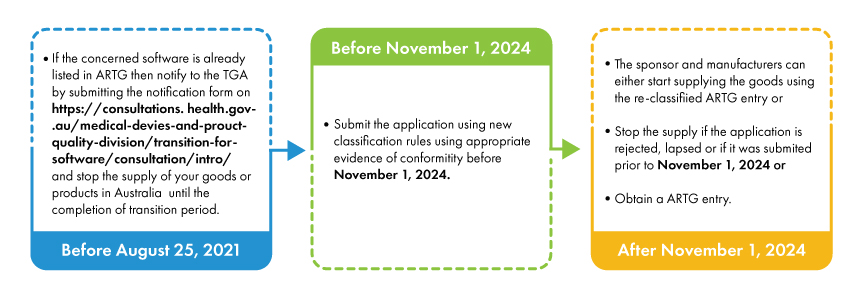
Classification des logiciels de dispositifs médicaux en Australie :
Les fabricants doivent spécifier l'usage prévu du SaMD, ce qui aidera à la classification et aux procédures d'évaluation de la conformité. La nouvelle réglementation introduit également de nouvelles règles de classification pour les dispositifs médicaux programmés et programmables ou les logiciels en tant que dispositifs médicaux, et la classe du logiciel dépendra de la gravité de la maladie surveillée/traitée.
![]()
Modifications des principes essentiels :
Voici les modifications apportées aux principes essentiels à compter du 25 février 2021, au dispositif médical logiciel.
Les modifications apportées par la TGA à la réglementation des logiciels peuvent alléger le fardeau du fabricant pour catégoriser ses logiciels comme réglementés ou non réglementés et peuvent faciliter la préparation en temps voulu des documents requis pour l'évaluation de la conformité de la TGA.
Tous les scénarios étant décodés, souhaitez-vous faire inscrire votre logiciel au Registre australien des produits thérapeutiques (ARTG) avec moins de contraintes ? Pour l'inscription à l'ARTG de dispositifs médicaux, de DIV ou de SaMDs, contactez un expert. Restez informé. Restez conforme.