
Le schéma thérapeutique médicamenteux est varié pour les médicaments qui peuvent être approuvés pour être utilisés en association avec un médicament précédemment approuvé ou pour deux nouveaux médicaments développés simultanément qui améliorent l'efficacité de manière synergique. Les monothérapies anticancéreuses ont montré de manière significative que la résistance aux médicaments constitue une menace majeure pour les patients sous traitement anticancéreux. Compte tenu de la diversité des thérapies combinées adoptées pour les traitements du cancer, les schémas thérapeutiques à deux médicaments remplacent progressivement la monothérapie comme norme de soins chez les patients. Au cours de la décennie, la thérapie combinée a offert de meilleures perspectives de traitement.
Si vous êtes une organisation bien consciente du changement de paradigme dans le développement des médicaments anticancéreux, passant du développement de médicaments uniques à des combinaisons innovantes, vous devez savoir que ce progrès a entraîné une augmentation des demandes d'approbation de demandes de cross-labeling par le demandeur. En tenant compte des discussions, des dernières tendances de l'industrie et de sa compréhension actuelle des exigences d'un promoteur, la US Food and Drug Administration (USFDA) a publié un ensemble de lignes directrices pour apporter un soutien concernant les modifications d'étiquetage pour les régimes médicamenteux avec des produits pharmaceutiques déjà approuvés.
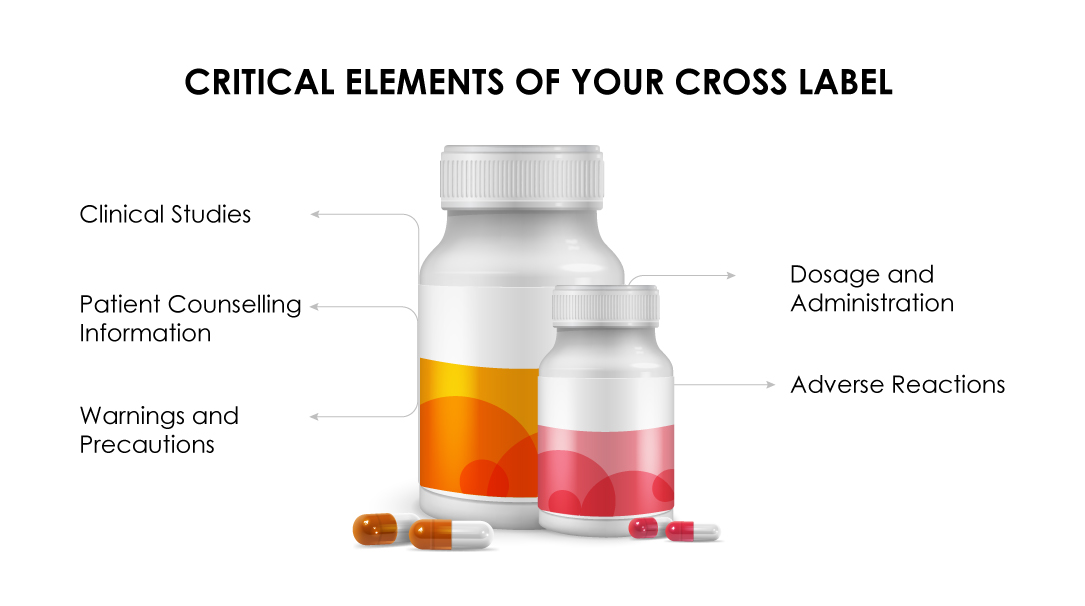
Félicitations ! Votre demande de directives sur l'étiquetage croisé a été accordée, si :
"(a) L'indication pour le régime de combinaison demandé est approuvée dans le cadre d'une
"(b) La section
"(c) Les
(d) La section « Avertissements et précautions » doit mentionner le caractère unique du traitement combiné en s'appuyant sur des données cliniquement significatives.
(e) Les effets indésirables doivent être mis en évidence tels qu'observés lors des essais cliniques.
(f) La notice d'information destinée aux patients doit se limiter aux effets indésirables spécifiques à la formulation.
Les informations relatives au médicament du promoteur uniquement doivent occuper les sections restantes de l'étiquette, à moins que des facteurs pharmacocinétiques uniques ne doivent être mentionnés.
Le guide approuvé pour l'étiquetage croisé cible spécifiquement les produits de thérapie anticancéreuse afin d'établir la compréhension fondamentale de l'étiquetage croisé. Pour aider les promoteurs face aux obstacles opérationnels et réglementaires concernant le changement d'étiquette, le guide stipule :
- Délais
Les demandeurs sont censés proposer le contenu préliminaire pour l'étiquetage croisé, avec une justification basée sur des preuves du rôle de chaque produit mentionné dans le régime, dans leur proposition d'étiquetage croisé d'un nouveau médicament anticancéreux dans une demande pré-NDA ou BLA.
L'étiquetage croisé est censé être identifié pour chaque médicament du régime thérapeutique en même temps. Cependant, l'approbation peut être accordée l'une après l'autre, de manière séquentielle, en raison des différences de calendrier des médicaments.
- Soumission réglementaire
Chaque demandeur souhaitant un étiquetage croisé doit déposer une demande originale ou un supplément d'efficacité pour l'étiquetage croisé.
Un demandeur peut choisir de faire référence aux données d'autres applications pour justifier les avantages synergiques du régime combiné.
Lorsqu'il fait référence à des données, le demandeur :
- doit s'assurer que les données référencées ont déjà été déposées auprès de la FDA.
- doit annoter chaque section des données du demandeur qui est référencée.
- devrait inclure (section ci-dessous) uniquement les informations pertinentes pour le médicament du demandeur :
- MISE EN GARDE ENCADRÉE (Le cas échéant)
- FORMES ET DOSAGES
- CONTRE-INDICATIONS
- INTERACTIONS MÉDICAMENTEUSES
- UTILISATION DANS DES POPULATIONS SPÉCIFIQUES
- SURDOSAGE
- DESCRIPTION
- PHARMACOLOGIE CLINIQUE
- TOXICOLOGIE NON CLINIQUE
- RÉFÉRENCES
- PRÉSENTATION / STOCKAGE ET MANIPULATION
L'étiquetage croisé pour les médicaments anticancéreux peut aider à informer la population de patients sur le dosage, l'efficacité et les avantages des résultats du traitement. Avec l'augmentation exponentielle de la thérapie combinée comme méthode standard, les étiquettes croisées peuvent s'avérer bénéfiques pour l'amélioration ou l'introduction des méthodes thérapeutiques actuelles. Nos experts chevronnés chez Freyr maîtrisent parfaitement les défis de l'étiquetage dynamique et peuvent apporter des solutions à vos questions d'étiquetage. Bénéficiez d'un soutien professionnel en matière d'étiquetage de la plus haute qualité. Contactez Freyr !










