Le Ninsho (certification des dispositifs médicaux) est un système de certification par une tierce partie au Japon où un organisme de certification enregistré (RCB), accrédité par le ministre de la Santé, du Travail et des Affaires sociales (MHLW), certifie les dispositifs médicaux hautement contrôlés désignés. Il s'applique aux dispositifs de classe II et à un nombre limité de dispositifs de classe III qui sont associés à une norme industrielle japonaise (JIS). Quelques dispositifs médicaux de classe II sans critères de certification établis nécessitent une approbation dans le cadre du programme Shonin.
Quelles sont les autres voies d'enregistrement des dispositifs au Japon ?
Au Japon, les voies Todokede et Shonin sont également utilisées pour les approbations de dispositifs médicaux, en plus de Ninsho. En fonction de la catégorie de risque du dispositif et de la disponibilité de dispositifs de référence au Japon, le fabricant doit planifier soigneusement sa demande d'autorisation de dispositif.
Quels sont les prérequis pour la certification Ninsho ?
Les fabricants qui enregistrent leurs dispositifs par la voie Ninsho doivent planifier méticuleusement les soumissions en ce qui concerne les éléments suivants :
- Sélection d'un RCB
- Soumission de données générales sur les dispositifs, telles que la catégorie de dispositif médical, l'utilisation prévue, les données d'analyse des risques d'efficacité, les données cliniques, etc.
- Fournir le Résumé de la Documentation Technique (STED)
- Les documents doivent être fournis uniquement en japonais
- Les fabricants étrangers sont tenus de désigner un titulaire de l'autorisation de mise sur le marché (MAH) ou un titulaire désigné de l'autorisation de mise sur le marché (TDAMM)
- Les fabricants étrangers doivent s'enregistrer auprès du MHLW et obtenir un certificat d'enregistrement de fabricant étranger (FMR) pour leurs établissements de fabrication.
Que sont les RCB ?
Les Organismes de Certification Enregistrés (RCBs) sont des organismes de certification tiers accrédités par le MHLW. Les RCBs sont responsables de l'examen et de la certification des dispositifs médicaux éligibles et soumis dans le cadre de la procédure Ninsho. Les RCBs sont également responsables de la réalisation de l'audit du système de gestion de la qualité (QMS) des installations du fabricant.
Quelles sont les exigences SGC pour l'enregistrement des dispositifs selon la voie Ninsho ?
Les fabricants doivent se conformer à toutes les exigences relatives au système de gestion de la qualité (SGQ) définies dans l'ordonnance n° 169. Le MAH le titulaire désigné de l'autorisation de mise sur le marché (TDAMM) doit soumettre la demande aux autorités de contrôle régionales (ACR). Les ACR procéderont à une inspection approfondie du SGQ dans les locaux du fabricant et, si la mise en œuvre du SGQ est jugée satisfaisante, délivreront le certificat.
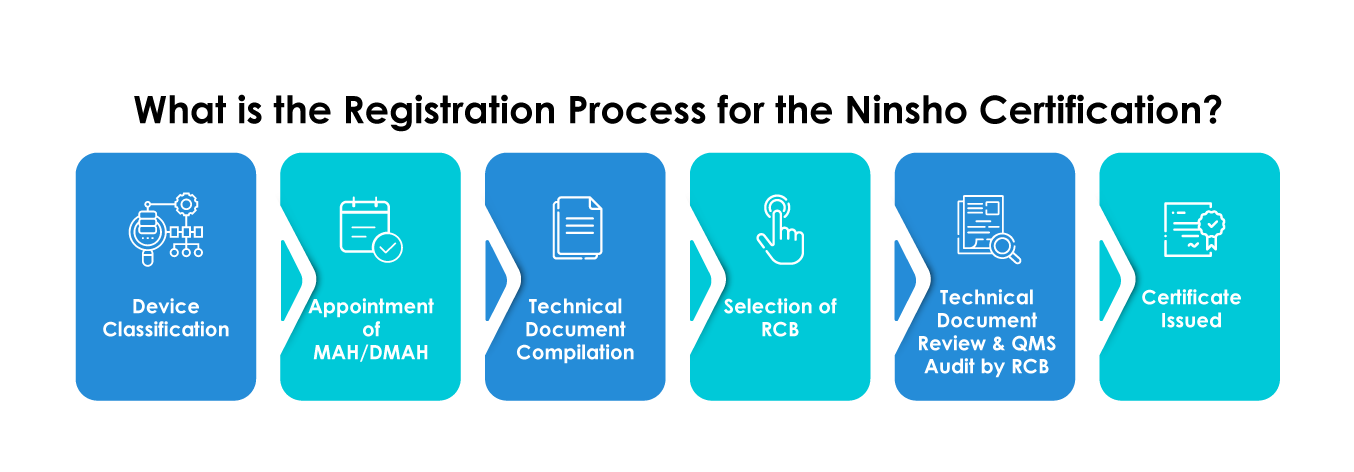
Quel est le délai moyen requis pour la certification Ninsho ?
L'organisme de certification et d'enregistrement (RCB) a généralement besoin de trois (03) à cinq (05) mois pour finaliser l'évaluation technique, effectuer l'audit du SMQ et délivrer le certificat Ninsho.
Y a-t-il un délai d'expiration pour la certification Ninsho ?
L'enregistrement des dispositifs médicaux n'expire pas, mais le promoteur doit renouveler les certificats QMS tous les cinq (05) ans.
Le Japon, étant le troisième plus grand marché pour les dispositifs médicaux après les US et la Chine, offre de grandes opportunités aux fabricants de dispositifs médicaux du monde entier. Les fabricants souhaitant commercialiser leurs dispositifs au Japon doivent planifier soigneusement la certification et l'approbation des dispositifs médicaux, car la PMDA a des exigences réglementaires spécifiques. Les fabricants peuvent opter pour un partenaire réglementaire fiable pour un accès sans tracas au marché japonais.
Pour en savoir plus sur la certification des dispositifs médicaux au Japon ou toute autre réglementation de la PMDA Japon, contactez Freyr dès aujourd'hui !
