
Les logiciels de dispositifs médicaux en Corée du Sud sont utilisés pour diagnostiquer, traiter et surveiller les patients dans le système de santé moderne. Ils comprennent à la fois des logiciels embarqués intégrés aux dispositifs médicaux et des logiciels autonomes pouvant être utilisés sur des PC, des appareils mobiles et des services web. Le ministère de la Sécurité alimentaire et pharmaceutique (MFDS) de Corée du Sud est responsable de la réglementation des logiciels de dispositifs médicaux et de la garantie de leur sécurité et de leur efficacité. Le 5 juillet 2023, le MFDS a établi des critères pour l'approbation et l'inspection des logiciels de dispositifs médicaux ; ces réglementations fournissent une structure que les demandeurs peuvent suivre lors de la soumission de logiciels pour approbation ou examen.
La réglementation aborde divers sujets, notamment le champ d'application, les exigences en matière de documentation technique et les rapports de vérification de la conformité. Outre les directives de la MFDS, il existe des normes et des lignes directrices internationales applicables aux logiciels destinés aux dispositifs médicaux, telles que la norme 62304 de la Commission électrotechnique internationale (CEI) relative aux processus du cycle de vie des logiciels et les recommandations de la Food and Drug Administration (FDAUS concernant les applications médicales mobiles.
Plan de développement logiciel et analyse des exigences
- Le plan de développement logiciel décrit l'approche globale du développement logiciel, y compris les spécifications, les méthodes et les outils de développement. Il couvre également la vérification, la gestion des risques des dispositifs médicaux, la gestion de la configuration et la documentation.
- Analyse des exigences établit les exigences logicielles des dispositifs médicaux, y compris les mesures de contrôle des risques et les méthodes de vérification. En planifiant et en analysant soigneusement le processus de développement logiciel, les développeurs peuvent s'assurer que le logiciel résultant répond aux normes nécessaires de sécurité et d'efficacité.
- Le rapport de vérification de la conformité logicielle comprend une description du plan de développement logiciel, le numéro de contrôle des documents du fabricant et un aperçu de l'analyse des exigences. En adhérant à ces directives, les logiciels de dispositifs médicaux peuvent être développés en toute confiance, sachant qu'ils ont subi des tests rigoureux et répondent aux normes nécessaires de sécurité et d'efficacité.
Vérification et validation des logiciels de dispositifs médicaux
- Vérification des logiciels de dispositifs médicaux : La vérification des logiciels de dispositifs médicaux garantit que le logiciel répond aux exigences spécifiées.
- Validation des logiciels de dispositifs médicaux : La validation des logiciels de dispositifs médicaux garantit que le logiciel répond aux besoins de l'utilisateur et à l'utilisation prévue.
- Le rapport de vérification et de validation du logiciel de dispositif médical décrit le processus de vérification et de validation, y compris le nom du produit, sa révision et les noms des personnes qui ont examiné et approuvé le rapport. Le rapport peut varier en fonction des caractéristiques du logiciel, mais il doit inclure une description du logiciel, les méthodes de vérification et de validation utilisées, ainsi que les résultats des tests.
Environnement d'exploitation et logiciel de provenance inconnue (SOUP)
- Si le logiciel dépend d'un matériel spécifique, tel qu'un logiciel embarqué, le document technique doit décrire les spécifications matérielles.
- Cependant, si le logiciel est autonome et conçu pour fonctionner sur du matériel à usage général, l'environnement d'exploitation doit être décrit dans les spécifications brutes. Cela inclut les spécifications minimales recommandées, telles que Microsoft Windows 10 ou version ultérieure.
- De plus, si le logiciel de dispositif médical inclut un Logiciel Commercial de Provenance Inconnue (SOUP), un environnement d'exploitation doit être créé pour assurer son bon fonctionnement. En décrivant soigneusement l'environnement d'exploitation et en gérant tout SOUP, les développeurs peuvent s'assurer que leur logiciel de dispositif médical est sûr et efficace pour l'usage auquel il est destiné.
Gestion des risques et exigences en matière de documentation pour les dispositifs médicaux
- Le processus de gestion des risques des logiciels en tant que dispositifs médicaux comprend l'identification des situations dangereuses, l'établissement de mesures de contrôle des risques, la vérification de ces mesures et la gestion des modifications logicielles.
- Le document de gestion des risques logiciels MFDS-RM fournit des informations sur la gestion des risques logiciels.
- De plus, les exigences en matière de documentation sont essentielles pour garantir que le logiciel respecte les normes nécessaires de sécurité et d'efficacité.
- Le plan de développement logiciel, l'analyse des exigences logicielles des dispositifs médicaux, ainsi que les rapports de vérification et de validation logicielles doivent être inclus dans la documentation.
- Le rapport de vérification de la conformité logicielle décrit les exigences en matière de documentation ; il inclut également un aperçu des documents applicables et le numéro de contrôle des documents du fabricant.
Figure 1 : Processus de gestion des risques des dispositifs médicaux
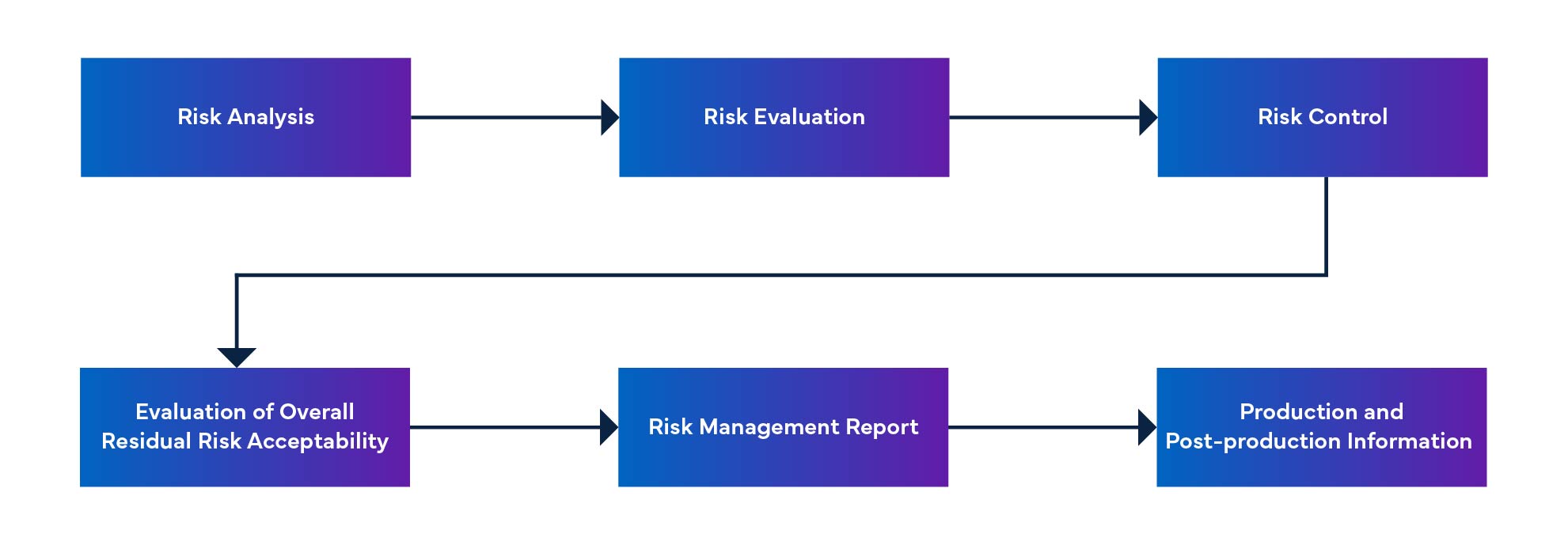
Anomalies non résolues et actions correctives pour les logiciels SaMD
- Le document MFDS-PR (résolution des problèmes logiciels) décrit le processus de résolution des problèmes logiciels, qui comprend le signalement des problèmes, l'analyse, la mise en œuvre et la vérification.
- Le document comprend également une liste des problèmes non résolus, des bogues, des défauts et des anomalies, ainsi qu'une évaluation des risques résiduels pour le système logiciel.
- Les actions correctives prises pour résoudre ces problèmes doivent être documentées dans le plan de maintenance logicielle, qui est établi conformément au processus de maintenance logicielle.
- Le document de maintenance du MFDS fournit des informations sur la maintenance et le dépannage des logiciels SaMD.
Exigences de révision et de soumission des documents techniques pour les logiciels SaMD
Les principaux documents d'examen au cours du processus d'examen sont les données de performance, le rapport de confirmation de conformité, les données de vérification et de validation du logiciel de dispositif médical, la Spécification de Conception Logicielle (SDS), l'Énoncé des Exigences Logiciel du dispositif médical (SRS), et les rapports de vérification et de validation. Le Rapport de Confirmation de Conformité et le Rapport de Vérification et de Validation du Logiciel de Dispositif Médical doivent être soumis.
Gestion des risques des logiciels de dispositifs médicaux
- Identifier les dangers potentiels liés au logiciel et à son utilisation.
- Évaluation de la gravité des risques associés à ces dangers.
- Mise en œuvre de mesures de contrôle des risques pour minimiser la probabilité de préjudice.
- Suivi et examen de l'efficacité de ces mesures de maîtrise des risques.
- Documenter toutes les activités et décisions relatives à la gestion des risques des dispositifs médicaux.
Dans un système logiciel, les éléments logiciels sont décomposés en parties plus petites, y compris des éléments logiciels détaillés. Lorsqu'un élément ne peut plus être décomposé, il est appelé une unité. Le système permet une décomposition jusqu'au niveau de l'unité, ce qui aide à déterminer le niveau de sécurité pour chaque élément logiciel. En assemblant ces éléments logiciels, nous sommes en mesure de déterminer le niveau de sécurité de l'ensemble du système logiciel.
Figure 2 : Désassemblage et intégration des logiciels de dispositifs médicaux
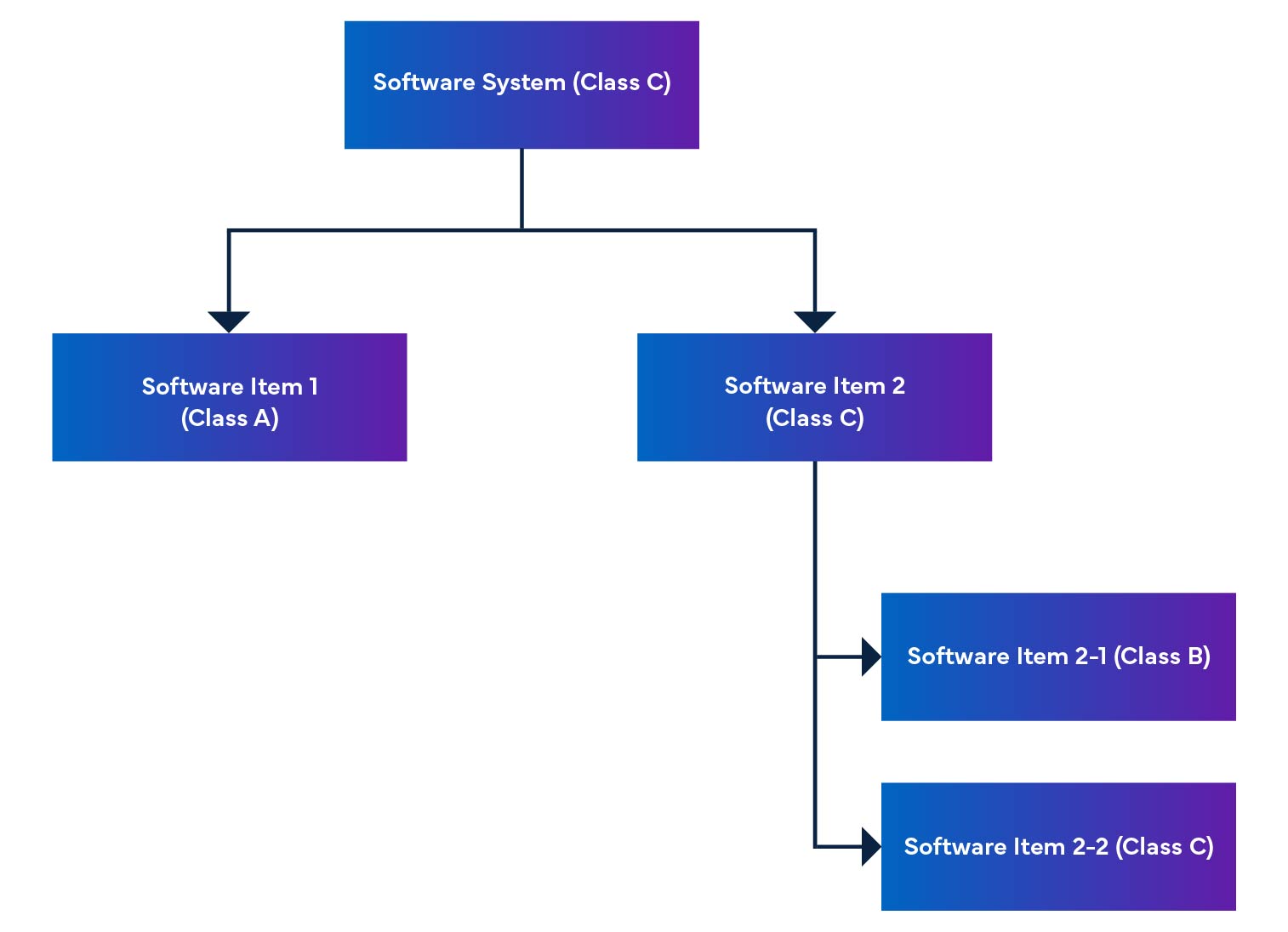
La réglementation mentionne également la classification de sécurité des logiciels, qui est une évaluation permettant d'identifier les risques des logiciels SaMD (voir Tableau 1).
Tableau 1 : Définition de la classification de sécurité
| Notation | Définition de la classe de sécurité des logiciels de dispositifs médicaux |
| Classe A | Aucune possibilité de blessure ou de dommage corporel. |
| Classe B | Des blessures moins graves (blessures mineures) sont probables. |
| Classe C | Possibilité de blessures graves ou de décès. |
Gestion de la configuration logicielle
- Maintenir une documentation précise et à jour pour toutes les versions logicielles, les modifications et les mises à jour.
- S'assurer que toute la documentation est correctement examinée et approuvée.
- Mise en place de procédures pour gérer les modifications de configuration logicielle.
- Documentation de toutes les activités et décisions de gestion de la configuration logicielle.
Maintenance logicielle
- Tester et surveiller régulièrement le logiciel pour s'assurer qu'il reste sûr et efficace pour l'usage auquel il est destiné.
- Mise en place de procédures pour traiter tout problème pouvant survenir, y compris les corrections de bugs et les mises à jour logicielles.
- Documentation de toutes les activités et décisions de maintenance logicielle.
Résolution de problèmes
- Identifier la cause première du problème.
- Mise en œuvre d'actions correctives pour résoudre le problème.
- Documentation de l'ensemble du processus de dépannage pour consultation ultérieure.
En suivant les directives ci-dessus, les développeurs peuvent s'assurer que tout problème lié à leur logiciel de dispositif médical est correctement traité et documenté, et que le logiciel répond aux exigences nécessaires pour l'approbation ou l'examen.
Si vous êtes un fabricant de dispositifs médicaux visant la conformité avec les normes logicielles des dispositifs médicaux sud-coréens, les experts en réglementation de Freyr peuvent vous guider à travers le paysage réglementaire complexe du pays. Nous veillerons à ce que vos dispositifs s'alignent sur les dernières réglementations sud-coréennes en matière de dispositifs médicaux pour une conformité sans faille. Contactez-nous pour en savoir plus !










