
Dans le secteur pharmaceutique actuel, fortement réglementé, le respect des bonnes pratiques (GxP) n'est pas seulement une obligation légale, c'est aussi un engagement en faveur de la sécurité des patients et de la qualité des produits. Alors que les autorités réglementaires du monde entier, notamment la FDA EMA, accordent une attention croissante aux contrôles de fabrication et à la cohérence des produits, la vérification continue des processus (CPV) s'est imposée comme une méthodologie révolutionnaire permettant de garantir GxP constant GxP tout au long du cycle de vie des produits.
Comprendre la vérification continue des processus
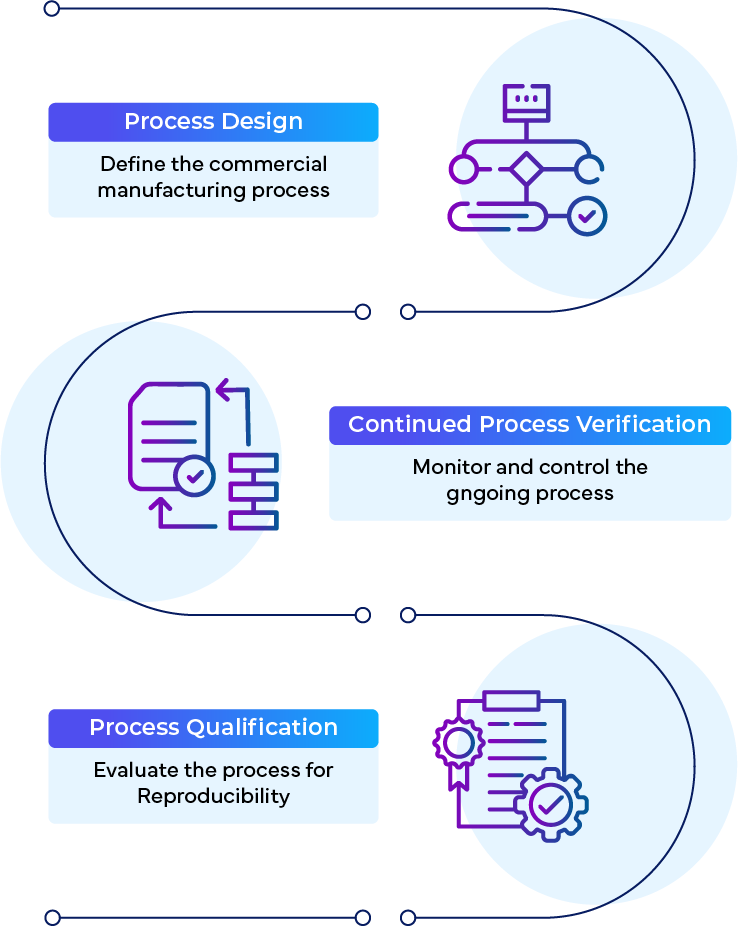
La CPV est l'une (1) des trois (3) étapes prévues dans les lignes directrices FDArelatives à la validation des procédés :
- Conception des processus
- Qualification des procédés
- Vérification continue des processus
Contrairement aux approches de validation traditionnelles, qui s'appuient souvent largement sur des données limitées issues de lots pré-commercialisation, la CPV met l'accent sur la collecte de données en temps réel et l'analyse des tendances au cours de la production courante. Ce passage d'une gestion de la qualité réactive à une gestion proactive permet aux fabricants de détecter les écarts de processus, d'atténuer les risques à un stade précoce et de maintenir un état validé tout au long du cycle de vie commercial du produit.
Pourquoi le CPV change la donne
d'assurance qualité en temps réel En collectant et en analysant les données à chaque cycle de production, CPV permet de détecter immédiatement les anomalies. Ces informations en temps réel facilitent la prise de décision, réduisent le risque de commercialisation de produits non conformes et évitent les rappels coûteux.- Amélioré Conformité réglementaire
Les autorités réglementaires attendent de plus en plus des entreprises pharmaceutiques qu'elles mettent en œuvre des approches de validation basées sur le cycle de vie. CPV répond à cette attente en démontrant un contrôle continu, en s'alignant sur les lignes directrices ICH , Q9 et Q10, et en garantissant la conformité aux exigences réglementaires mondiales. - Optimisation des coûts
Bien que la mise en œuvre du CPV nécessite un investissement initial dans les technologies d'analyse et la formation, elle permet à terme de réduire les coûts à long terme. Elle minimise la nécessité de revalidations fréquentes, diminue les rejets de lots et améliore l'efficacité de la production. - Prise de décision fondée sur les données
CPV s'appuie sur des outils statistiques avancés et l'automatisation pour traiter de vastes quantités de données. Cette approche structurée de la gestion des données facilite la planification stratégique, l'amélioration continue et la gestion éclairée des risques, qui constituent les piliers des systèmes de qualité modernes.
Meilleures pratiques de mise en œuvre
1. Définir les paramètres critiques de processus (CPP)
Commencez par identifier et définir les CPP et les attributs critiques de qualité (CQA) à partir des données historiques et expérimentales. Ces indicateurs constituent la base de la surveillance en temps réel.
2. Tirer parti des outils numériques et de l'automatisation
Intégrez le logiciel CPV à vos systèmes d'exécution de la fabrication (MES) et à vos systèmes de gestion de l'information de laboratoire (LIMS). L'automatisation améliore la précision et la fréquence des données, ainsi que la visualisation des tendances.
3. Collaboration interfonctionnelle
La mise en œuvre réussie du CPV nécessite une coordination entre les équipes chargées de l'assurance qualité, de la fabrication et de l'informatique. La mise en place d'une stratégie CPV unifiée garantit la cohérence et une responsabilité partagée.
4. Développer des modèles d'analyse de données robustes
Utiliser le contrôle statistique des processus (SPC), l'analyse multivariée et les algorithmes d'apprentissage automatique pour analyser les tendances, prévoir les écarts et favoriser l'amélioration continue.
5. Harmonisation réglementaire
Documentez chaque étape de votre processus CPV et assurez-vous que votre système est prêt pour un audit. Alignez votre documentation et vos pratiques sur les exigences réglementaires internationales.
Le CPV en pratique : un exemple concret
Prenons l'exemple d'une entreprise pharmaceutique qui fabrique des produits injectables stériles. Avant la mise en œuvre du CPV, ses efforts de validation se concentraient principalement sur trois (3) lots pré-commercialisation. Les variations post-commercialisation passaient souvent inaperçues jusqu'à ce que des réclamations concernant le produit soient formulées.
En adoptant le CPV, l'entreprise a déployé des capteurs de température et de pression en temps réel sur l'ensemble de sa chaîne de production. Les données ont été analysées en continu à l'aide de graphiques SPC. Cela a permis de détecter un écart mineur mais récurrent dans le volume de remplissage, suffisamment tôt pour prendre des mesures correctives avant que cet écart n'affecte la qualité du produit. Cette transition a non seulement garanti GxP , mais a également permis de réduire considérablement les temps d'arrêt et les retouches sur les produits.
Conclusion
La vérification continue des processus ne se résume pas à une simple formalité réglementaire. Il s'agit d'une approche stratégique visant à garantir une qualité constante des produits, l'efficacité opérationnelle et la conformité aux GxP en constante évolution. Grâce à des outils adaptés, un état d'esprit adéquat et les conseils d'experts, les entreprises pharmaceutiques peuvent transformer leurs programmes de validation et assurer une conformité durable.
Laissez Freyr vous guider dans votre parcours CPV
Chez Freyr, nous sommes spécialisés dans les services end-to-end et de conformité destinés à l'industrie pharmaceutique. Que vous en soyez aux prémices de la mise en œuvre de votre système de CPV ou que vous souhaitiez améliorer votre système actuel, nos experts peuvent vous aider à concevoir, déployer et valider des cadres CPV robustes et adaptés à vos besoins.
Prêt à améliorer votre GxP ? Contactez Freyr dès aujourd'hui pour découvrir comment nous pouvons vous aider à pérenniser vos opérations pharmaceutiques.










