
Le Règlement sur les dispositifs médicaux (MDR) de l'Union européenne (UE) fait l'actualité depuis un certain temps. Le MDR a remplacé la Directive sur les dispositifs médicaux (MDD) et la Directive sur les dispositifs médicaux implantables actifs (AIMDD). Initialement, la transition complète devait être effective d'ici mai 2020 ; cependant, en raison de l'émergence de la pandémie de COVID-19, la mise en œuvre a été repoussée au 26 mai 2021. Dans ce calendrier, d'ici le 26 mai 2024, tous les certificats MDD deviendront caducs, et les fabricants de dispositifs devront se conformer à l'EU MDR. En outre, les dispositifs MDD légalement mis sur le marché conformément aux Directives 90/385/CEE et 93/42/CEE avant le 26 mai 2020, et les dispositifs mis sur le marché à partir du 26 mai 2020 en vertu d'un certificat, continueront d'être disponibles sur le marché jusqu'au 27 mai 2025. Les échéances sont représentées ci-dessous –
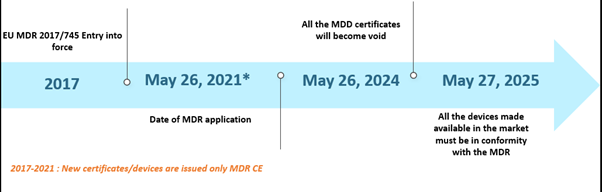
L'EU MDR : Chronologie des scénarios passés
Cependant, la capacité limitée des organismes notifiés (ON) et le manque de préparation des fabricants ont posé des défis dans la mise en œuvre du MDR selon le calendrier donné. En octobre 2022, il y avait au total trente-huit (38) organismes notifiés (ON), et ces ON ont reçu environ 8120 demandes de certification EU MDR, dont 1990 certificats ont été délivrés. Selon leurs estimations avec le calendrier initial, seuls 7000 certificats pouvaient être traités, ce qui a conduit à la prolongation du délai. De plus, l'une des autres raisons probables de la prolongation était d'assurer la disponibilité continue de dispositifs médicaux sûrs dont les certificats avaient déjà expiré ou devaient expirer avant le 26 mai 2024. Le scénario actuel pour le calendrier prolongé est décrit ci-dessous :
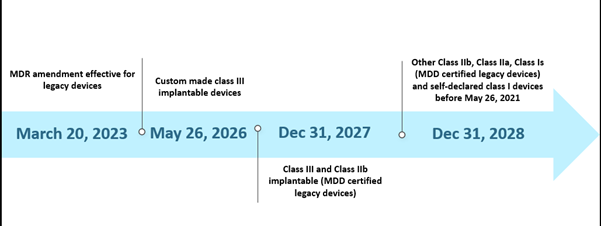
L'EU MDR : Chronologie des scénarios passés
La nouvelle prolongation s'applique aux dispositifs existants (legacy devices) remplissant l'article 120 (3e) avec un marquage CE MDD valide ou une dérogation au 20 mars 2023, et restera sur le marché aux côtés des dispositifs marqués CE MDR. D'ici le 26 mai 2024, les fabricants de dispositifs existants devront avoir mis en place un système de gestion de la qualité (QMS) et déposé une demande d'évaluation de la conformité auprès d'un organisme notifié (NB) désigné MDR, et d'ici le 26 septembre 2024, les fabricants de dispositifs existants devront avoir conclu un accord avec un organisme notifié (NB) désigné MDR.
Examinons maintenant l'impact que cette prolongation pourrait avoir sur les fabricants.
Opportunités pour les fabricants avec cette extension :
- Accès étendu au marché pour les fabricants de dispositifs certifiés MDD/AIMDD qui ont déjà pris les initiatives de conformité au MDR.
- Les fabricants certifiés MDR dont les certificats CE MDD/AIMDD n'ont pas été révoqués sont autorisés à mettre sur le marché des dispositifs existants jusqu'à la fin de la période de transition, en plus de leurs dispositifs conformes au MDR.
- Les fabricants qui bénéficient d'une dérogation nationale au 20 mars 2023 peuvent bénéficier de la période de transition.
- La période de prolongation permet de gagner du temps pour une meilleure compréhension des règles et réglementations, ce qui contribue à rationaliser le processus et à atteindre la conformité au MDR.
Défis qui pourraient survenir pour les fabricants avec cette extension :
- Il n'y a aucun avantage commercial pour les fabricants d'anciens dispositifs qui n'ont pas souhaité se conformer au MDR.
- La prolongation du MDR peut entraîner la prolongation des processus de certification et retarder les lancements de produits, ce qui est une conséquence directe de l'arriéré des examens par les organismes notifiés (ON).
Quelles actions les fabricants doivent-ils prendre ?
- Il est impératif que les fabricants déterminent la classe de risque MDR de leur dispositif médical afin d'identifier rapidement le calendrier de transition approprié, conformément aux réglementations MDR modifiées.
- Pour assurer la conformité avec les réglementations MDR, il est crucial d'identifier et d'initier la communication avec les NBs désignés MDR possédant la compétence spécifique requise pour la classification de votre dispositif médical.
- Il est essentiel de réaliser une évaluation complète des écarts pour votre dispositif médical certifié selon la MDD/AIMDD, d'identifier et de corriger toute non-conformité avec les réglementations MDR et d'assurer une conformité rapide.
Il est essentiel pour les fabricants de prendre des mesures immédiates pour assurer la conformité au MDR. Le calendrier prolongé offre des opportunités aux fabricants pour atteindre la conformité au MDR, mais il présente également des défis, tels que des processus de certification retardés et le coût de la conformité. Pour relever ces défis et capitaliser sur les opportunités, laissez notre équipe de professionnels vous assister tout au long du processus de conformité au MDR et assurer votre succès dans cet environnement réglementaire exigeant. Prenez rendez-vous avec nous dès aujourd'hui pour en savoir plus sur la façon dont nous pouvons vous aider à atteindre la conformité au MDR et à garder une longueur d'avance. Restez informé. Restez conforme.









