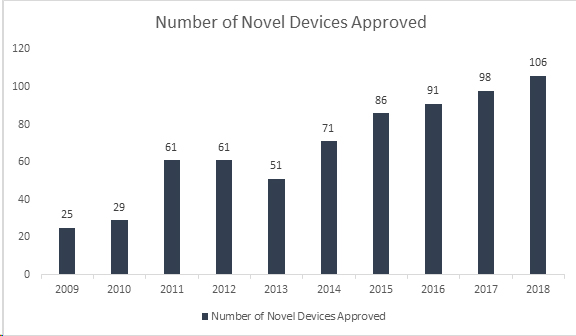
Le saviez-vous ? L'Agence US et médicamenteux (FDA) a établi un nouveau record en approuvant 106 nouveaux dispositifs médicaux en 2018, faisant de cette année la plus fructueuse jamais enregistrée dans ce domaine. Grâce à cette performance, FDA dépassé son record vieux de 40 ans, établi en 2017 avec 99 dispositifs approuvés, et affiche ainsi une croissance continue depuis huit ans. Parmi les dispositifs approuvés figurent toute une gamme de produits innovants, tels que des systèmes automatisés d'administration d'insuline pour les enfants, la plus petite valve cardiaque au monde destinée aux nouveau-nés, la première application médicale mobile destinée à aider à la prise en charge des troubles liés à l'abus d'opioïdes et de substances, ainsi que des technologies d'intelligence artificielle permettant de diagnostiquer la rétinopathie diabétique.
FDA toujours encouragé la sécurité et l'innovation dans le domaine des dispositifs médicaux afin de garantir leur haute qualité. Pour faire face à l'augmentation du nombre d'autorisations accordées à ces nouveaux dispositifs et en garantir la sécurité, FDA de « moderniser » la procédure d'autorisation des dispositifs médicaux. Selon l'agence, cette modernisation pourrait nécessiter la création d'une nouvelle autorité. En 2018, FDA le Center for Devices and Radiological Health (CDRH) ont publié un document conjoint indiquant que la procédure 510(k) était l'un des deux types de demande ajoutés à la définition des dispositifs innovants. Par ailleurs, les exemptions pour dispositifs humanitaires (HDEs) ont également été ajoutées à la définition des dispositifs innovants à la suite des modifications apportées au programme des dispositifs médicaux révolutionnaires du CDRH en vertu de la loi 21st Century Act.
La proposition de la FDA du CDRH répond à la nécessité potentielle d'obtenir de nouveaux pouvoirs pour moderniser la procédure 510(k). L'objectif de cette proposition est de limiter l'utilisation de dispositifs de référence, considérés comme « substantiellement équivalents » (SE), datant de plus de dix ans, afin de favoriser l'innovation. Il s'agit d'une avancée par rapport aux lignes directrices publiées par l'agence en avril 2018. Le projet a été publié par la FDA proposer l'extension du programme 510(k) abrégé au sein du CDRH FDAsous le titre « Safety and Performance-based Pathway » (Voie fondée sur la sécurité et la performance). Il a été introduit pour alléger la charge réglementaire pesant sur les dispositifs médicaux. Cette approche vise également à accroître l'efficacité de l'examen des demandes 510(k), réduisant ainsi la pression sur l'agence.
Voici quelques-uns des points saillants des lignes directrices :
- Cette nouvelle voie évalue la sécurité et l'efficacité des dispositifs par rapport à des normes de sécurité et des critères de performance établis.
- Malgré les nouvelles normes, les dispositifs devront être conformes aux normes existantes pour être commercialisés.
- La technologie moderne sera testée selon les normes modernes
- Cette approche favorisera une plus grande concurrence pour le développement de dispositifs plus sûrs.
Le nombre de dispositifs médicaux soumis à autorisation a augmenté de manière exponentielle au fil des ans. Cela a donné à la FDA une grande latitude FDA adopter et mettre en œuvre des mesures innovantes visant à améliorer les procédures d'autorisation. L'agence est fermement convaincue du bien-fondé de cette proposition, mais la réaction du secteur reste encore à déterminer.
La FDA publiant FDA de nouveaux documents d'orientation visant à améliorer l'enregistrement des dispositifs médicaux, il est indispensable que les fabricants de dispositifs médicaux se tiennent informés de ces évolutions et s'y conforment. Restez à jour. Restez en conformité.