24 septembre 2016 ; à un mois seulement de la date limite de conformité à l'identifiant unique de dispositif (UDI) pour les dispositifs de Classe II, nous supposons, si ce n'est une certitude, que tous les fabricants de dispositifs médicaux sont bien préparés avec une feuille de route réglementaire complète. Outre une solide maîtrise des prérequis de gouvernance, les fabricants doivent être prêts pour les audits de conformité. De la validation des enregistrements d'identifiant de dispositif (DI) et d'identifiant de produit (PI) aux soumissions GUDID réussies, ils doivent maîtriser les données à soumettre et les procédures à suivre. Que ce soit avant ou après la soumission, une meilleure connaissance du savoir-faire procédural pourrait protéger les fabricants des défis correspondants liés à l'agrégation des données, à la soumission des enregistrements DI, à la gestion des rapports de dispositifs, au suivi des accusés de réception des autorités compétentes, etc.
Pour mieux outiller les fabricants dans de tels scénarios, nous proposons ici une infographie facile à comprendre sur les défis et les solutions de la conformité UDI, qui pourrait vous faire gagner du temps pour décoder les complexités de la conformité et mieux planifier et structurer la feuille de route.
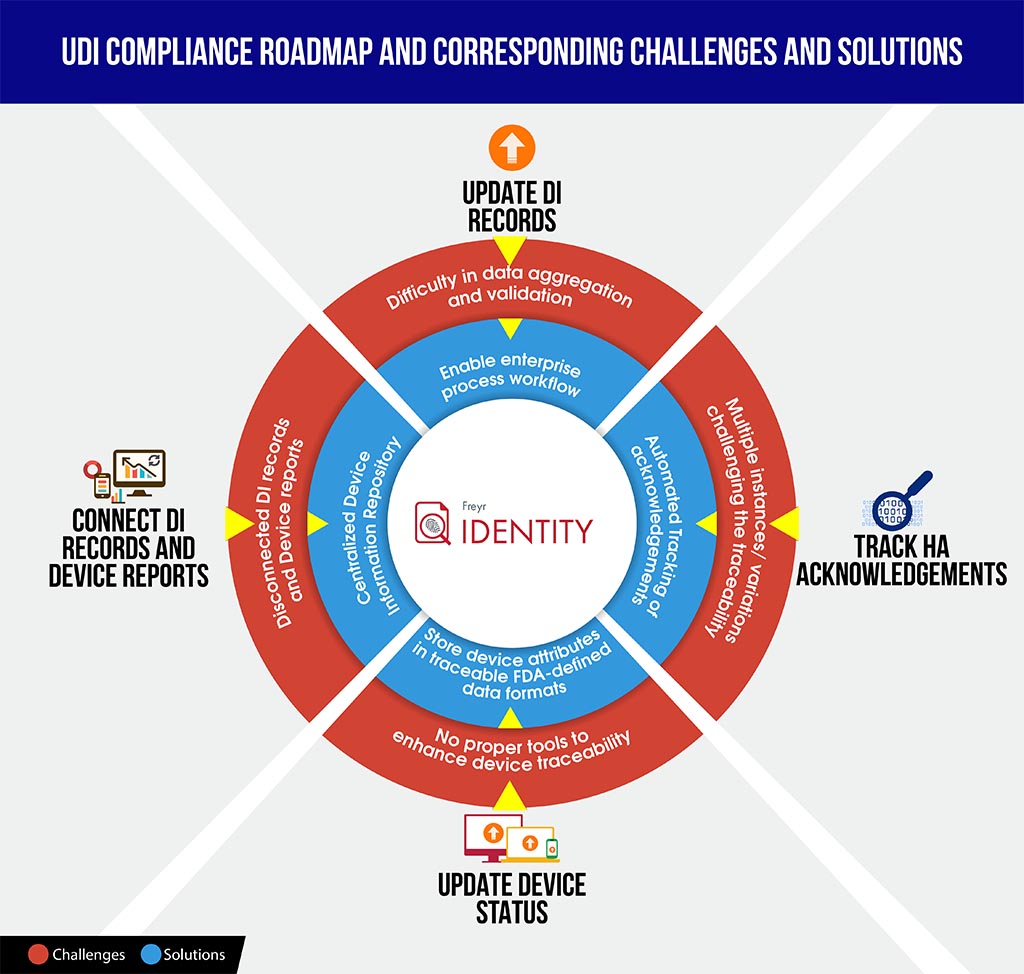
Pour guider en douceur votre organisation à travers ce processus de conformité complexe, Freyr offre le meilleur des deux mondes – une solution logicielle UDI à la demande, entièrement configurable, Freyr IDENTITY, ainsi qu'un Centre d'Excellence UDI (CoE) qui propose des services UDI de premier ordre, rentables et personnalisables, conçus pour répondre à vos exigences uniques et spécifiques.









