
Dans le monde en évolution des dispositifs médicaux, la conformité n'est pas une tâche ponctuelle, c'est un engagement continu. La surveillance et les mises à jour continues des rapports clés tels que les Rapports d'Évaluation Clinique (CER), les Rapports d'Évaluation des Performances (PER) et les Rapports Périodiques Actualisés de Sécurité (PSUR) sont essentielles tout au long du cycle de vie d'un dispositif médical, de la recherche initiale à la surveillance après commercialisation. À mesure que le paysage des avancées médicales et des exigences réglementaires évolue continuellement, garantir la sécurité et la conformité des dispositifs médicaux et des DIV par une rédaction médicale efficace reste la pierre angulaire du succès et de la viabilité à long terme.
Examinons comment la gestion du cycle de vie reste essentielle au succès d'un dispositif médical
Le lancement d'un dispositif médical est l'aboutissement d'années d'efforts consacrés à plusieurs phases telles que la recherche, le développement, les essais cliniques, les soumissions réglementaires et la surveillance après commercialisation. Ce processus s'étend sur de nombreuses années et chaque phase accumule une grande quantité de données vitales, qui doivent être soigneusement compilées et analysées pour garantir que le dispositif reste sûr.
La conformité n'est pas une action ponctuelle, et une gestion efficace du cycle de vie permet d'éviter des retards qui pourraient être coûteux par la suite. Ces retards sont souvent dus à une planification inefficace face à des changements réglementaires imprévus ou à un non-respect des normes qui aurait pu être négligé. Des mises à jour régulières des documents critiques tels que les CER, les PER et les PSUR garantissent que les fabricants répondent aux exigences réglementaires en constante évolution et maintiennent la sécurité des produits. La gestion du cycle de vie garantit que les fabricants, dès le départ, ont planifié chaque étape, ce qui leur permet d'éviter les pièges et d'assurer une entrée réussie sur le marché et la longévité de leurs dispositifs.
Maintenez-vous votre conformité ?
Des pansements aux implants, l'industrie des dispositifs médicaux est un secteur de pointe, créatif et riche en opportunités. Malgré le fort désir des fabricants de fournir au marché des produits sûrs et de haute qualité, des ambiguïtés subsistent néanmoins. L'EU MDR a remplacé la Directive sur les dispositifs médicaux (MDD) et la Directive sur les dispositifs médicaux implantables actifs (AIMDD). Cette réglementation a été mise en œuvre pour imposer des contrôles plus rigoureux, améliorer la sécurité des patients et promouvoir une transparence accrue au sein du secteur de la santé. Il existe beaucoup d'incertitude concernant ces normes, et des problèmes de conformité cruciaux sont fréquemment négligés. Cependant, les fabricants de dispositifs médicaux devraient prendre des mesures pour éviter les difficultés réglementaires.
Examinons les défis les plus courants auxquels sont confrontés les fabricants de dispositifs médicaux
- Maintien de la CAPA (Corrective and Preventive Action)
- Respecter les procédures de traitement des plaintes
- Suivi des procédures de vigilance
- Évaluation clinique et surveillance après commercialisation
- Se connecter avec les organismes notifiés.
Meilleures pratiques pour assurer la conformité
Pour surmonter ces défis, chez Freyr, nous avons mis en place
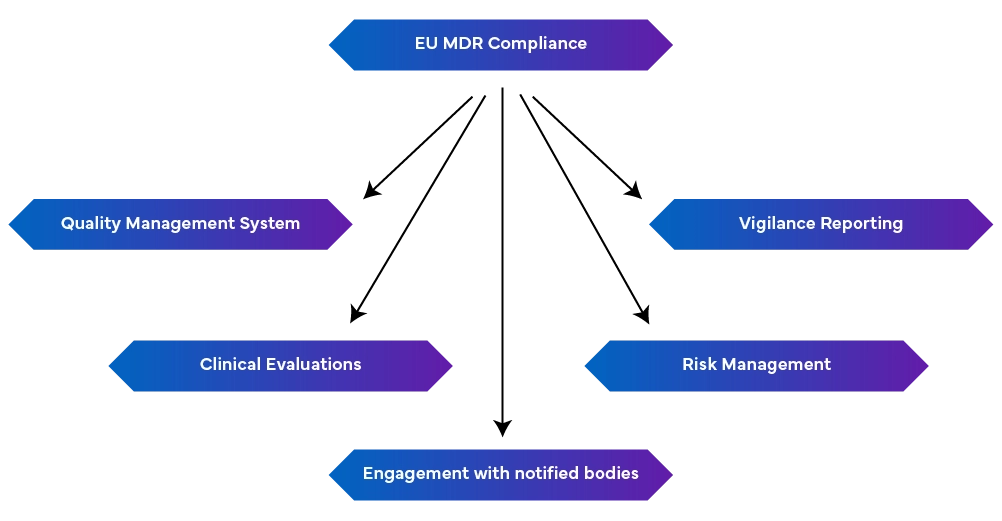
-un système de gestion de la qualité rigoureux (EN ISO 13485:2016) : celui-ci couvre les aspects liés à la production, notamment la conformité réglementaire, la documentation technique, les déclarations de conformité de l'UE et la gestion des risques.
-Déclaration de vigilance : Maintenir la déclaration de vigilance comme un processus continu plutôt qu'un effort ponctuel.
- Gestion proactive des risques : Cela permet d'identifier et d'atténuer les risques tout au long du cycle de vie du dispositif en se mettant à jour régulièrement pour faire face aux risques émergents.
- Réaliser des évaluations cliniques et une surveillance après commercialisation : Cela se fait en démontrant la sécurité et la performance du dispositif à l'aide de données cliniques. Si nécessaire, des investigations cliniques doivent être menées, et les évaluations cliniques doivent être régulièrement mises à jour avec les données de surveillance après commercialisation. Des rapports périodiques de mise à jour de la sécurité résumant les résultats sont également requis.
- Connexion avec les organismes notifiés : Les changements de réglementation peuvent affecter les exigences du MDR, rendant crucial le maintien d'une bonne relation avec les organismes notifiés pour des mises à jour et des modifications rapides.
Comment un expert en réglementation peut vous aider
Il peut être difficile de suivre l'évolution constante du paysage réglementaire. Alors, pourquoi ne pas laisser un expert vous guider dans ce labyrinthe ? Gérer les exigences réglementaires tout au long du cycle de vie d'un dispositif médical est non seulement complexe, mais aussi gourmand en ressources. Pour les petites entreprises, où les ressources internes pourraient être mieux utilisées dans d'autres domaines, l'aide d'un partenaire réglementaire externe peut s'avérer indispensable. Ils offrent une connaissance spécialisée des réglementations en constante évolution et veillent à ce que vos rapports clés – tels que les CER, PER et PSUR – soient continuellement mis à jour et conformes.
Vous pouvez éviter des retards coûteux, prévenir la non-conformité et rationaliser votre processus d'approbation. De plus, un expert en réglementation peut offrir des solutions adaptées aux besoins spécifiques de votre dispositif, garantissant que la surveillance après commercialisation, l'analyse des lacunes et toute la documentation de conformité sont à jour. Leur implication peut simplifier le processus global, minimiser les risques et garantir que le dispositif peut répondre aux attentes en matière de sécurité et de performance.
Freyr peut vous aider avec tous vos besoins réglementaires concernant la gestion du cycle de vie. Contactez-nous dès aujourd'hui !










