Les autorités sanitaires de tous les pays, à l'exception du Canada, exigent que tous les fabricants étrangers de dispositifs médicaux désignent un représentant local, dans le pays concerné, ou un représentant autorisé. Le rôle d'un représentant légal consiste à représenter le fabricant et le dispositif dans le pays cible et à assurer la liaison entre les autorités sanitaires et les fabricants étrangers. Il existe une terminologie spécifique à chaque pays pour désigner le représentant local. Aux États-Unis, le représentant local est appelé « US » ( US ), tandis qu'au Royaume-Uni, on parle de « personne responsable au Royaume-Uni UKRP . Au Sri Lanka, le représentant local est appelé « agent local sri-lankais » ou « représentant agréé sri-lankais », qui est également le titulaire de l'autorisation de mise sur le marché (MAH) du dispositif.
Les fabricants étrangers de dispositifs médicaux peuvent choisir de désigner leur distributeur comme agent local, qui serait alors, par défaut, également le titulaire de l'autorisation de mise sur le marché (MAH). Il est toutefois recommandé de désigner comme MAH un prestataire de services tiers ne présentant aucun conflit d'intérêts. Les avantages liés à la désignation d'un prestataire de services tiers indépendant comme MAH énumérés ci-dessous. Un MAH :
- Maîtriser les affaires réglementaires nationales et les exigences PMS
- Atteindre les objectifs commerciaux en désignant plusieurs distributeurs pour la pénétration du marché
- Capacité à se concentrer sur la conformité réglementaire
- Techniquement compétent pour répondre aux questions soulevées par l'Agence
- Étiquettes communes pour un seul MAH le pays
- Éviter les complications liées à la mise à jour des étiquettes en cas de changement de distributeur, qui agirait également en tant que titulaire de l'autorisation de mise sur le marché (TAMM) ou agent MAH
Dans certains pays, comme en Inde, il n'existe aucune disposition permettant le transfert de l'autorisation de mise sur le marché, et une nouvelle demande doit être déposée. En revanche, au Sri Lanka, l'Autorité nationale de réglementation des médicaments (NMRA) autorisele transfert MAH . Le principal défi auquel sont confrontés les fabricants étrangers de dispositifs médicaux lors du changement de MAH l'obligation de présenter un certificat ou une lettre de non-objection (NoC/NoL) émis par le MAH actuel. La NMRA facilite également le MAH , même lorsque ce MAH réticent à délivrer un NoC.
Le changement de nom et/ou d'adresse du titulaire MAH au Sri Lanka MAH pas considéré comme un transfert d'AMM si le titulaire reste la même personne physique ou morale ; ce changement doit être notifié au moyen d'une demande de modification post-autorisation. Le fabricant doit contacter directement la NMRA s'il a l'intention de modifier les coordonnées du MAH dans la demande, alors que celle-ci est encore en cours d'examen par la NMRA.
La nécessité de transférer un MAH lorsque le fabricant décide de se désengager de l'autorisation de mise sur le marché actuelle ou lorsque cette autorisation est reprise par une autre entité juridique. Le MAH du transfert est appelé « cédant », tandis que la société, la société de personnes, la personne physique ou l'entité juridique à laquelle le transfert est destiné est appelée « cessionnaire ».
Pour que la procédure MAH puisse débuter, le cédant doit délivrer une lettre de non-objection (NOL) dans laquelle il donne son accord au transfert. Si le cédant refuse de délivrer la NOL, l'autorité accorde un délai de 14 jours pour présenter une objection à la désignation du cessionnaire (nouveau MAH). Si le motif de l'objection est valable et concerne le fabricant, l'autorité invite ce dernier à résoudre le problème et poursuit la procédure de transfert. Si le cédant a un conflit commercial avec le cessionnaire ou le fabricant, la NMRA poursuivra le processus de transfert, car l'autorité se préoccupe davantage de la disponibilité des dispositifs sur le marché sri-lankais que des obligations commerciales entre les différentes parties prenantes.
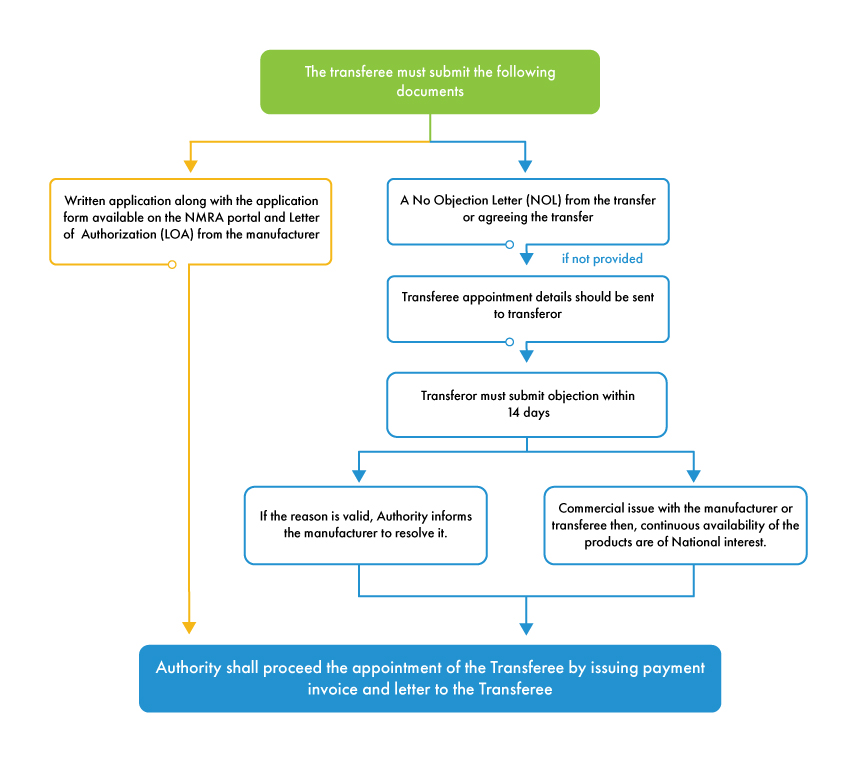
Contrairement à d'autres pays, la réglementation de la NMRA est favorable aux fabricants étrangers en matière de MAH . La NMRA autorise MAH dès lors que tous les documents requis sont fournis, à moins que l'objection soulevée par le cédant ne soit fondée et sérieuse. Il est dans l'intérêt de tous les fabricants étrangers de désigner un MAH indépendant MAH éviter toute complication dans le processus d'autorisation de mise sur le marché de leurs produits au Sri Lanka. Le soutien apporté par les agents locaux spécialisés dans les dispositifs médicaux au Sri Lanka offre une plateforme permettant à tous les fabricants étrangers de désigner et de changer de titulaire de l'MAH , avec les documents appropriés.
PourMAH d'agent local ou de titulaire de l'autorisation de mise sur le marché (MAH ), ou pour les services MAH au Sri Lanka, reach un expert régional en réglementation. Restez informé. Restez en conformité.









