Au fil des ans, avec les avancées logicielles et la numérisation, il y a eu un changement radical dans la manière dont les dispositifs médicaux sont gérés et fournis. L'intégration des logiciels aux dispositifs médicaux a rapidement augmenté, entraînant des avancées incroyables dans la fourniture de solutions de soins de santé dans divers domaines tels que le diagnostic, la prévention des maladies et le traitement des blessures ou des maladies.
Cependant, l'effet des logiciels sur la sécurité et la performance des dispositifs médicaux a été incertain, en particulier lorsque le dispositif est un produit uniquement logiciel. Par conséquent, les réglementations relatives aux logiciels de dispositifs médicaux sont constamment révisées pour déterminer la considération d'un logiciel comme dispositif médical (SaMD). Récemment, le conseil consultatif de la Commission européenne – le Groupe de coordination des dispositifs médicaux (MDCG) – s'est concentré sur l'amélioration des réglementations relatives aux logiciels de dispositifs médicaux et a publié un guide décrivant l'approche à appliquer pour déterminer si un logiciel est un dispositif médical ou non. Que décrit ce guide ? Découvrons-le.
La portée des lignes directrices
Le guide MDCG couvre à la fois les logiciels de dispositifs médicaux et les logiciels de dispositifs médicaux de diagnostic in vitro (DIV). Selon le document, un Logiciel de Dispositif Médical (MDSW) est défini comme un logiciel destiné à être utilisé seul ou en combinaison, dans un but spécifié dans la définition d'un « dispositif médical » dans le Règlement sur les dispositifs médicaux 2017/745 (MDR) ou le Règlement sur les dispositifs médicaux de diagnostic in vitro 2017/746 (IVDR). Il décrit les critères à appliquer pour déterminer si un logiciel soumis à examen est un dispositif médical ou non et vise à fournir des clarifications et des recommandations supplémentaires sur les MDSW aux fabricants de dispositifs médicaux et aux autres parties concernées.
Premièrement, ce guide énonce les termes les plus importants utilisés dans le contexte des MDSW, notamment :
Destination : L'utilisation à laquelle un dispositif est destiné selon les données fournies par le fabricant sur l'étiquette, dans la notice d'utilisation, ou dans les documents ou déclarations promotionnels ou de vente, et telle que spécifiée par le fabricant dans l'évaluation clinique.
Accessoire : Un article qui, bien que n'étant pas un dispositif médical en soi, est destiné par son fabricant à être utilisé avec un ou plusieurs dispositifs médicaux afin de permettre à ces derniers d'être utilisés conformément à leur destination prévue, ou d'en assister la fonctionnalité spécifiquement et directement en fonction de leur destination. De plus, le MDCG mentionne que l'accessoire logiciel peut piloter ou influencer l'utilisation d'un dispositif médical, et que les instructions d'utilisation et autres documents fournis par le fabricant doivent contenir des détails sur la manière dont les logiciels et accessoires appropriés doivent être sélectionnés.
Logiciel : Il s'agit d'un ensemble d'instructions qui traite les données d'entrée et crée des données de sortie.
Détermination du logiciel de dispositif médical
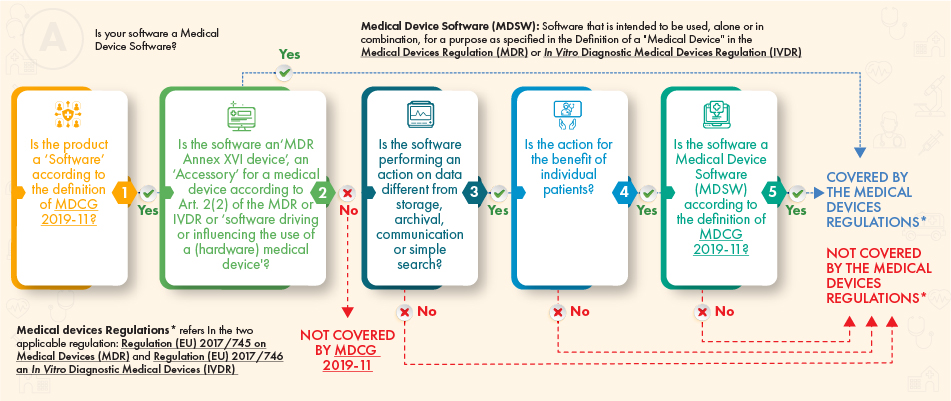
Conformément à l'organigramme d'orientation ci-dessus, le logiciel en question devrait être soumis à la réglementation s'il répond aux critères suivants :
- La définition d'un dispositif médical, d'un accessoire de celui-ci, ou qui régit le fonctionnement du dispositif médical, ou
- Il effectue un traitement supplémentaire des données (pas seulement le stockage ou la communication) et son action crée des avantages pour les patients, répondant ainsi à la définition d'un logiciel de dispositif médical conformément aux directives du MDCG.
Détermination des logiciels pour dispositifs médicaux de diagnostic in vitro
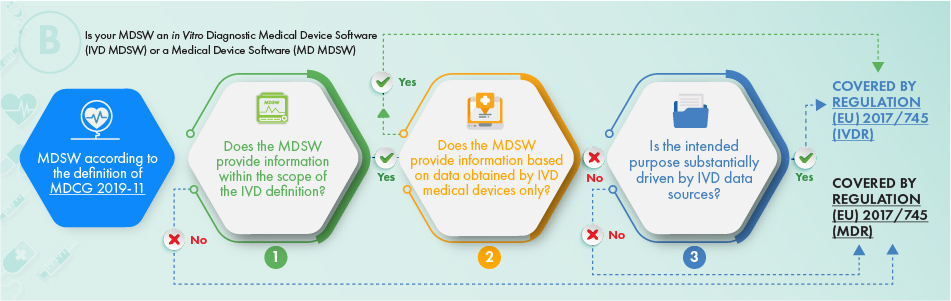
L'organigramme ci-dessus décrit l'approche à appliquer en ce qui concerne les produits destinés à des fins de diagnostic in vitro. Pour déterminer si le logiciel en question doit être soumis à la réglementation, les critères suivants doivent être pris en compte :
- La définition d'un dispositif médical, d'un accessoire de celui-ci, ou qui régit le fonctionnement du dispositif médical, ou
- Il fournit les informations habituellement fournies par les dispositifs médicaux de diagnostic in vitro et uniquement les informations recueillies auprès d'un dispositif médical de diagnostic in vitro, ou
- La finalité du logiciel est liée aux questions relatives à l'IVDR.
Conformément à l'orientation du MDCG, le type d'interconnexion entre le logiciel de dispositif médical et le dispositif n'affecte pas la qualification du logiciel en tant que dispositif au titre du MDR et de l'IVDR. Un logiciel de dispositif médical pourrait exister soit en tant que produit autonome, soit être incorporé dans un dispositif matériel et clarifie les exigences réglementaires suivantes :
- Compte tenu de sa qualification et de sa classification, un logiciel dispositif médical autonome doit être soumis à l'ensemble des procédures réglementaires conformément à la législation applicable.
- Un logiciel de dispositif médical qui fait partie intégrante d'un dispositif médical matériel pourrait être mis sur le marché selon une procédure simplifiée. Son évaluation ne serait pas effectuée séparément, mais lors de l'évaluation générale du dispositif médical matériel lui-même.
Pour résumer, les lignes directrices du MDCG couvrent les aspects essentiels liés à la classification des logiciels en tant que dispositifs médicaux et à la détermination des exigences réglementaires à appliquer. Les fabricants de dispositifs médicaux, les développeurs de logiciels et les autres parties doivent suivre et mettre en œuvre les recommandations du MDCG pour assurer la conformité. Pour obtenir plus d'informations sur la détermination de votre logiciel en tant que dispositif médical, consultez un expert en réglementation. Restez informé. Restez conforme.









