
La procédure 510(k) est une demande préalable à la mise sur le marché adressée à la FDA démontrer que le dispositif destiné à être commercialisé est aussi sûr et efficace, c'est-à-dire substantiellement équivalent, qu'un dispositif déjà légalement commercialisé (dispositif de référence). Les dispositifs présentant un risque modéré doivent faire l'objet d'une notification 510(k) ; cela concerne une minorité de dispositifs de classe I et III et la majorité des dispositifs de classe II.
Il existe trois (03) types de programmes 510(k) : Traditionnel, Abrégé et Spécial. La voie de la sécurité et de la performance a été introduite en 2019 et s'est appuyée sur le programme abrégé. Le programme eSTAR, introduit en 2020, permet une soumission complète de dispositifs médicaux via un formulaire PDF interactif.
Qui doit obtenir une certification 510(k) ?
Le 510(k) est essentiellement le nom du processus/de la voie que les fabricants de dispositifs médicaux ayant l'intention de commercialiser leurs dispositifs à risque modéré à élevé aux US suivent pour démontrer que le produit à commercialiser est aussi sûr et efficace qu'un dispositif légalement commercialisé.
Vous trouverez ci-dessous le processus étape par étape pour l'obtention d'une autorisation 510(k).
Étape 1 - Identification du code de classe du dispositif, du type de soumission et du dispositif de référence
- Identifier le code produit et le numéro de réglementation – Pour déterminer les exigences en matière de tests 510(k), il faut d'abord identifier le code produit et le numéro de réglementation. Il est possible d'effectuer une recherche dans la FDA afin de trouver le numéro de réglementation à 7 chiffres dont la description correspond à l'usage prévu du dispositif en question.
- Le code FDA se compose de trois (03) lettres. Ce code permet de trouver des informations concernant la classification du produit, la description de la réglementation et les exigences en matière de bonnes pratiques de fabrication (BPF).
- Choix du type de demande : le demandeur peut choisir l'un des trois (03) types de demande mentionnés précédemment. La procédure 510(k) traditionnelle concerne les premières soumissions, la procédure 510(k) spéciale s'adresse aux fabricants de dispositifs médicaux qui souhaitent soumettre des modifications à un dispositif existant, et la procédure 510(k) abrégée peut être choisie lorsque le dispositif est conforme à des normes consensuelles volontaires établies. Dans le cas d'une procédure 510(k) abrégée, le demandeur doit se référer aux documents FDA .
- Identification du dispositif de référence - Un fabricant de dispositifs médicaux doit prouver que le dispositif qu'il a l'intention de commercialiser a la même utilisation prévue et les mêmes caractéristiques techniques que le dispositif légalement commercialisé, également appelé dispositif de référence. S'il existe des différences dans les caractéristiques techniques, le demandeur doit prouver qu'aucune préoccupation en matière de sécurité et d'efficacité n'est associée à cette différence.
Étape 2 – Préparation du dossier 510(k)
L'étape suivante consiste à préparer le dossier 510(k), les lignes directrices et les informations disponibles sur le FDA . Ce dossier comprend la liste de contrôle de conformité pour les trois (03) types de programmes 510(k) ainsi qu'un microsite intitulé « Content for 510(k) », qui contient notamment des informations concernant les déclarations relatives aux indications d'utilisation, la comparaison d'équivalence substantielle et l'étiquetage proposé, entre autres renseignements utiles.
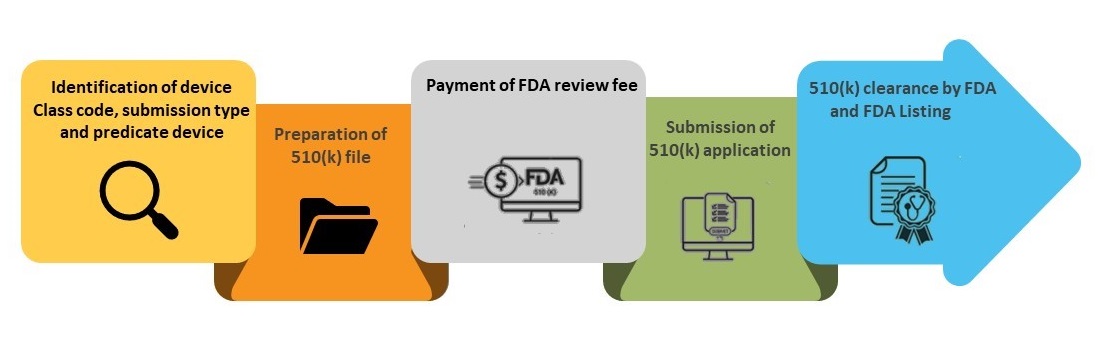
Étapes du processus de dépôt 510(k)
Étape 3 – Paiement des frais FDA
Tous les types de demandes 510(k) sont soumis aux frais d'utilisateur. Pour l'exercice fiscal 2023, les frais standard pour le 510(k) sont de 19 870 $. Pour les entreprises certifiées par le Centre pour le diagnostic et la santé radiologique (CDRH), également connues sous le nom de petites entreprises, les frais sont de 4 967 $. Ces frais sont susceptibles de changer au cours du prochain exercice fiscal.
Étape 4 - Dépôt de la demande 510(k)
Le déclarant peut envoyer une copie électronique (eCopy) ou une soumission pré-commercialisation via le modèle et la ressource de soumission électronique (eSTAR) par le portail du CDRH.
À partir du 1er octobre 2023, toutes les soumissions 510(k), sauf exemption conformément aux directives finales, devront être soumises sous forme électronique via eSTAR.
Une fois la demande 510(k) déposée, un numéro de référence unique est attribué, appelé « numéro 510(k) » ou « numéro K ». FDA deux vérifications : la première consiste à vérifier si les frais de dossier requis ont bien été acquittés, et la seconde à vérifier si un dossier eCopy ou eSTAR valide a été fourni.
- Au plus tard le septième jour, FDA une lettre d'accusé de réception si les frais de dossier ont été acquittés et qu'une copie électronique (eCopy) ou un dossier électronique (eSTAR) valide a été fourni. Dans le cas contraire, la FDA une lettre de suspension pour signaler les problèmes non résolus.
- Au plus tard le 15e jour, FDA un examen préliminaire FDA alors le demandeur si la demande 510(k) est admise pour examen approfondi ou si elle fait l'objet d'une suspension pour refus d'acceptation (RTA).
- Au 60e jour, FDA un examen approfondi. FDA , par le biais d'une « interaction approfondie » (
), FDA l'examen interactif ou FDA suspendre la procédure 510(k) et de demander des informations complémentaires.
Étape 5 – FDA et inscription dans la base de données FDA (k) FDA
L'objectif de la FDA de rendre publique sa décision relative à la loi MDUFA (Medical Device User Fee Amendments) dans un délai de 90 FDA . FDA correspondent aux jours calendaires écoulés entre la date de réception de la demande 510(k) et la date de la décision MDUFA, à l'exclusion des jours pendant lesquels le dossier a été suspendu en raison d'une demande d'informations complémentaires. Les décisions MDUFA concernant les demandes 510(k) incluent les conclusions de « substantiellement équivalent » (SE) ou « non substantiellement équivalent » (NSE).
Une fois la décision prise, FDA une lettre de décision au demandeur par courrier électronique. Une demande 510(k) pour laquelle une lettre de décision « SE » a été émise est considérée comme « autorisée ». Elle est alors répertoriée dans la base de données 510(k), accompagnée des indications d'utilisation du dispositif médical ainsi que du résumé 510(k) ou de la déclaration 510(k) en pièces jointes.
On peut en conclure qu'une planification et une exécution minutieuses, s'appuyant sur une documentation exhaustive et une compréhension approfondie du cadre réglementaire, sont essentielles pour garantir le succès d'une demande 510(k) auprès de FDA.
Pour obtenir de l'aide concernant le processus de soumission 510(k) de votre dispositif médical, vous pouvez nous écrire à sales@freyrsoltions.com, ou planifier un appel avec nos experts, qui pourront vous aider à naviguer dans les procédures. Restez informé. Restez conforme.









