
Le Système de Management de la Qualité (SMQ) est un composant essentiel de l'industrie des dispositifs médicaux, garantissant la sécurité, l'efficacité et la conformité réglementaire des dispositifs médicaux tout au long de leur cycle de vie. Le SMQ est mis en œuvre à toutes les étapes du cycle de vie des dispositifs médicaux, y compris la phase de conception et de développement, pour s'assurer que le dispositif répond aux exigences réglementaires et aux besoins des utilisateurs, et que tout risque potentiel est identifié et traité.
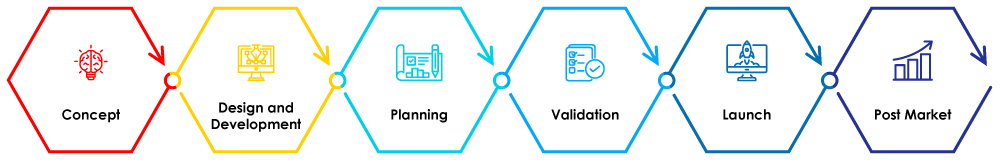
Figure 1 – Étapes du cycle de vie des dispositifs médicaux
Dans ce blog, nous discuterons de l'importance du QMS dans la phase de conception et de développement du cycle de vie des dispositifs médicaux.
Phase de conception et de développement dans le cycle de vie des dispositifs médicaux
La phase de conception et de développement est l'une des étapes les plus critiques du cycle de vie d'un dispositif médical. Au cours de cette étape, la conception du dispositif est élaborée et des prototypes sont créés, suivis par des tests de vérification et de validation dans le cadre du cycle de vie du dispositif médical.
Pour s'assurer que le dispositif médical répond aux exigences réglementaires, de sécurité, d'efficacité et aux attentes des utilisateurs, la mise en œuvre d'un Système de Gestion de la Qualité (SGQ) est essentielle au stade de la conception et du développement du cycle de vie d'un dispositif médical.
La documentation est essentielle pendant la phase de conception et de développement des dispositifs médicaux. Le SMQ garantit que toute la documentation liée à la conception et au développement est contrôlée, gérée et enregistrée.
Le dossier historique de conception (DHF) est un fichier/enregistrement important, contenant toute la documentation relative à la conception et au développement du dispositif. Le DHF fournit la preuve que la conception du dispositif répond aux exigences réglementaires.
Le DHF devrait contenir la documentation relative aux entrées de conception, aux sorties de conception, aux revues de conception, à la vérification de la conception, à la validation, aux modifications de la conception et à la gestion des risques. En savoir plus sur le DHF ici.
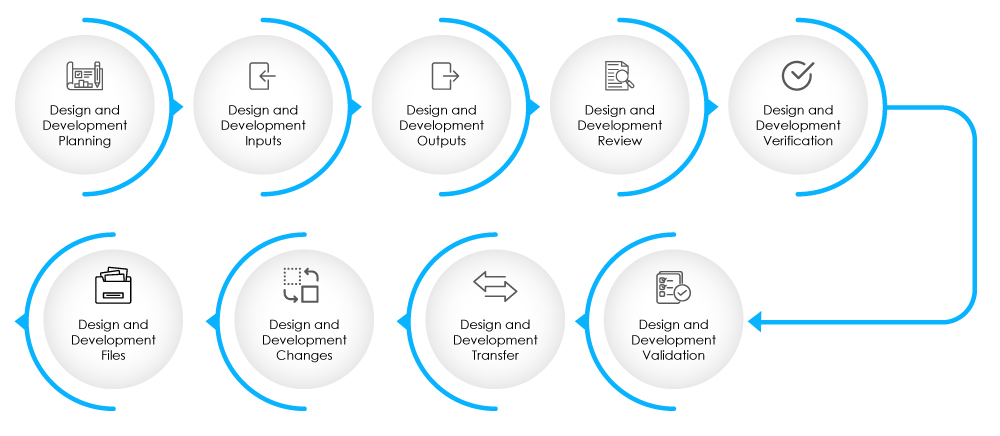
Fig. 2 – Étapes de la phase de conception et de développement
Bonnes pratiques pour l'étape de conception et de développement
- Établir une approche structurée : Développez une approche structurée pour le développement et la gestion du DHF (Dossier de Conception), adaptée aux besoins spécifiques de votre organisation. Cette approche doit inclure des directives claires, des procédures et des flux de travail pour le développement et la gestion du DHF.
- Définir et documenter les données d'entrée de conception : Définir et documenter clairement les données d'entrée de conception, y compris les exigences et les spécifications pour le dispositif. Cela peut aider à garantir que le DHF est complet et exhaustif.
- Gérer les Modifications de Conception : Mettre en œuvre un processus de gestion des modifications solide qui comprend des procédures pour documenter, évaluer et approuver les modifications de conception. Cela permet de s'assurer que les modifications sont correctement documentées et évaluées quant à leur impact sur la sécurité et l'efficacité de l'appareil.
- Assurer la traçabilité : Développer une matrice de traçabilité qui relie les entrées de conception aux sorties de conception et s'assurer que toutes les activités de conception et de développement sont correctement documentées et enregistrées. Cela peut aider à garantir que le DHF est traçable et que le processus de prise de décision est bien documenté.
- Balancer l'innovation et la conformité : Développer une culture de l'innovation tout en veillant à ce que les exigences de conformité liées au DHF, telles que les contrôles de conception et la gestion des risques, soient respectées. Ceci peut être réalisé en élaborant des procédures et des flux de travail qui facilitent l'innovation tout en garantissant le respect des exigences réglementaires.
- Mettre en œuvre le contrôle des documents : Mettre en œuvre des procédures de contrôle des documents qui garantissent que les documents du DHF sont correctement contrôlés, gérés en termes de versions et accessibles au personnel autorisé. Cela peut aider à garantir que les documents du DHF sont sécurisés et que les modifications sont correctement documentées et approuvées.
- Former l'équipe: Assurez-vous que l'équipe responsable du développement et de la gestion du DHF (Dossier Historique de Conception) est correctement formée aux exigences du DHF et possède l'expertise technique nécessaire pour développer le produit. Cela peut être réalisé par des sessions de formation régulières, du mentorat et l'embauche de professionnels expérimentés possédant les compétences et l'expertise requises.
En suivant ces meilleures pratiques, l'industrie des dispositifs médicaux peut assurer la conformité aux exigences réglementaires, promouvoir la sécurité et l'efficacité de ses produits, et maintenir son avantage concurrentiel sur le marché.
En conclusion, la mise en œuvre d'un SMQ dès la phase de conception et de développement est essentielle au succès dans l'industrie des dispositifs médicaux, fortement réglementée. En maintenant des enregistrements systématiques et en respectant les exigences réglementaires, l'industrie des dispositifs médicaux peut s'assurer de fournir des produits de haute qualité et de maintenir la satisfaction de ses clients.
Chez Freyr, nous offrons des services QMS pour aider l'industrie des dispositifs médicaux à répondre aux exigences réglementaires à toutes les étapes du cycle de vie des dispositifs médicaux. Contactez nos experts QMS et réglementaires pour en savoir plus.









