
Regulatory Affairs (RA) spielen eine zentrale Rolle bei der Gewährleistung der Sicherheit, Wirksamkeit und Qualität von Arzneimitteln in der dynamischen Pharmabranche. Chemistry, Manufacturing, and Controls (CMC) RA ist für die Compliance unerlässlich. Sie zielt darauf ab, die Patientengesundheit zu schützen und das Vertrauen der Öffentlichkeit in pharmazeutische Produkte zu fördern, indem sie Konsistenz und Qualität während des gesamten Arzneimittelherstellungsprozesses gewährleistet.
CMC RA umfasst Dokumentations- und Compliance-Anforderungen im Zusammenhang mit der Herstellung, Qualitätskontrolle und Stabilität von pharmazeutischen Produkten. Es erfordert Sorgfalt und die Einhaltung regulatorischer Richtlinien während des gesamten Lebenszyklus der Arzneimittelentwicklung. Um mehr über die Bedeutung von CMC RA zu erfahren, konsultieren Sie unsere Experten.
In diesem Blog werden wir uns mit den Grundlagen von CMC RA befassen und seine Bedeutung für die Einhaltung von Vorschriften und die Aufrechterhaltung hoher Qualitätsstandards untersuchen.
Die Rolle von CMC in der Arzneimittelentwicklung
CMC-Überlegungen beginnen früh im Arzneimittelentwicklungsprozess und setzen sich durch alle Phasen fort, von der präklinischen Forschung bis zur Kommerzialisierung. CMC-Daten und -Dokumentationen sind entscheidende Bestandteile regulatorischer Einreichungen, wie z. B. Anträge für klinische Prüfungen (IND), Zulassungsanträge für neue Arzneimittel (NDA) und Anträge auf Marktzulassung (MAA). Regulierungsbehörden prüfen CMC-Daten, um die Sicherheit, Identität, Wirksamkeit und Qualität eines Arzneimittelprodukts sowie die Zuverlässigkeit und Konsistenz des Herstellungsprozesses zu bewerten.
Einhaltung der CMC RA gewährleisten
Die Einhaltung der regulatorischen CMC-Anforderungen ist für einen erfolgreichen Markteintritt von größter Bedeutung. Regulierungsbehörden wie die USFDA (United States Food and Drug Administration), die EMA (European Medicines Agency) und andere regionale Gesundheitsbehörden (HAs) sind für die Festlegung von Richtlinien und Standards verantwortlich, die eingehalten werden müssen. Diese Richtlinien decken verschiedene Aspekte ab, darunter Herstellungspraktiken, Qualitätssysteme, Analysemethoden, Stabilitätsprüfungen und Validierung. Compliance umfasst eine sorgfältige Dokumentation, die Einhaltung der Guten Herstellungspraxis (GMP) und die Implementierung effektiver Qualitätsmanagementsysteme (QMS).
Die Rolle der CMC-Compliance für den Erfolg eines Pharmaunternehmens
Die Aufrechterhaltung hoher Standards der CMC-Compliance bietet Pharmaunternehmen mehrere Vorteile. Einige der Hauptvorteile sind:
- Minderung regulatorischer Risiken.
- Unterstützung erfolgreicher regulatorischer Genehmigungen.
- Reduzierung der Wahrscheinlichkeit von Produktrückrufen.
- Einen positiven Ruf für Qualität und Zuverlässigkeit fördern.
Wichtige Punkte für eine erfolgreiche RA-CMC-Funktion:
- Aktuelles regulatorisches Wissen: Sich entwickelnde regulatorische Anforderungen von Gesundheitsbehörden (HAs) erfordern, mit den neuesten Richtlinien auf dem Laufenden zu bleiben. Die kontinuierliche Überwachung regulatorischer Aktualisierungen und deren Integration in die CMC-Praktiken ist entscheidend, um die Compliance aufrechtzuerhalten.
- Aufbau von Qualitätssystemen: Dies umfasst die Entwicklung und Pflege umfassender Standardarbeitsanweisungen (SOPs), Dokumentenkontrollverfahren, Änderungskontrollprozesse und Schulungsprogramme, um sicherzustellen, dass die Mitarbeiter die festgelegten Protokolle verstehen und befolgen.
- Risikobewertung und -minderung: Unternehmen sollten potenzielle Risiken während der gesamten Arzneimittelentwicklung und des Herstellungsprozesses identifizieren und geeignete Risikominderungsstrategien implementieren. Dies umfasst die Bewertung kritischer Prozessparameter, der Variabilität von Rohstoffen, potenzieller Verunreinigungen und Lieferkettenrisiken, die die Einhaltung von Vorschriften gewährleisten.
- Dokumentation und Datenintegrität: Die Pflege genauer und vollständiger Dokumentationen ist unerlässlich, um die Einhaltung von Vorschriften nachzuweisen. Unternehmen müssen robuste Dokumentationspraktiken etablieren, einschließlich der Pflege von Chargenprotokollen, Analysedaten, Stabilitätsstudien und Validierungsberichten. Die Gewährleistung der Integrität, Rückverfolgbarkeit und Sicherheit von Daten ist entscheidend, um Compliance-Probleme zu vermeiden.
- Effektives Änderungsmanagement: Unternehmen müssen klar definierte Änderungskontrollverfahren implementieren, um Änderungen zu bewerten und zu dokumentieren, deren Auswirkungen auf die Produktqualität und die Einhaltung regulatorischer Vorschriften zu beurteilen und die erforderlichen Genehmigungen einzuholen, bevor Änderungen umgesetzt werden.
- Starke Lieferantenpartnerschaften und -management: Dies beinhaltet die Auswahl qualifizierter Lieferanten, die Durchführung von Audits und den Abschluss von Qualitätsvereinbarungen, die Verantwortlichkeiten und Erwartungen festlegen. Regelmäßige Überprüfungen der Einhaltung der aktuellen Guten Herstellungspraxis (cGMP) durch Lieferanten sind unerlässlich.
- Bereitschaft für Audits und Inspektionen: Unternehmen sollten Selbstbewertungen durchführen, um Verbesserungsbereiche zu identifizieren und die Bereitschaft für regulatorische Audits sicherzustellen. Tatsächlich sind die schnelle Behebung von Auditfeststellungen und die Umsetzung von Korrekturmaßnahmen entscheidend für die Aufrechterhaltung der Compliance.
- Kontinuierliche Verbesserung: Dies kann durch die Förderung des Mitarbeiterengagements, die Bereitstellung von Schulungen und Weiterbildungen zu regulatorischen Anforderungen sowie die Etablierung einer qualitätsorientierten Denkweise auf allen Ebenen der Organisation erreicht werden.
- Behebung von Korrektur- und Vorbeugemaßnahmen (CAPA): Durch die systematische Behebung von Nicht-Konformitäten mithilfe der CAPA-Methodik können Pharmaunternehmen ihr Engagement für kontinuierliche Verbesserung und Compliance demonstrieren.
- Kenntnis der regulatorischen Änderungen nach der Zulassung: Das Verständnis der regulatorischen Anforderungen für Änderungen nach der Zulassung ist unerlässlich, um die Einhaltung von Vorschriften zu gewährleisten. Die Implementierung geeigneter Änderungsmanagementprozesse und eine effektive Kommunikation mit den zuständigen Behörden kann helfen, diese Änderungen zu bewältigen und gleichzeitig die Compliance sicherzustellen.
Die Rolle eines regulatorischen Anbieters im CMC-Compliance-Prozess
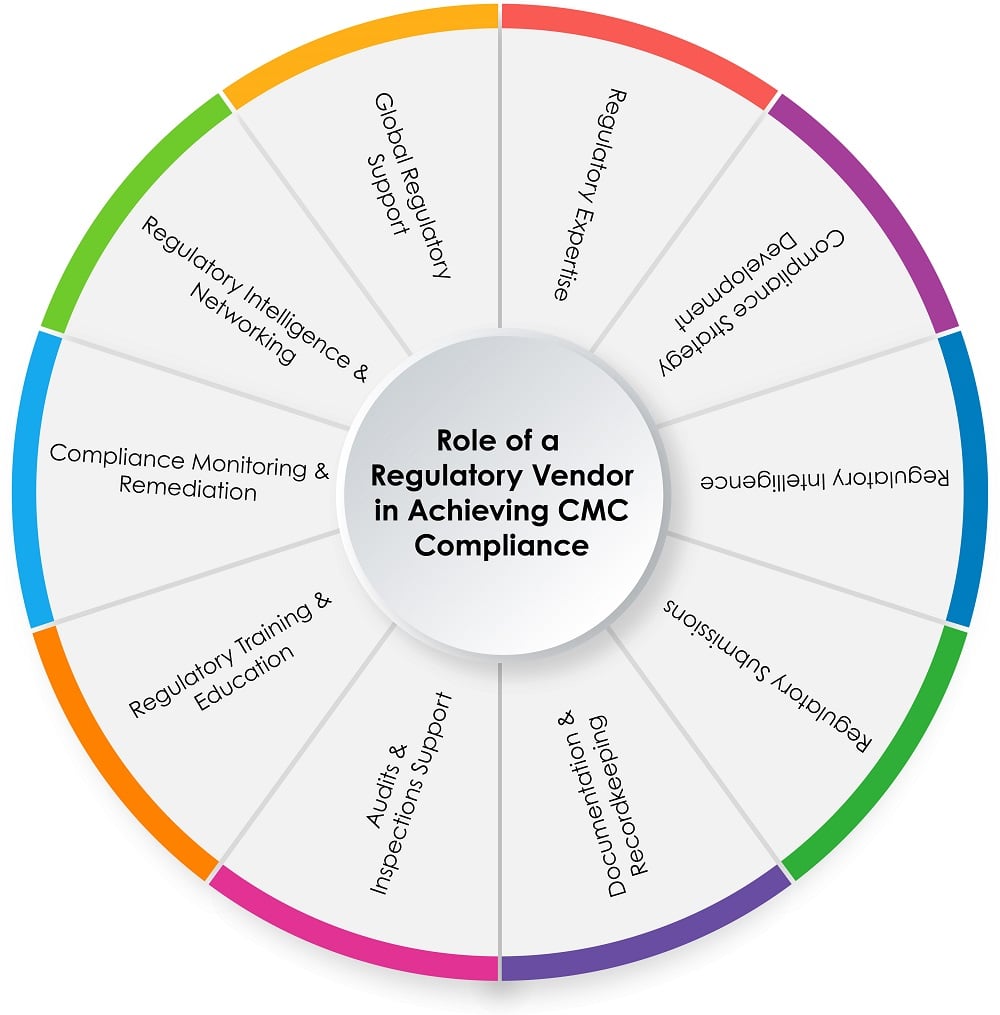
Das Tortendiagramm unten (Abbildung 1) zeigt die Rolle eines regulatorischen Anbieters im CMC-Compliance-Prozess:
Abbildung 1: Rolle eines regulatorischen Anbieters bei der Erreichung der CMC-Compliance
Fazit
Die Erreichung und Aufrechterhaltung der Compliance mit CMC-Anforderungen erfordert einen strategischen Ansatz, der eine funktionsübergreifende Zusammenarbeit, starke Qualitätssysteme und kontinuierliche Regulatory Intelligence (RI) beinhaltet. Dies ist auch entscheidend für einen erfolgreichen Marktzugang und die kontinuierliche Produktverfügbarkeit. Ein umfassendes Verständnis der Grundlagen von CMC RA und die Implementierung effektiver Compliance-Strategien können Pharmaunternehmen dabei helfen, sich in der regulatorischen Landschaft zurechtzufinden, Zulassungen zu erhalten und die höchsten Standards für Qualität und Patientensicherheit aufrechtzuerhalten. Strategische regulatorische Partnerschaften können diese entscheidenden Schritte synergetisch unterstützen, indem sie erstklassige Expertise für die Einhaltung der Vorschriften bieten. Kontaktieren Sie uns, um mehr über unsere Dienstleistungen zu erfahren!









