
Am 9. Februar 2022 begann die Europäische Arzneimittel-Agentur (EMA) mit der Einrichtung eines Koordinationszentrums für Datenanalyse und ein Netzwerk zur Integration von Real-World-Daten (DARWIN EU®). Dies ist der erste Schritt zur Integration von Real-World Evidence (RWE) in die Bewertung von Arzneimitteln in der gesamten Europäischen Union (EU). Die Gewährleistung der Sicherheit und Wirksamkeit von Arzneimitteln ist die Hauptaufgabe jeder Regulierungsbehörde, und RWE erweist sich als zuverlässige Quelle für die Sammlung von Echtzeitdaten aus globalen Gesundheitsdatenbanken. Dieser Schritt der EMA soll daher die Qualität von Arzneimitteln in der EU-Region verbessern und deren schnellere Verfügbarkeit ermöglichen.
Wichtige geplante Aktivitäten für das Koordinationszentrum für DARWIN EU®
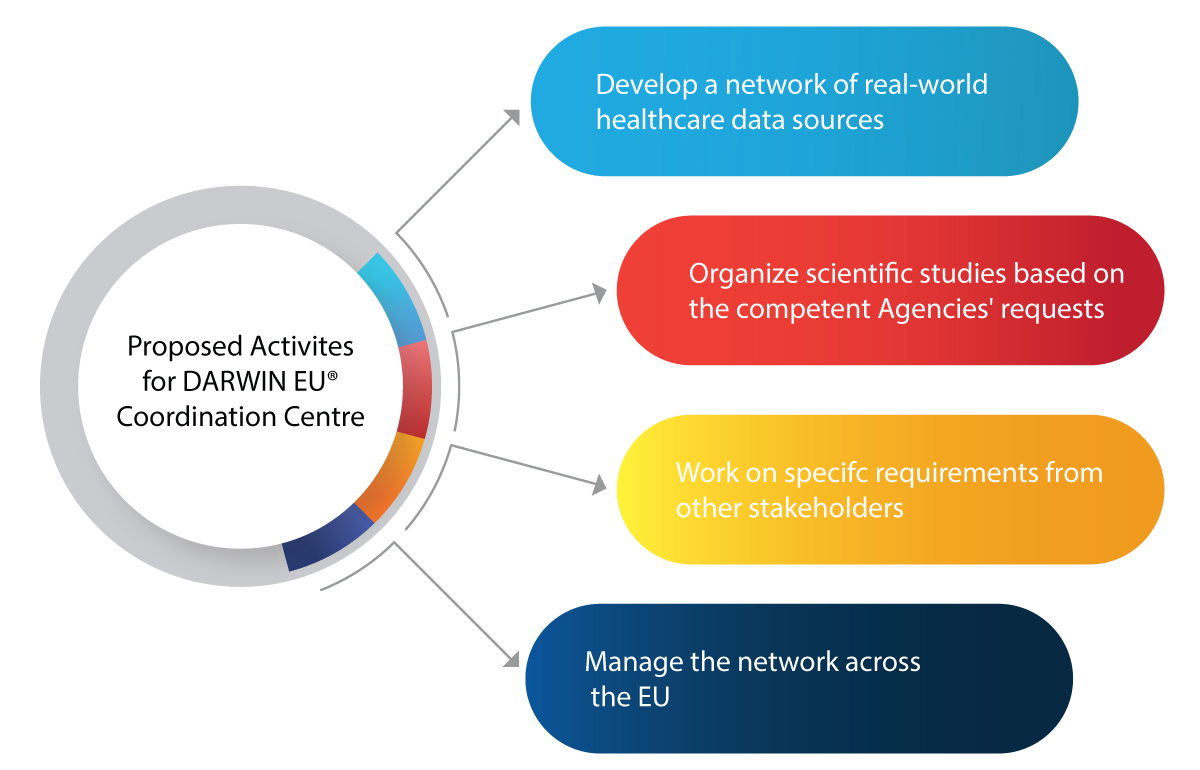
Wie wird DARWIN EU® der EMA und den zuständigen Behörden im regulatorischen Bereich helfen?
Innovative Arzneimittel, die Patienten schnell zur Verfügung stehen, werden dringend benötigt. Die regulatorischen Prozesse für Entwicklung, Zulassung, Vermarktung und Überwachung nach der Markteinführung nehmen erheblich viel Zeit in Anspruch, wodurch der Bedarf an neuen Medikamenten ungedeckt bleibt. Die Verkürzung der Markteinführungszeit bei gleichzeitiger Gewährleistung der Sicherheit, Wirksamkeit und Qualität innovativer Arzneimittel ist der richtige Weg. Mehrere globale Gesundheitsbehörden erkennen die Vorteile der Integration von RWE in ihre Zulassungsverfahren, und DARWIN EU® ist eine Initiative der EMA.
Die EMA plant, das europäische Netzwerk für die Arzneimittelregulierung mit dem Europäischen Gesundheitsdatenraum (EHDS) zu verbinden, um im Rahmen dieses Programms einen besseren Datenaustausch und einen verbesserten Zugang zu verschiedenen Arten von Gesundheitsdaten zu ermöglichen. Es wird auch Standards für wissenschaftliche Bewertungen und die regulatorische Entscheidungsfindung festlegen.
Hier sind einige Aktivitäten, die DARWIN EU® erreichen möchte:
- Nutzung von RWE bei Entscheidungsfindungen für die Regulierung neuer Medikamente, Impfstoffe usw.
- Integration von RWE in den gesamten Lebenszyklus eines Arzneimittels, wie Entwicklung, Zulassung und Überwachung nach der Markteinführung
- Vorbereitung auf zukünftige medizinische Notfälle wie Pandemien
- Die Pharmaindustrie mit aufschlussreichen und zuverlässigen RWE zu Patienten, Krankheiten und der Anwendung von Medikamenten unterstützen.
- Fundierte regulatorische Entscheidungen auf Grundlage von RWE für die sichere und wirksame Anwendung von Arzneimitteln treffen.
- Verbesserte Zugänglichkeit lebensrettender Medikamente für bedürftige Patienten dank genauer und zeitnaher Datenanalyse.
Vorgeschlagene Zeitpläne, damit DARWIN EU® ein voll funktionsfähiges Netzwerk in der EU wird
Die EMA legt auch die Zeitpläne fest, damit DARWIN EU® voll funktionsfähig wird, und diese sehen wie folgt aus:
- 2021 – Projektstart
- 2022 – Gründung von DARWIN EU®
- 2023 – Entwicklung von DARWIN EU® und Definition seiner Anwendungsbereiche
- 2024 – Vollständige Inbetriebnahme von DARWIN EU®
- 2025 – Die regulatorische Nutzung von Gesundheitsdaten durch Erweiterung der Anwendungsbereiche hinsichtlich Medikamenten, Geografie usw. verbessern.
Die EMA arbeitet mit dem Erasmus University Medical Center Rotterdam für die Gründung von DARWIN EU® zusammen. Ziel dieser Partnerschaft ist die Einrichtung des Koordinationszentrums, um ein verteiltes Datennetzwerk aufzubauen. Beide haben auch die Aufgaben übernommen, wissenschaftliche Studien durchzuführen, regulatorische Entscheidungsprozesse zu unterstützen und einen Katalog von Real-World-Datenquellen zu verwalten.
Was bedeutet die Einführung von DARWIN EU® für die Zukunft?
Die EMA und die Leiter der Arzneimittelbehörden (HMA) haben stets zusammengearbeitet, um Herausforderungen zu identifizieren, zeitgebundene Ziele festzulegen und Prioritäten in ihren Fünfjahres-Strategiedokumenten zu definieren. Dies soll die strategische Ausrichtung für die Aktivitäten des europäischen Netzwerks für die Arzneimittelregulierung vorgeben.
Die Einführung von DARWIN EU® ist ein wichtiger Schritt zur Umsetzung der Netzwerkstrategie der EMA. Die Durchführung wissenschaftlicher Studien zur Beantwortung von Forschungsfragen, die Unterstützung der Bewertung von Arzneimitteln in der EU und die Pflege von Metadata für regulatorische Arzneimittelaktivitäten sind die Hauptziele. DARWIN EU® wird als wichtiger Akteur in der Arzneimittelregulierung in Europa angesehen, und die Pilotstudien sollen bis Ende 2022 abgeschlossen sein.
Wenn Sie ein Arzneimittelhersteller sind und mehr über RWE erfahren möchten und wie es die Zukunft der regulatorischen Entscheidungsfindung prägt, kontaktieren Sie die Regulatory Affairs Experten von Freyr.









