
Die Therapeutic Goods Administration (TGA) in Australien hat strenge Regeln für die Registrierung neuer verschreibungspflichtiger Arzneimittel mit neuartigen Wirkstoffen. Kürzlich hat die TGA ein überarbeitetes Verfahren eingeführt, um die Wirksamkeit lebensrettender verschreibungspflichtiger Medikamente zu verbessern und sie Patienten schneller zugänglich zu machen. Diese Änderungen sind relevant für Anträge, die durch nicht-klinische, klinische und/oder Bioäquivalenzdaten (Kategorie 1 und Kategorie 2) gestützt werden müssen. Die TGA veröffentlichte im August ein Dokument mit Details zu den regulatorischen Anforderungen hierfür.
Wesentliche Merkmale im neuen Registrierungsprozess für verschreibungspflichtige Arzneimittel
- Die TGA hat einen phasenweisen Registrierungsprozess entwickelt und die einzelnen Phasen als Meilensteine bezeichnet. Jede Phase folgt einem separaten Pfad.
- Das neue Verfahren zielt darauf ab, die Qualität des Dossiers zu verbessern. Dossiers werden auf der Grundlage eines Common Technical Document (CTD)-Formats erstellt und erfüllen alle regulatorischen Anforderungen.
- Die Planungsphase vor der Einreichung ist wichtig, da Antragsteller die Details des voraussichtlichen Antrags einreichen. Dies geschieht mindestens zweieinviertel (02 ¼) Monate vor der Einreichung des vollständigen Dossiers. Diese Phase soll der TGA helfen, die Termine der nachfolgenden Meilensteine festzulegen und die Ressourcen für die Verwaltung des CTD bereitzustellen.
- Die nächste Phase ist die Einreichung. Sobald dies erfolgt ist, erlaubt die TGA dem Antragsteller nicht, nach dem Einreichungsdatum zusätzliche Daten oder Informationen anzubieten. Es ist zwingend erforderlich, ein vollständiges, korrektes und qualitativ hochwertiges Dossier einzureichen.
- Gemäß Abschnitt 31 des Therapeutic Goods Act 1989 fordert die TGA in der Bewertungsphase zusätzliche Informationen an. Nach der ersten Bewertung werden alle Anfragen gesammelt und an den Antragsteller gesendet.
Um die Meilensteine im erneuerten Verfahren zu verstehen, beachten Sie bitte die folgenden Flussdiagramme.
Meilenstein 1
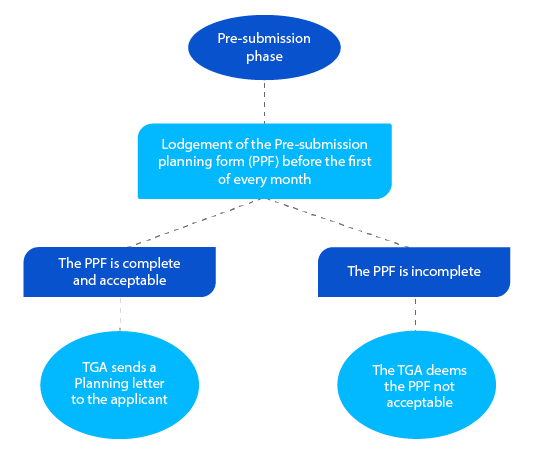
Das Planungsschreiben enthält das erwartete Datum, an dem die TGA die Einreichung des Dossiers erwartet, sowie weitere Zielmeilensteintermine für den Antrag auf Zulassung des verschreibungspflichtigen Arzneimittels.
Meilenstein 2
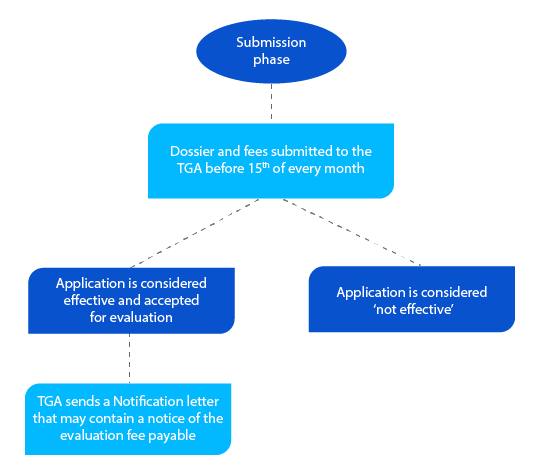
Das Dossier enthält Informationen, die der TGA bei der Bewertung des Antrags helfen, und wenn alles akzeptabel ist, wird ein Benachrichtigungsschreiben vor dem Ende des Monats versandt, in dem der Antragsteller das Dossier eingereicht hat.
Meilenstein 3
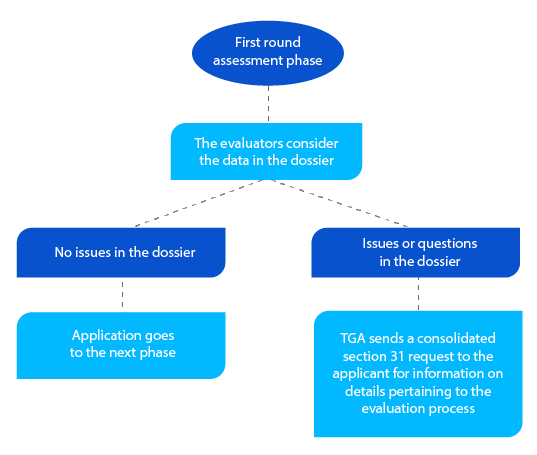
Zusätzlich zum konsolidierten Abschnitt 31 sendet die TGA, sofern zutreffend und angefordert, Kopien der Bewertungsberichte, die von den Gutachtern für Qualität, nichtklinische und klinische Aspekte sowie für Risikomanagementpläne (RMP) erstellt wurden.
Meilenstein 4
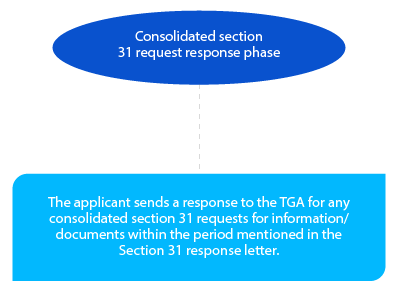
Der Antragsteller kann die Frist für die Beantwortung des Abschnitts 31 festlegen. Diese kann entweder dreißig (30) oder sechzig (60) Tage betragen und sollte im PPF hervorgehoben werden. Dieser Zeitraum muss von der TGA im Planungsbrief bestätigt werden. Das akzeptable Format der Antwort ist CTD, und diese muss in Form von gedruckten und elektronischen Kopien eingereicht werden.
Da dies die letzte Gelegenheit für den Antragsteller ist, fehlende Informationen an die TGA zu übermitteln, muss dies vorschriftsmäßig erfolgen.
Meilenstein 5
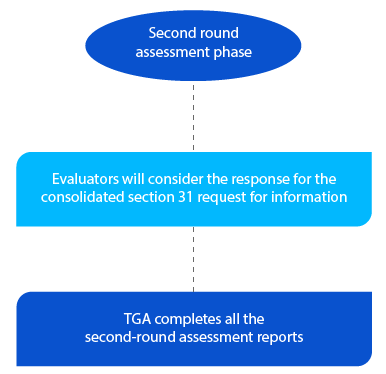
Die TGA hat zwei (02) Monate Zeit für Anträge auf neue Generika für die zweite Runde der Bewertungsberichte und einen (01) Monat für alle anderen Antragsarten. Die Berichte werden nach Abschluss der zweiten Bewertung an die jeweiligen Antragsteller gesendet.
Meilenstein 6
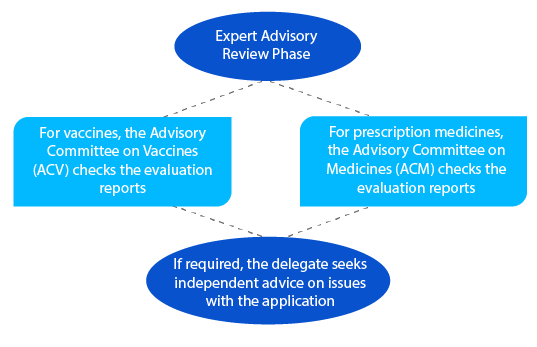
Nach der beratenden Überprüfung sendet die TGA eine Benachrichtigung mit den Einzelheiten der Empfehlung, die sie vom ACV oder ACM erhält.
Meilenstein 7
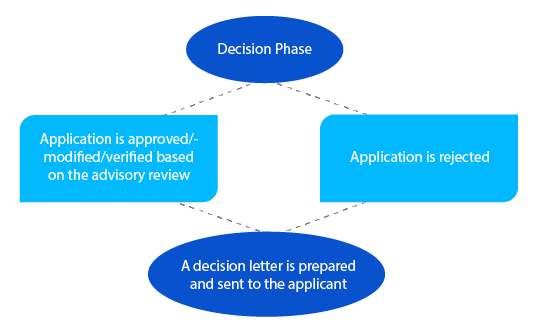
Bei noch offenen Fragen kann der Delegierte in dieser Phase vor einer Entscheidung mit dem Antragsteller in Kontakt treten. Für Anträge gemäß Abschnitt 23 des Therapeutic Goods Act von 1989 (neu bewertete gelistete Arzneimittel im australischen Register für therapeutische Produkte (ARTG)) wird dem Antragsteller innerhalb von achtundzwanzig (28) Tagen nach der Entscheidung eine Benachrichtigung zugesandt.
Meilenstein 8
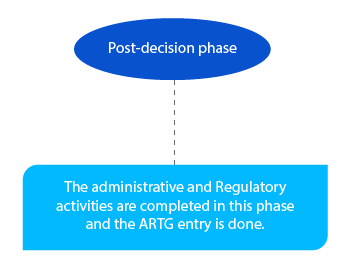
Die ausstehenden Zahlungen werden in dieser Phase beglichen. Dies muss bis zum Ende des Monats nach der Entscheidung des Delegierten abgeschlossen sein.
Da die TGA alle Vorkehrungen trifft, um die Sicherheit, Wirksamkeit und Qualität von verschreibungspflichtigen Arzneimitteln zu gewährleisten und gleichzeitig deren Markteinführungszeit zu verkürzen, liegt die Verantwortung beim Antragsteller, die entsprechenden Einreichungen für einen reibungslosen Registrierungsprozess vorzunehmen. In jeder Phase ist die Zusammenarbeit mit einem End-to-End Regulatory Services Provider, der Experte für die Registrierung verschreibungspflichtiger Arzneimittel ist, die ideale Situation. Kontaktieren Sie eine erfahrene regulatorische Einrichtung für einen konformen Weg; bleiben Sie auf dem Laufenden und bleiben Sie konform.










