
Unerfüllter medizinischer Bedarf (UMN) gehört zu den dringendsten Prioritäten der Gesundheitssysteme. Die sich ständig weiterentwickelnde Wissenschaft und Technologie im Gesundheitswesen birgt das Potenzial, verschiedene Therapieoptionen zu erforschen. Gesundheitsbehörden fördern innovative Therapien, die erhebliche Vorteile für die Lebensqualität der Patienten versprechen. Aufbauend auf der Priorisierung von Innovationen und der Ausrichtung auf unerfüllte Patientenbedürfnisse in der Arzneimittelentwicklung führte die Europäische Arzneimittel-Agentur (EMA) 2016 den PRIority MEdicines (PRIME)-Pfad ein. Seitdem ist der PRIME-Pfad eine Methode, um Zulassungen für innovative Therapien in einem beschleunigten Zeitrahmen zu erteilen. Diese Art von beschleunigtem Verfahren kann von jedem Unternehmen, von Start-ups über mittelständische Biotech-Unternehmen bis hin zu großen multinationalen Organisationen, in Betracht gezogen werden. Die Qualifikation für diesen Pfad ist jedoch auf Produkte beschränkt, die sich in der Entwicklung befinden und noch keine Marktzulassung über das zentrale Verfahren beantragt haben. Die Qualifikationskriterien werden streng angewendet. Zwischen März 2016 und April 2022 erhielten nur 24 % der Anträge die Genehmigung, während 72 % der PRIME-Anträge abgelehnt wurden. Von den 24 %, die für den PRIME-Pfad ausgewählt wurden, gehörte die Mehrheit zum therapeutischen Bereich der Onkologie.
Innovatoren, die Marktzulassungen für seltene Krankheiten oder Orphan-Arzneimittel anstreben, verfügen oft nur über begrenzte Datensätze als Nachweis zur Unterstützung ihrer neuartigen Arzneimittelanträge, wie von den Regulierungsbehörden gefordert. Anträge für Arzneimittel für neuartige Therapien (ATMPs) und Orphan-Arzneimittel stehen in der Regel vor solchen Herausforderungen. Aufgrund begrenzter Patientendaten wird eine ständige Interaktion mit den Regulierungsbehörden gefördert, um bessere Einblicke für die wissenschaftliche Überprüfung und die Genehmigungsanforderungen zu ermöglichen. Das PRIME-Verfahren kann für solche Therapien nützlich sein, da die Regulierungsbehörden frühzeitig eingebunden werden, um proaktive Unterstützung und Anleitung bei der Datenerfassung und Nutzen-Risiko-Bewertung zu bieten.
Vorteile des PRIME-Verfahrens
- Hilft Innovatoren, einen gut ausgearbeiteten Entwicklungsplan zu erstellen.
- Vorteile für Innovatoren durch die Einbindung der Gesundheitsbehörden in einem frühen Entwicklungsstadium; dies trägt zur Erstellung qualitativ hochwertiger Anträge auf Marktzulassung bei.
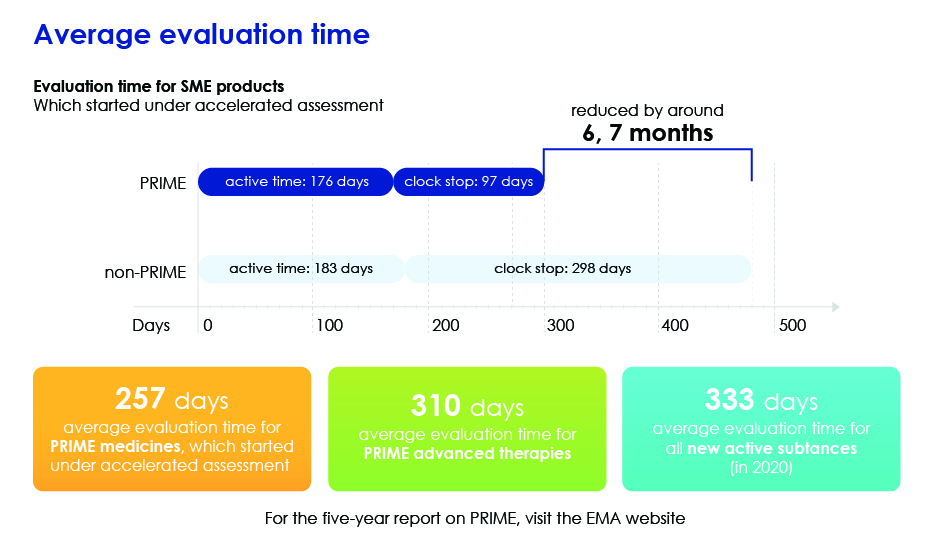
- Beschleunigt die Gesamtbewertung durch Reduzierung der durchschnittlichen Bewertungszeit, sodass Medikamente Patienten schneller erreichen können.
- Unterstützt Innovatoren dabei, ihre Aufmerksamkeit auf die Entwicklung von Medikamenten zu richten, um Patientenergebnisse zu verbessern und unerfüllte Patientenbedürfnisse anzugehen.
Bewertungszeit im Detail
Anträge für das PRIME-Verfahren
Das PRIME-Verfahren priorisiert unerfüllte medizinische Bedürfnisse. Von 384 seit März 2016 eingegangenen PRIME-Anfragen schafften es bis Juni 2021 nur 18 bis zur Marktzulassung.

Sind Sie PRIME-bereit?
Die Existenz des PRIME-Verfahrens ist auf erhebliche unerfüllte medizinische Bedürfnisse und den Fokus des Europäischen Netzwerks der Arzneimittelregulierungsbehörden (EMRN) zurückzuführen, diese Lücken zu schließen. Um die Eignung eines Produkts für das PRIME-Verfahren zu bewerten, muss Folgendes berücksichtigt werden:
- Erkenntnisse: Antragsteller müssen den unerfüllten medizinischen Bedarf darlegen und ein überzeugendes Argument liefern, wie ihr Produkt das Problem angehen wird.
- Potenzial: Antragsteller müssen das vorteilhafte Potenzial der Therapie im Rahmen der Kriterien für unerfüllten medizinischen Bedarf aufzeigen.
- Präklinische Daten: Antragsteller müssen Daten zur Wirksamkeit oder Leistung der Therapie im menschlichen biologischen System vorlegen. Nicht-klinische Modelle, so genau sie auch sein mögen, liefern jedoch keinen exakten Überblick über ihr Verhalten im menschlichen biologischen System.
- Entwicklungsstadium: Antragsteller müssen das richtige Stadium für den Eintritt in das PRIME-Verfahren identifizieren, um optimale Anleitung von den Regulierungsbehörden zu erhalten und mit dem Antrag fortzufahren.
Nach der PRIME-Zulassung
Sobald einem Antragsteller die Möglichkeit gewährt wurde, den beschleunigten Weg zu beschreiten, wird die EMA:
- Einen Berichterstatter aus dem Ausschuss für Humanarzneimittel (CHMP) oder im Falle von Arzneimitteln für neuartige Therapien aus dem Ausschuss für neuartige Therapien (CAT) benennen.
- Organisieren Sie ein Auftakttreffen mit dem CHMP/CAT-Berichterstatter und einer multidisziplinären Expertengruppe, um Anleitung zum gesamten Entwicklungsplan und zur regulatorischen Strategie zu geben.
- Benennen Sie eine zentrale Kontaktperson für den Antragsteller.
- Bieten Sie wissenschaftliche Beratung bei jedem wichtigen Entwicklungsschritt an, unter Einbeziehung weiterer Interessengruppen wie Organisationen für die Bewertung von Gesundheitstechnologien – um Patienten einen schnelleren Zugang zu neuen Medikamenten zu ermöglichen.
- Bestätigen Sie zum Zeitpunkt eines Antrags das Potenzial für eine beschleunigte Bewertung unter Berücksichtigung der Marktzulassung.
Ist Ihr Antrag für den PRIority MEdicine-Pfad bereit (PRIME-ready)? Kontaktieren Sie Freyr noch heute und lassen Sie ihn bewerten. Erfahren Sie mehr darüber, wie wir Ihnen bei Ihrer regulatorischen Strategie und der PRIME-Pfad-Bezeichnung helfen können. Bleiben Sie informiert. Bleiben Sie konform.









