
Innovationen bei Arzneimittel-Medizinprodukt-Kombinationen haben zu erheblichen Fortschritten in der Patientenversorgung geführt. Arzneimittelprodukte in Verbindung mit Medizinprodukten ermöglichen eine gezielte Arzneimittelabgabe, verbesserte Therapieergebnisse und eine höhere Patientenadhärenz. Die Navigation in der regulatorischen Landschaft für Arzneimittel-Medizinprodukt-Kombinationen kann jedoch komplex sein.
Dieser Blogbeitrag beleuchtet die Überlegungen und Herausforderungen im Zusammenhang mit den regulatorischen Abläufen für Arzneimittel-Medizinprodukt-Kombinationen und bietet Einblicke in die Optimierung der Prozesse.
Übersicht und regulatorischer Rahmen für Arzneimittel-Medizinprodukt-Kombinationen
Arzneimittel-Medizinprodukt-Kombinationen verbinden die therapeutischen Effekte pharmazeutischer Arzneimittel mit den Verabreichungsfähigkeiten von Medizinprodukten. Zu den Arzneimittel-Medizinprodukt-Kombinationen gehören medikamentenfreisetzende Stents, Inhalatoren und Atemwegsgeräte, transdermale Pflaster, Insulin-Verabreichungssysteme, Arzneimittel-Infusionssysteme und medikamentenbeschichtete Ballons. Gezielte Verabreichung, verbesserte Wirksamkeit, höhere Patientenadhärenz und präzise Kontrolle über die Behandlung sind einige der bemerkenswerten Eigenschaften dieser Produkte.
Regulierungsbehörden wie die US FDA (United States Food and Drug Administration), die EMA (European Medicines Agency) und andere haben Leitlinien für Arzneimittel-Medizinprodukte-Kombinationen festgelegt. In den letzten Jahren gab es bemerkenswerte Entwicklungen im regulatorischen Umfeld, mit einem verstärkten Fokus auf Harmonisierung, risikobasierten Bewertungen und der Überwachung nach dem Inverkehrbringen.
Wichtige Überlegungen für regulatorische Abläufe
Bei der Navigation durch die regulatorischen Abläufe für Arzneimittel-Medizinprodukt-Kombinationen sind einige der zu berücksichtigenden Punkte unten aufgeführt:
Verständnis der Produktklassifizierung und der regulatorischen Wege
Das Verständnis der Klassifizierung von Arzneimittel-Medizinprodukt-Kombinationen und die Auswahl des geeigneten regulatorischen Weges sind entscheidend. Hersteller müssen festlegen, ob es sich um eine Arzneimittel-Medizinprodukt-Kombination, eine Kategorie von arzneimittelbeschichteten Medizinprodukten oder eine Kategorie von gemeinsam verpackten Produkten handelt. Die Auswahl des korrekten Weges für den spezifischen Produkttyp ist entscheidend für einen erfolgreichen Marktzugang.
Berücksichtigung der wissenschaftlichen und technischen Anforderungen
Dazu gehört die Sicherstellung der Kompatibilität zwischen den Arzneimittel- und Gerätekomponenten, die Durchführung von Stabilitätsstudien zur Bewertung der Produktlagerfähigkeit, die Validierung von Herstellungsprozessen und die Implementierung von Risikobewertungen zur Identifizierung und Minderung potenzieller Gefahren.
Patientenversorgung und Usability-Tests
Patientenversorgung und Usability Engineering spielen eine wichtige Rolle bei der Entwicklung solcher Kombinationsprodukte. Die Berücksichtigung von Faktoren wie Benutzeroberfläche, Ergonomie, Gerätehandhabung und Patientenadhärenz während der Produktentwicklung trägt dazu bei, deren sichere und effektive Anwendung durch Patienten und medizinisches Fachpersonal mit minimalen Fehlern zu gewährleisten.
Überlegungen nach der Markteinführung
Verpflichtungen nach dem Inverkehrbringen sind ein kritischer Aspekt der regulatorischen Compliance für Arzneimittel-Medizinprodukt-Kombinationen. Hersteller müssen Prozesse für die Meldung unerwünschter Ereignisse, die Überwachung nach dem Inverkehrbringen (Post-Market Surveillance) und die Vigilanzberichterstattung etablieren, um die Sicherheit und Leistung ihrer Produkte zu überwachen.
Auf dem Laufenden bleiben bezüglich aktueller regulatorischer Leitlinien und Aktualisierungen
Die Verfolgung der neuesten Leitlinien und Aktualisierungen ist entscheidend, um die Compliance sicherzustellen und regulatorische Strategien an die aktuellen Erwartungen anzupassen. Die regulatorische Landschaft für Arzneimittel-Medizinprodukt-Kombinationen entwickelt sich ständig weiter. Die Ausrichtung an den Leitlinien der FDA, der EU-Medizinprodukte-Verordnung (MDR) und des International Council for Harmonization of Technical Requirements for Pharmaceuticals for Human Use (ICH) kann Herstellern helfen, konform zu bleiben.
Bewährte Verfahren zur Optimierung regulatorischer Abläufe
Um die regulatorischen Abläufe für Arzneimittel-Medizinprodukte-Kombinationen zu optimieren, können Pharmaunternehmen die im folgenden Tortendiagramm dargestellten bewährten Verfahren anwenden:
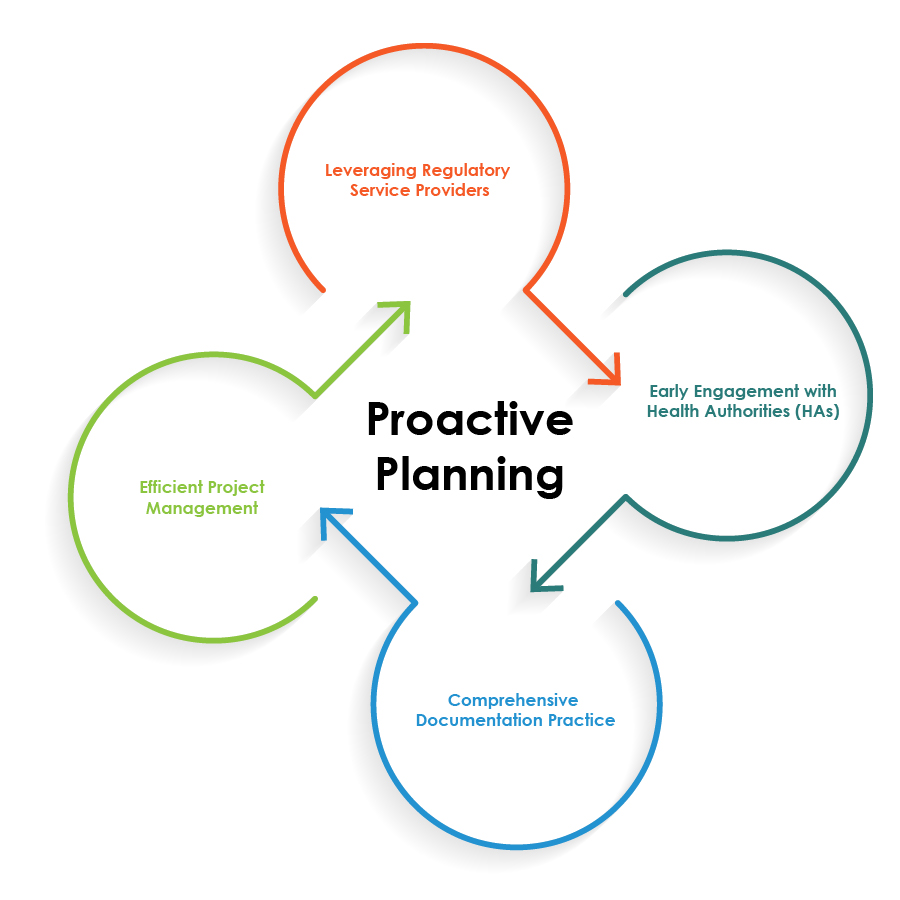
Proaktive Planung ist der Grundstein für reibungslose regulatorische Abläufe bei Arzneimittel-Medizinprodukte-Kombinationen.
Zukünftige Trends und Herausforderungen
Die Beobachtung zukünftiger Trends und Schwächen ist entscheidend für Pharmaunternehmen und Fachleute im Bereich Regulierung, die an den regulatorischen Abläufen dieser Produkte beteiligt sind. Im Folgenden sind einige Trends und Herausforderungen aufgeführt, die es zu beachten gilt:
- Neue Technologien: Nanotechnologie, 3D-Druck und verwandte Anwendungen beeinflussen die Entwicklung innovativer Arzneimittel-Medizinprodukte-Kombinationen. Diese technologischen Trends ermöglichen eine gezielte Medikamentenabgabe, personalisierte Medizin und eine verbesserte Patientenüberwachung. Sie stellen jedoch auch einzigartige regulatorische Herausforderungen in Bezug auf Sicherheit, Wirksamkeit und Qualitätskontrolle dar.
- Cybersicherheit: Mit der zunehmenden Vernetzung von Medizinprodukten wird die Gewährleistung der Datensicherheit und der Schutz vor Cyberbedrohungen von größter Bedeutung. Die Integration robuster Cybersicherheitsmaßnahmen und die Kenntnis der bewährten Verfahren für die Gerätesicherheit sind entscheidende Überlegungen für regulatorische Abläufe.
- Verschiedene Herausforderungen: Dazu gehören komplexe globale Lieferketten, wie die Beschaffung von Rohstoffen, die Verfügbarkeit von Komponenten und die Herstellungsprozesse, die Herausforderungen bei der Aufrechterhaltung der Einhaltung von Vorschriften und der Sicherstellung der Produktqualität darstellen. Robuste Praktiken im Lieferkettenmanagement, Risikobewertungen und die Überwachung von Lieferanten sind unerlässlich, um diese Herausforderungen anzugehen und die damit verbundenen Risiken zu mindern.
Die Navigation in der regulatorischen Landschaft für Arzneimittel-Medizinprodukt-Kombinationen erfordert ein umfassendes Verständnis des regulatorischen Rahmens, der neuesten Leitlinien und bewährter Praktiken. Die Berücksichtigung wichtiger Aspekte, das Bleiben auf dem neuesten Stand der Änderungen und die Implementierung bewährter Praktiken werden Pharmaunternehmen dabei unterstützen, ihre regulatorischen Abläufe zu optimieren. Die Zusammenarbeit mit regulatorischen Dienstleistern ermöglicht es Unternehmen, spezialisiertes Wissen und Erfahrungen zu nutzen und ihre Chancen auf regulatorischen Erfolg in diesem sich ständig entwickelnden und anspruchsvollen Bereich zu optimieren. Mit unserer ausgewiesenen Expertise in der Einhaltung globaler regulatorischer Normen kann Freyr Ihnen helfen, einen konformen Produktlebenszyklus zu erreichen. Um mehr zu erfahren, kontaktieren Sie uns.









