
Um die Zugänglichkeit innovativer Medikamente für Patienten im UK nach dem Brexit zu verbessern, wurde im Januar 2021 ein neuer und beschleunigter Zulassungsweg, bekannt als Innovative Licensing and Access Pathway (ILAP), eingeführt. Sein Hauptziel war es, allen Beteiligten einen integrierten Fahrplan zur Verfügung zu stellen, der den Prozess der Produktentwicklung verbessert. ILAP unterstützt darüber hinaus kommerzielle und nicht-kommerzielle Entwickler, indem es den Zugang innovativer Medikamente für die Patientenpopulation durch die Verkürzung der Markteinführungszeit erleichtert. Pharmaunternehmen können ILAP als Weg in Betracht ziehen, sobald die nicht-klinischen Daten konsolidiert sind. Es ist anwendbar für New Chemical Entities (NCE), biologische Medikamente, neue Indikationen und neu positionierte Medikamente.
Der ILAP ist eine Initiative, die gemeinsam von der Medicines and Healthcare products Regulatory Agency (MHRA) in Zusammenarbeit mit dem All-Wales Therapeutics and Toxicology Centre (AWTTC), dem National Institute of Health and Care Excellence (NICE) und dem Scottish Medicines Consortium (SMC) als ständige Partner entwickelt wurde. Zu den unterstützenden Partnern des ILAP gehören der National Health Service England (NHS), die Health Research Authority (HRA) und das National Institute for Health Research (NIHR). Gemeinsam liefern die Beteiligten verbesserte regulatorische, wissenschaftliche, ethische und kommerzielle Beiträge in der frühen Phase der Medikamentenentwicklung während klinischer Studien.
Nach Ansicht von Freyr bietet der ILAP große Chancen für Entwickler innovativer Behandlungen, insbesondere für diejenigen, die ungedeckte Patientenbedürfnisse ansprechen. Für eine relativ geringe Gebühr (ca. 8000 £) könnte ein Unternehmen frühzeitige Beratung erhalten, eine Bezeichnung für sein Produkt erlangen und ein Zielentwicklungsprofil vereinbaren. Dies hat das Potenzial, eine erhebliche Menge an Zeit im gesamten Produktentwicklungszyklus einzusparen. Es gibt auch Vorteile, über die Marktzulassung hinauszublicken und frühzeitig Vorbereitungen für Verhandlungen über die Kostenerstattung zu treffen.
Der ILAP schneidet im Vergleich zu ähnlichen Programmen innerhalb des europäischen Arzneimittelnetzwerks (wie dem PRIME) günstig ab. Obwohl Konzept und Umsetzung unterschiedlich sind, hat der ILAP breitere Akzeptanzkriterien und eine höhere Akzeptanzrate. Der ILAP bietet auch einen Weg zur Integration mit dem Project Orbis der United States Food and Drug Administration (USFDA) für neuartige Onkologieprodukte.
Wie beantragt man den ILAP?
Um Zugang zum ILAP zu erhalten, müssen Antragsteller einen Innovation Passport (IP) beantragen. Die Sicherung einer IP-Bezeichnung ermöglicht es Arzneimittelentwicklern, den Weg auf der Grundlage der Nachweise zu nutzen, die erforderlich sind, damit ein Produkt die von NICE, SMC, AWTTC und der MHRA definierten Zulassungskriterien erfüllt.
Diese Bezeichnung wirkt als Katalysator für innovative Produkte von der präklinischen bis zur mittleren Entwicklungsphase. Der IP kann zur Definition eines Target Development Profile (TDP)-Dokuments führen. Das TDP ist ein Fahrplan, der den Zugang zu den ILAP-Partnern in frühen Phasen des Arzneimittelentwicklungszyklus erleichtert, um Patienten einen schnelleren Zugang zu neuen und innovativen Behandlungen zu ermöglichen und zu beschleunigen. Patienten sind Teil dieses gesamten Prozesses. Mehrere vom ILAP bereitgestellte Tools unterstützen Antragsteller in allen Phasen des Design-, Entwicklungs- und Genehmigungsprozesses.
Kriterien für die Innovative-Passport-Bezeichnung
Die MHRA-Leitlinien klären die Kriterien für eine IP-Bezeichnung. Dies ist besonders relevant für innovative Produkte und schneidet auch im Vergleich zu gleichwertigen Programmen in Europa günstig ab.
Zukünftig kann sich eine spezifische Anwendbarkeit des IP für Medizinprodukte und Kombinationsprodukte, Bereiche, in denen es stets erhebliche Innovationen gibt, als vorteilhaft erweisen.
Die IP-Bezeichnung wird von den ständigen und unterstützenden Partnern anhand der folgenden Kriterien bewertet:
- Kriterium 1: Details zur Erkrankung, zum Patienten oder zum Bereich der öffentlichen Gesundheit
- Für lebensbedrohliche und schwerwiegende Erkrankungen
- Wenn der Bedarf für Patienten entscheidend ist
- Kriterium 2: Das Arzneimittel erfüllt einen oder mehrere spezifische Bereiche, die Folgendes umfassen:
- Innovatives Arzneimittel
- Arzneimittel mit einer neuen Indikation
- Arzneimittel für seltene Krankheiten
- Arzneimittel in Entwicklung zum Zweck der öffentlichen Gesundheit im Vereinigten Königreich
- Kriterium 3: Das Arzneimittel hat das Potenzial zu bieten
- Eine kurze Erläuterung, wie das vorgeschlagene Arzneimittel oder die Indikation den Patienten zugutekommen wird.
- Ansichten von Patienten oder Patientenorganisationen werden begrüßt.
Nach Einreichung des IP-Antrags findet ein Treffen zwischen den Antragstellern und der MHRA statt, um zu klären, ob das Produkt die drei (03) Kriterien erfüllt.
Gemäß den neuesten Informationen vom Januar 2022 hat die MHRA einundsiebzig (71) Anträge erhalten, von denen einundvierzig (41) zu einer IP-Bezeichnung führten, zweiundzwanzig (22) bearbeitet werden und sieben (07) Anträge abgelehnt wurden.
Der richtige Zeitpunkt für den Eintritt in den ILAP wird unten genannt.
- Im frühen bis mittleren Entwicklungsstadium des Produkts
- Wenn relevante Daten verfügbar sind
- Wenn die Antragsteller das Bedürfnis verspüren, Input von den Stakeholdern zu erhalten
- Die Antragsteller streben an, neue innovative Ansätze zu verfolgen
- Nicht wenn sich das Produkt dem Ende der Entwicklungsphase nähert
Übersicht über die Arzneimittelentwicklung
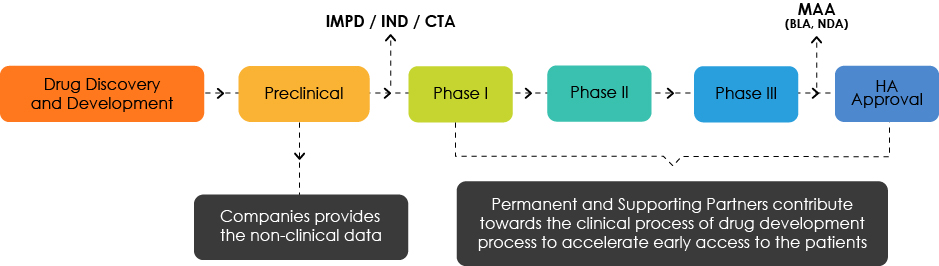
Das Target Development Profile (TDP) verstehen
Die TDP-Experten analysieren die Produkteigenschaften und zeigen Mängel aus regulatorischer Sicht auf. Sie sind dafür verantwortlich, den Arzneimittelentwicklern einen Fahrplan aufzuzeigen, der einen frühen Patientenzugang zu ihren Produkten ermöglicht.
TDP ist ein Dokument, das in Echtzeit gemäß den Anforderungen der Produktentwicklung aktualisiert wird. Daher erfährt ein Produkt mehrere TDP-Änderungen, sobald neue Daten generiert werden.
Die Patientenzugänglichkeit zu essenziellen Arzneimitteln kann durch Marktverzögerungen beeinträchtigt werden. Um solche Szenarien zu vermeiden, fungieren beschleunigte Verfahren als Katalysator. Das ILAP ist ein Beispiel für ein flexibles Zulassungsverfahren, das in der gesamten Branche gut akzeptiert ist und die Entwicklungszeit innovativer Arzneimittel beschleunigen kann. Die detaillierten Kriterien des britischen Gesundheitssystems ermöglichen es Antragstellern, ihre Berechtigung für die Beantragung einer IP-Bezeichnung zu prüfen. Die Förderung ungedeckter klinischer und Patientenbedürfnisse durch beschleunigte Verfahren wie das ILAP erleichtert den Markteintritt und kann gefährdeten Patientengruppen Erleichterung verschaffen. Um die Interessen der Patienten zu schützen, gehen die Gesundheitsbehörden keine Kompromisse bei der Sicherheit, Wirksamkeit oder Qualität des Produkts ein, während sie gleichzeitig einen beschleunigten Genehmigungsprozess gewährleisten. Die End-to-End regulatorischen Dienstleistungen von Freyr erleichtern den Dokumentationsprozess, um die Innovative Passport-Bezeichnung in beschleunigter Zeit zu unterstützen und so dazu beizutragen, dass Ihre Produkte Patienten früher erreichen. Kontaktieren Sie Freyr.










