
Ab dem 31. Januar 2022 ist die neue pharmazeutische Verordnung der Europäischen Union (EU) für klinische Prüfungen (Clinical Trials Regulation, CTR) verbindlich geworden und ersetzt die Richtlinie über klinische Prüfungen 2001/20/EG. Die Verordnung harmonisiert die Protokolle für die Bewertung und Überwachung klinischer Prüfungen in der gesamten EU. Die Leitlinien wurden überarbeitet, um einen einheitlichen Ansatz in der klinischen Forschung zu fördern, wobei die Sicherheit der Teilnehmer an klinischen Prüfungen und eine verstärkte öffentliche Offenlegung betont werden.
Die Verordnung führt ein neues zweiteiliges Bewertungssystem für alle klinischen Prüfungen in der EU ein. Teil I besteht aus einer wissenschaftlichen Bewertung der zentralen Unterlagen der klinischen Prüfung und Teil II aus einer ethischen Bewertung der Dokumentation auf nationaler Ebene. Nach dieser zweiteiligen Bewertung wird jeder Mitgliedstaat eine einheitliche Entscheidung über die Prüfung treffen und den Sponsor über das Klinische Studien Informationssystem benachrichtigen.
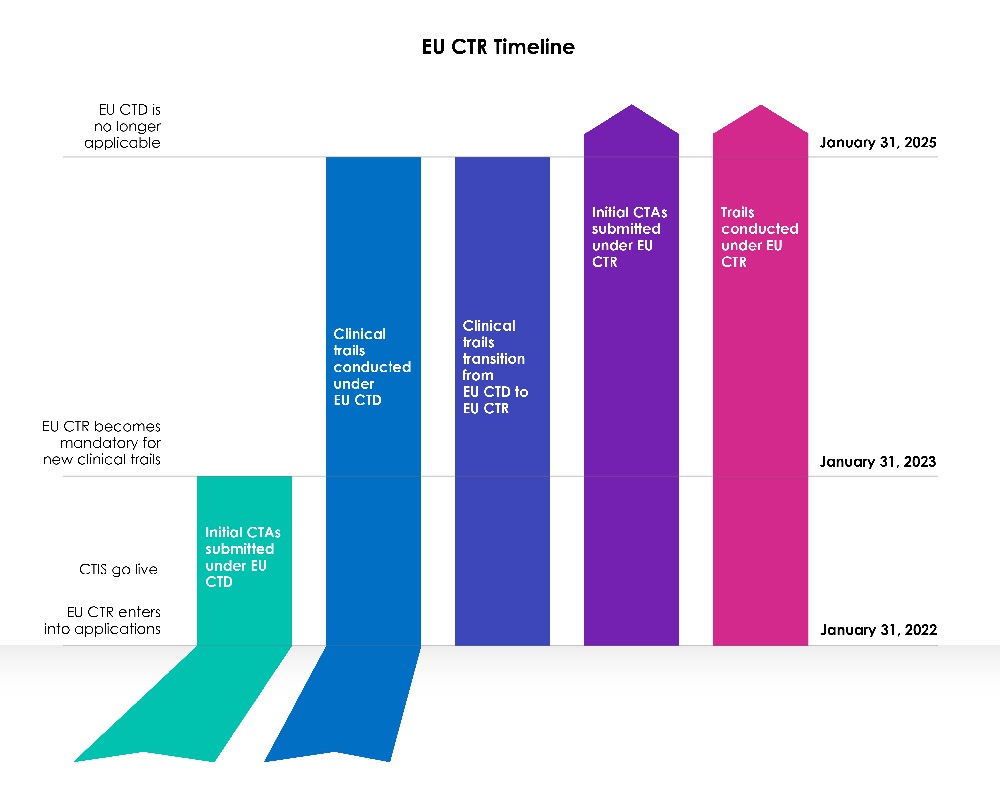
Übergangsfristen für neue Antragsteller
Eine dreijährige Übergangsphase begann mit dem Startdatum des EU CTIS.
Jahr 1 (31. Januar 2022 bis 30. Januar 2023):
Die Richtlinie 2001/20/EG der Europäischen Union (EU) über klinische Prüfungen (EU-CTD) regelte klinische Prüfungen in der EU seit 2004. Sie zielte darauf ab, Regeln zu standardisieren und die Patientensicherheit in klinischen Prüfungen erheblich zu verbessern. In der Praxis führte sie jedoch zu unbeabsichtigten Folgen. Im ersten Jahr nach der Einführung von CTIS konnten Sponsoren wählen, ob sie einen neuen Antrag auf klinische Prüfung (CTA) entweder über das Clinical Trial Information System (CTIS) gemäß der Richtlinie über klinische Prüfungen (CTD: Richtlinie 2001/20/EG) einreichen oder CTIS gemäß der aktuellen Gesetzgebung, der Verordnung über klinische Prüfungen (EU) Nr. 536/2014, nutzen wollten.
Beide Ansätze waren umsetzbar, und die Sponsoren hatten die Möglichkeit zu wählen, welche Gesetzgebung sie anwenden wollten.
Die Member States waren bereit, das Clinical Trial Information System (CTIS) zu nutzen und nahmen am ersten Tag des CTIS-Betriebs Anträge gemäß der neuen Gesetzgebung, der Verordnung über klinische Prüfungen (EU CTR), entgegen.
Jahre 2 und 3 (31. Januar 2023 bis 31. Januar 2025):
Ab dem 31. Januar 2023 müssen alle neuen Anträge für klinische Prüfungen über das CTIS gemäß der neuen Gesetzgebung (CTR) eingereicht werden.
Neue Anträge für klinische Prüfungen dürfen nicht mehr in EudraCT gemäß der Richtlinie über klinische Prüfungen (CTD) eingereicht werden. Die EU-Richtlinie über klinische Prüfungen erlaubt nach dem 31. Januar 2023 keine Aufnahme neuer Member States mehr. Prüfungen, die unter der CTD durchgeführt wurden, müssen zuerst überführt werden, danach kann ein zusätzlicher, die Member States betreffender Antrag über EU CTIS eingereicht werden.
Für bestehende Antragsteller
CT-Anträge, die vor dem 30. Januar 2023 nach der alten Gesetzgebung (CTD) unter Verwendung von EudraCT eingereicht wurden, dürfen bis zum Abschluss gemäß dieser Richtlinie (CTD: Richtlinie 2001/20/EG) bis zum 30. Januar 2025 weitergeführt werden. Die Verfahren bleiben unverändert, und Sponsoren können wesentliche Änderungen und Abschlussmeldungen von Studien gemäß den Vorschriften einreichen. EudraCT bleibt während der Übergangszeit aktiv, um die Fortsetzung dieser Studien zu ermöglichen.
Es ist jedoch wichtig zu beachten, dass Übergangsanträge jederzeit während der dreijährigen (03) Übergangsfrist eingereicht werden können. Sponsoren werden ermutigt, den Prozess frühzeitig in der Übergangsfrist abzuschließen, um die Kontinuität der klinischen Studien in der EU über den 30. Januar 2025 hinaus zu gewährleisten, unter Berücksichtigung gesetzlicher Feiertage und der zwei (02)wöchigen Winterpause.
Nicht übertragbare Studien
- Prüfungen, die entweder bereits abgeschlossen sind oder kurz vor dem Ende der EU/EEA-Übergangsperiode abgeschlossen werden, dürfen nicht überführt werden.
- Wenn eine Abschlussmeldung der Prüfung in allen EU/EEA Member States abgeschlossen wurde, das globale Ende der Prüfung jedoch noch nicht gemeldet wurde, sollte die Studie nicht überführt werden. Gemäß der Richtlinie sollten das globale Ende der Prüfung und die zusammenfassenden Ergebnisse der Prüfung über EudraCT veröffentlicht werden.
- Studien, die vor der Umsetzung der Richtlinie 2001/20/EG begonnen wurden, profitieren nicht von einem solchen Übergangsverfahren. Wenn sie interventionell sind und nach dem Ende der CTR-Übergangsphase weitergeführt werden müssen, muss ein neuer CT-Antrag gemäß der CTR gestellt werden.
- Pädiatrische Prüfungen, die außerhalb des EU/EEA durchgeführt wurden, für die jedoch eine EudraCT-Nummer zugewiesen wurde, sollten ebenfalls nicht umgestellt werden.
- Studien, die nach Ablauf der Übergangsfrist pausiert sind, können nicht überführt werden. Die Wiederaufnahme der Studie unter diesen Umständen würde die Einreichung eines neuen CT-Antrags gemäß der CTR erfordern.
CTIS EMA technische Updates von der EMA , um seine Funktionen und Leistungsmerkmale zu verbessern. Bei größeren Änderungen am CTIS EMA die EMA Release-Hinweise, in denen die Änderungen am System beschrieben werden. Updates können Verbesserungen bestehender Funktionen und Leistungsmerkmale, die Hinzufügung neuer Funktionen sowie funktionale und technische Optimierungen umfassen. Ein erfahrener Partner im Bereich Regulatory Affairs kann potenzielle Herausforderungen angehen und Sponsoren im Rahmen ihrer klinischen Entwicklungsstrategien beim Übergang bestehender und künftiger Studien unterstützen. Klicken Sie hier, um mehr über das CTIS die Expertise von Freyr in diesem Bereich zu erfahren: https://www.freyrsolutions.com/medical-devices/regulatory-affairs.










