
Die US FDA hat im Dezember 2022 einen Leitfaden veröffentlicht, eine Überarbeitung des Leitfadens vom Juli 2022 mit dem Titel „Failure to Response to an ANDA Complete Response Letter (CRL) Within the Regulatory Timeframe Guidance for Industry“. Er soll Antragsteller von Abbreviated New Drug Applications (ANDAs), die gemäß Abschnitt 505(j) des Federal Food, Drug, and Cosmetic Act (FD&C Act) (21 U.S.C. 355(j)) eingereicht werden, Orientierung bieten. Eine vollständige und relevante Antwort auf einen CRL ist entscheidend für die Zulassung des Generikums. Das Leitliniendokument enthält Empfehlungen zu den Folgen des Erhalts eines CRL und zu den Maßnahmen, die die FDA ergreifen kann, wenn der CRL nicht innerhalb der festgelegten Frist beantwortet wird.
Die FDA muss sicherstellen, dass die zugelassenen Generika die Standards für Sicherheit, Qualität, Wirksamkeit und Erschwinglichkeit erfüllen. Wenn die ANDA die regulatorischen Anforderungen der FDA nicht erfüllt, wird ein CRL an den Antragsteller gesendet, das die während der Prüfung festgestellten Mängel enthält.
Im Folgenden wird bildlich beschrieben, was ein Antragsteller innerhalb eines Jahres nach Erhalt des CRL tun kann:
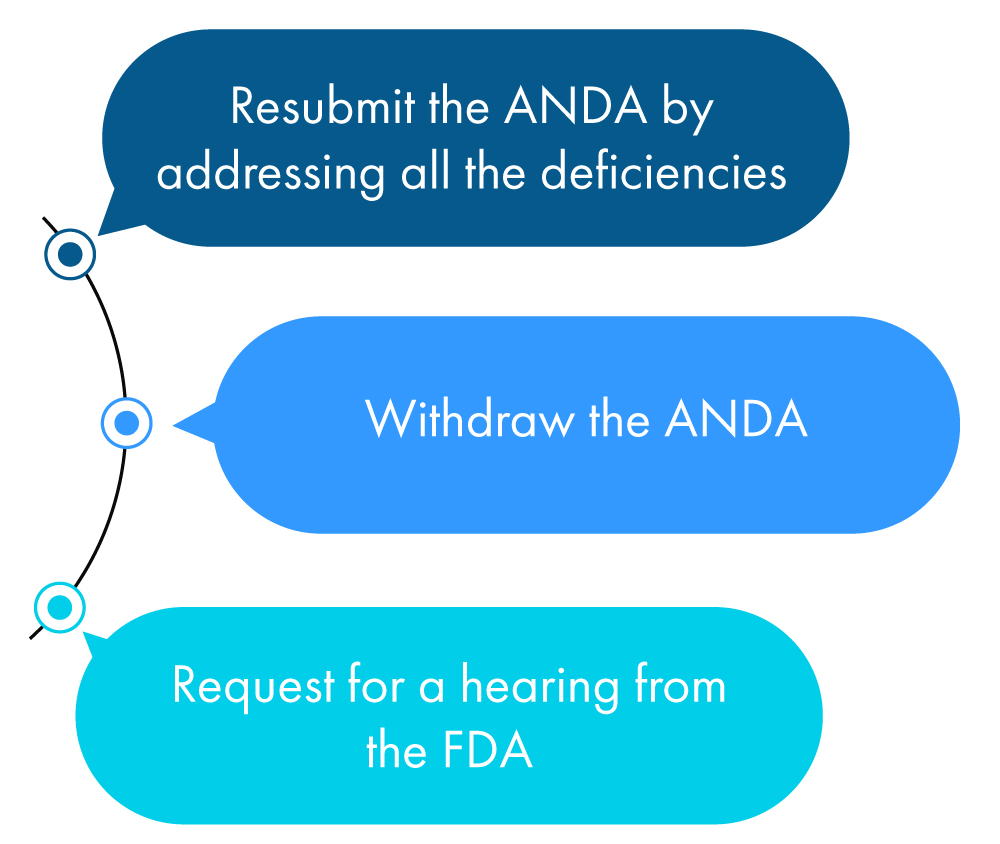
Wenn der Antragsteller keine der oben genannten Maßnahmen ergreift, betrachtet die FDA dies als Antrag auf Rücknahme der ANDA, es sei denn, der Antragsteller hat eine Fristverlängerung beantragt, um alle im CRL genannten Unstimmigkeiten zu prüfen.
Was geschieht nach einem (01) Jahr nach Ausstellung des CRL?
Die FDA sendet eine schriftliche Benachrichtigung, dass der Antragsteller ab der Benachrichtigung dreißig (30) Tage Zeit für Folgendes hat:
- Gründe angeben, warum die ANDA nicht zurückgezogen werden sollte
- Antrag auf Fristverlängerung zur Behebung aller im CRL genannten Mängel
Sobald die FDA einen Antrag auf Fristverlängerung vom Antragsteller erhält, berücksichtigt sie verschiedene Faktoren, wie unten aufgeführt, und entscheidet anschließend über den Antrag:
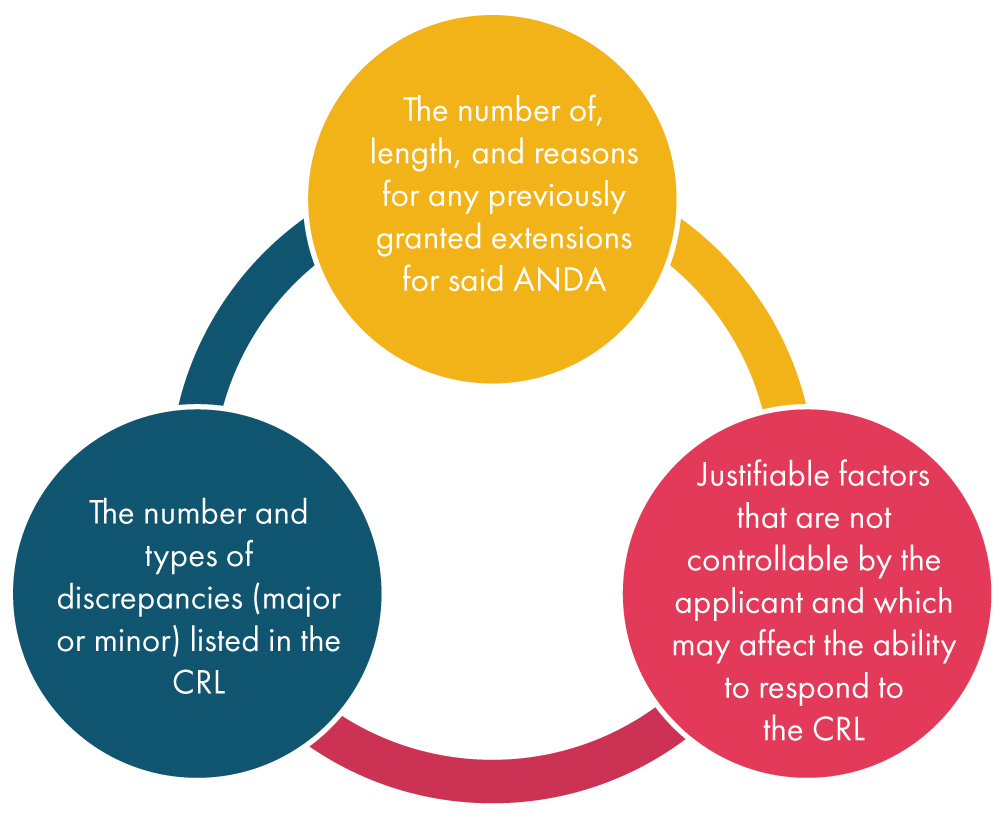
Was ist eine Änderung?
Der Antragsteller muss einen Antrag auf Fristverlängerung zur Beantwortung eines CRL durch eine Änderung einreichen. Die FDA stuft eine Änderung als wesentlich oder unwesentlich ein, basierend auf ihrer Auswirkung auf den Genehmigungsprozess.
Wichtige FDA-Empfehlungen, die Antragsteller kennen sollten:
- Die FDA wird eine geringfügige Änderung als wesentliche Änderung neu einstufen, wenn die Änderung nach einem Jahr des CRL eingereicht wird, es sei denn, die ANDA betrifft ein Produkt auf der Liste der Arzneimittelengpässe gemäß Abschnitt 506E des FD&C Act (21 U.S.C. 356e), oder ist Gegenstand einer Reaktion auf einen vom Sekretär des US-Gesundheitsministeriums gemäß Abschnitt 319 des Public Health Service Act (42 U.S.C. 247d) erklärten öffentlichen Gesundheitsnotstand, oder es wird erwartet, dass es zum Zeitpunkt der Einreichung denselben Kriterien unterliegt, die für eine solche Erklärung gelten.
- Wenn der Antragsteller die Unstimmigkeiten im CRL nicht innerhalb der von der FDA gewährten Fristverlängerung behebt, kann die FDA die Rücknahme der ANDA in Betracht ziehen.
- Benötigt der Antragsteller mehr als die dreißigtägige Verlängerungsfrist, kann er eine weitere Verlängerung beantragen. Der Antrag muss dann neue Informationen enthalten, die es der FDA ermöglichen, zu entscheiden, ob die Verlängerung gewährt werden kann.
Der Erhalt eines CRL von der FDA kann für ANDA-Antragsteller eine große Herausforderung darstellen. Von der Behebung der Unstimmigkeiten bis zur Angabe der korrekten Gründe/Informationen für eine Verlängerung müssen alle relevanten Anforderungen erfüllt werden, um eine schnellere Arzneimittelzulassung zu gewährleisten. Freyr ist ein erwiesenermaßen erfahrener Regulierungsexperte mit umfassendem Wissen bei der Beantwortung von CRLs und der Sicherstellung der Einhaltung der FDA-Anforderungen. Kontaktieren Sie uns jetzt für End-to-End strategische Unterstützung bei ANDA-Einreichungen.










