
Die Einführung hochwertiger und preisgünstiger Generika auf dem Markt ist eine weit verbreitete Herausforderung für zahlreiche Gesundheitsbehörden. Mehrere Länder ergreifen Maßnahmen, um dieses Problem anzugehen und mehr Generika auf dem Markt verfügbar zu machen, wodurch der Wettbewerb auf globaler Ebene zunimmt.
Sprechen wir über den Pharmamarkt der US. Die Entwicklung von Generika ist ein bereits schwieriger Prozess. Zusätzlich müssen Hersteller sicherstellen, dass die Einreichungen für Abbreviated New Drug Applications (ANDA) alle vorgeschriebenen Anforderungen für schnellere Zulassungen erfüllen. Um dies zu erleichtern, kündigte die Food and Drug Administration (FDA) im Jahr 2017 den Drug Competition Action Plan (DCAP) an, um den Wettbewerb bei der Entwicklung von Generika zu fördern.
Mit dem DCAP zielt die FDA darauf ab, die Hindernisse für die Entwicklung von Generika zu beseitigen, indem sie einen schnelleren Markteintritt ermöglicht, damit diese bedürftigen Patienten zu erschwinglichen Preisen zur Verfügung stehen. Während die Markteinführungszeit mit diesem Plan verkürzt wird, gewährleistet die FDA auch die Sicherheit und Wirksamkeit der Generika mithilfe eines transparenten und effizienten Arzneimittelprüfverfahrens.
Wichtige Merkmale des DCAP
Abstimmung mit dem Generic Drug User Fee Program (GDUFA) II – Nachfolgend finden Sie eine anschauliche Erklärung, wie dies erreicht wird.
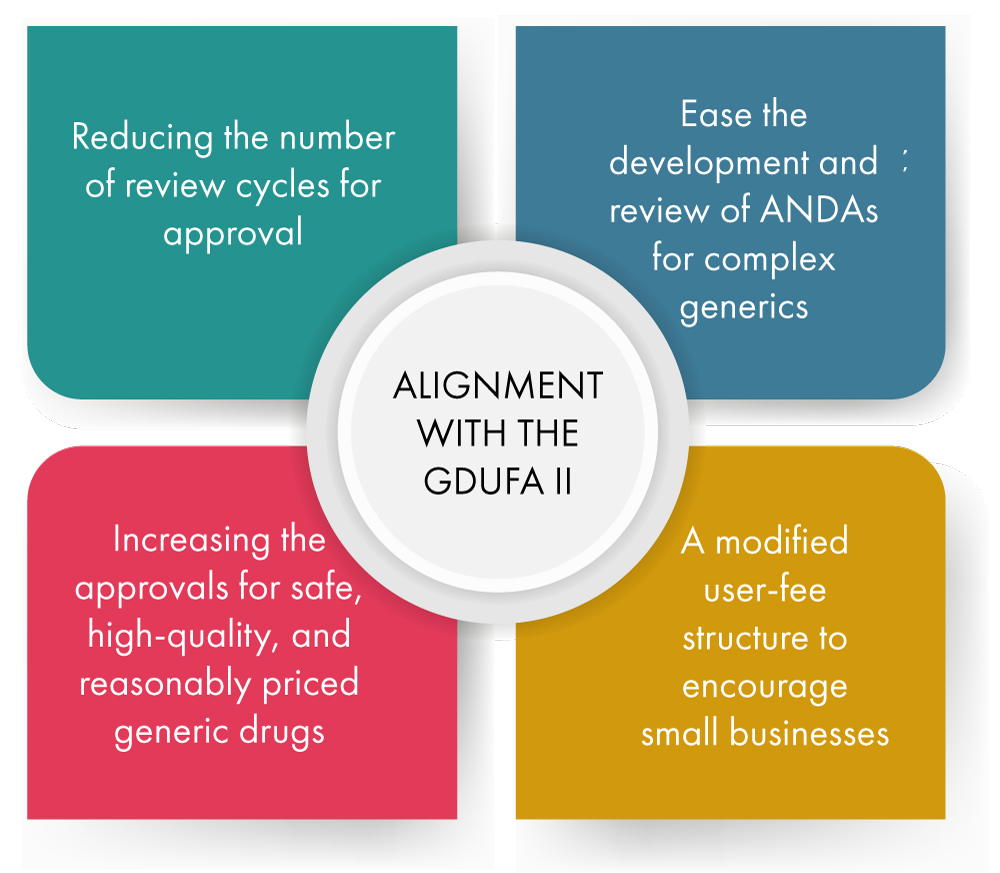
Steigern Sie die Effizienz der Entwicklung von Generika und beschleunigen Sie gleichzeitig den Prüf- und Genehmigungsprozess – Die FDA ergreift verschiedene Initiativen, um sicherzustellen, dass der Prüf- und Genehmigungsprozess für Generika alle Sicherheitsstandards erfüllt, bevor diese schneller auf den Markt gebracht werden können. Nachfolgend wird dargestellt, wie dies geschieht.
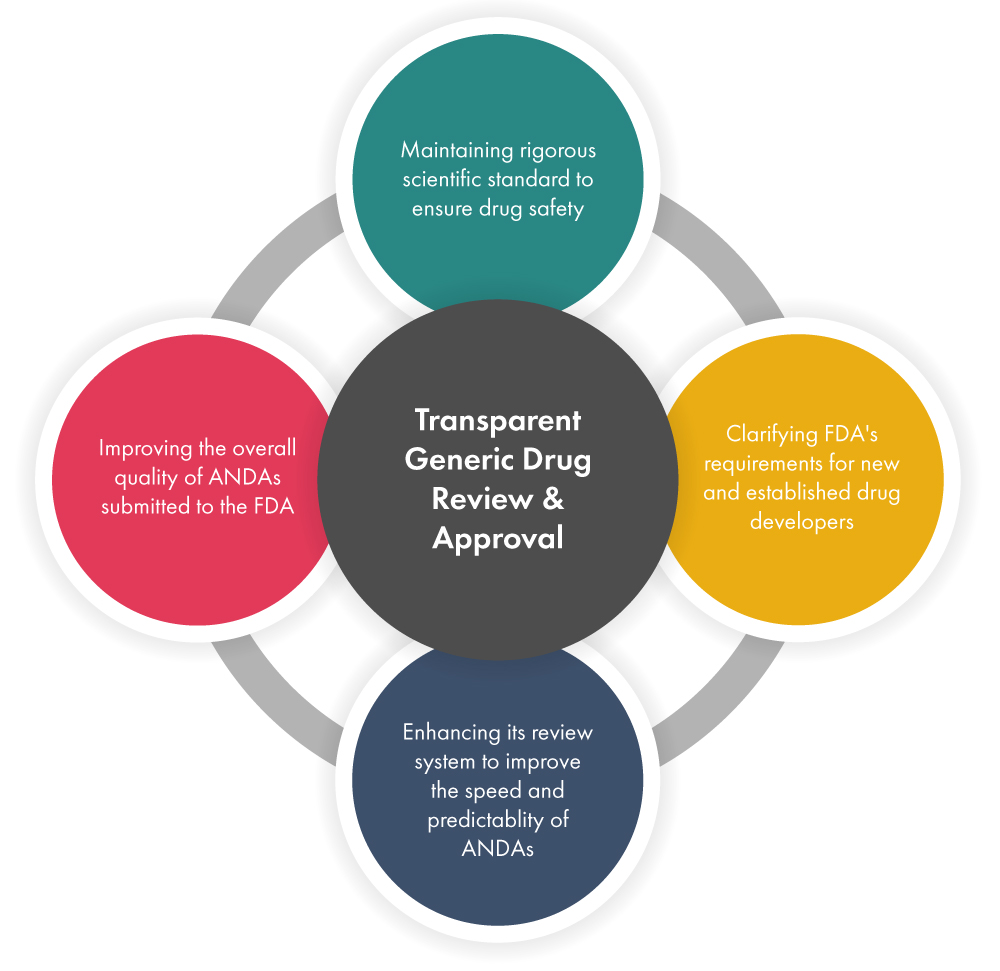
Erhöhung der wissenschaftlichen und regulatorischen Klarheit bei komplexen Generika – Es ist eine Tatsache, dass komplexe Generika im Vergleich zu einfachen Generika schwieriger zu entwickeln sind. Folglich ist der Wettbewerb für solche Medikamente wesentlich geringer. Da der DCAP vorschlägt, den Wettbewerb auf dem Generikamarkt zu erhöhen, hat die FDA mehrere Leitfäden für Generikahersteller herausgegeben. Einige davon sind unten aufgeführt.
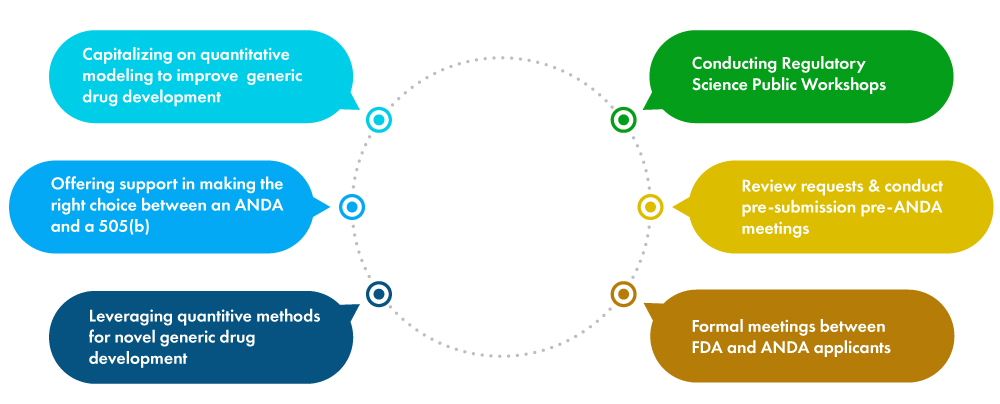
Schließung von Schlupflöchern, die es Innovator-Arzneimittelherstellern ermöglichen, den Generika-Wettbewerb zu verzögern, den der Kongress mit dem DCAP anstrebt - Diese Methode, die von Markenarzneimitteln angewendet wird, wird von der FDA auch als „Gaming“ bezeichnet. Sie verzögert den Genehmigungsprozess für Generika und reduziert folglich den Wettbewerb. Die Behörde zielt darauf ab, den Entwicklungs- und Genehmigungsprozess durch Vorhersehbarkeit und Transparenz zu optimieren.
Fazit
Das Hauptziel des DCAP ist die Verringerung der Monopolisierung von Markennamen bei der Entwicklung und Zulassung von Generika, indem ein effizienter Prozess geschaffen und gleichzeitig deren Qualität sichergestellt wird. Patienten müssen keine teuren Marken kaufen, da sie Zugang zu preisgünstigeren und wirksamen Generika haben, die auf dem Markt leicht erhältlich sind.
Die FDA veröffentlicht zu diesem Zweck neue Leitfäden für die Industrie, und Generikahersteller müssen diese kennen und befolgen, um schnellere Zulassungen zu gewährleisten. Ein bewährter regulatorischer Partner wie Freyr kann Ihnen helfen, mit den neuesten Vorschriften auf dem Laufenden zu bleiben. Konsultieren Sie Freyr für bewährte Compliance-Praktiken.









