
Das Informationssystem für klinische Prüfungen (CTIS) ist eine zentrale Datenbank, die die Durchführung klinischer Prüfungen in der Europäischen Union (EU) unterstützt. Es wurde im Januar 2022 eingeführt und ist ein wichtiger Bestandteil der Verordnung über klinische Prüfungen (CTR), die darauf abzielt, die Effizienz und Transparenz klinischer Prüfungen in der EU zu verbessern. Das CTIS verfügt über eine Reihe von Funktionen, die es zu einem wertvollen Werkzeug für Sponsoren klinischer Prüfungen, Forschende und Regulierungsbehörden machen.
Diese Merkmale umfassen:
- Eine zentrale Anlaufstelle für die Einreichung und Verwaltung klinischer Studien in mehreren Ländern.
- Eine sichere und effiziente Möglichkeit zum Informationsaustausch zwischen Sponsoren, Forschern und Aufsichtsbehörden.
- Eine durchsuchbare Datenbank klinischer Studien, die der Öffentlichkeit zugänglich ist.
- Tools zur Unterstützung der Überwachung und Aufsicht klinischer Studien.
- CTIS hat bereits einen positiven Einfluss auf die Landschaft klinischer Prüfungen in der EU. Es macht es einfacher und schneller, klinische Prüfungen durchzuführen, und gewährleistet, dass Daten aus klinischen Prüfungen transparenter und zugänglicher sind.
Entdecken Sie CTIS-Lösungen für Ihre klinischen Prüfungen
Optimieren Sie Ihre klinischen Studien jetzt
Wie CTIS die Landschaft klinischer Prüfungen verändert:
- CTIS erleichtert die Durchführung klinischer Prüfungen in mehreren Ländern:
Zuvor mussten Sponsoren für jedes Land, in dem sie eine klinische Studie durchführen wollten, separate Anträge einreichen. Dies war ein zeitaufwändiger und kostspieliger Prozess. CTIS ermöglicht es Sponsoren, einen einzigen Antrag einzureichen, der in allen EU Member States gültig ist. Dies hat die Durchführung klinischer Studien in mehreren Ländern für Sponsoren erheblich einfacher und schneller gemacht.
- CTIS verbessert die Effizienz des Prüfprozesses für klinische Studien:
Regulierungsbehörden in verschiedenen Ländern können nun über CTIS einfacher zusammenarbeiten. Dies bedeutet, dass Prüfungen nun schneller und effizienter durchgeführt werden können.
- CTIS macht Daten aus klinischen Studien transparenter:
Die öffentliche Website von CTIS bietet Zugang zu Informationen über alle im System registrierten klinischen Studien. Diese Informationen umfassen das Studienprotokoll, die Studienergebnisse und alle Sicherheitsbedenken. Diese erhöhte Transparenz trägt dazu bei, das Vertrauen der Öffentlichkeit in klinische Studien zu stärken.
CTIS ist ein wertvolles Instrument, das hilft, einige zentrale Herausforderungen bei klinischen Studien zu bewältigen. Indem CTIS die Durchführung klinischer Studien einfacher, schneller und transparenter macht, ermöglicht es, neue Behandlungen zügig zu den Patienten zu bringen.
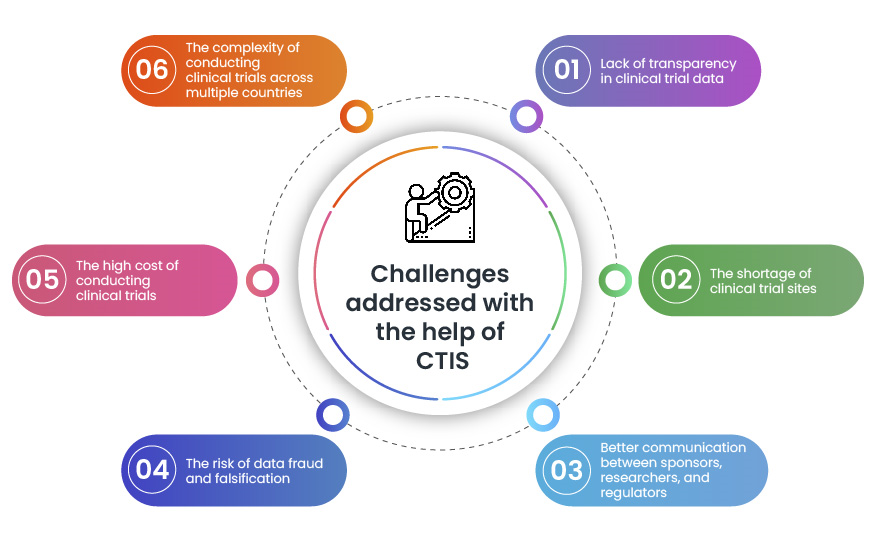
CTIS ist noch ein relativ neues System, hat aber das Potenzial, die Art und Weise, wie klinische Studien in der EU durchgeführt werden, zu revolutionieren. In einer Welt, in der wissenschaftliche Fortschritte wichtiger denn je sind, birgt CTIS, in Synergie mit einem globalen regulatorischen Partner wie Freyr, den Schlüssel zur Erschließung neuer Horizonte im Gesundheitswesen. Indem wir diese transformativen Technologien annehmen, ebnen wir den Weg für schnellere, sicherere und wirkungsvollere Entdeckungen, die das Potenzial haben, die Zukunft der Medizin für kommende Generationen zu gestalten.










