
Der malaysische Pharmamarkt entwickelt sich zu einem wachsenden Zentrum in Südostasien und bietet globale Unternehmen große Chancen. Angesichts der steigenden Nachfrage nach hochwertiger Gesundheitsversorgung und eines zunehmend strukturierten regulatorischen Rahmens wird der malaysische Pharmamarkt zu einem attraktiven Standort sowohl für Generika- als auch für Innovator-Hersteller.
Marktüberblick Malaysia: Vielversprechende Aussichten auf dem malaysischen Pharmamarkt
Sowohl Generika als auch neue chemische Wirkstoffe (NCEs) haben auf dem malaysischen Pharmamarkt, einer sich rasch entwickelnden Branche in Südostasien, gute Aussichten. Das Land bietet Pharmaunternehmen aufgrund seiner wachsenden Bevölkerung und des steigenden Bedarfs an Gesundheitsversorgung ein dynamisches Umfeld. Die Gesundheitsbranche ist ein lukrativer Markt für Arzneimittel, da sie gut etabliert ist und über erstklassige medizinische Einrichtungen verfügt.
Der malaysische Pharmamarkt ist durch eine steigende Nachfrage nach neuartigen Medikamenten gekennzeichnet, insbesondere in Therapiebereichen wie Diabetes, Herz-Kreislauf-Erkrankungen und Onkologie. Das regulatorische Umfeld ist besser strukturiert geworden und verfügt über präzise Vorschriften für die Produktzulassung und den Markteintritt, während sich die Regierung weiterhin auf die Verbesserung der öffentlichen Gesundheitsversorgung und des Zugangs zu Medikamenten konzentriert.
Anmeldeverfahren in Malaysia:
Das Verfahren zur Zulassung von Arzneimitteln in Malaysia wird von der National Pharmaceutical Regulatory Agency ( NPRA) geregelt, die für die Gewährleistung der Sicherheit, Wirksamkeit und Qualität von Arzneimitteln zuständig ist.
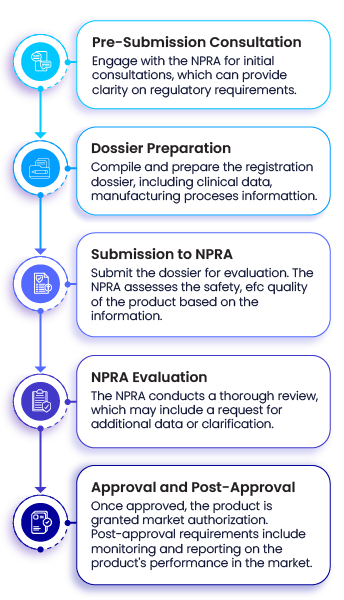
NPRA für die Zulassung von Arzneimitteln entsprechen den Leitlinien und Empfehlungen der Weltgesundheitsorganisation (WHO) zu Qualität, Sicherheit und Wirksamkeit sowie anderen international anerkannten Standards wie denen der Internationalen Konferenz zur Harmonisierung (ICH). Die wichtigsten Schritte des Zulassungsverfahrens sind folgende:
Grundlegende regulatorische Anforderungen:
Ein Arzneimittel muss mehrere wichtige behördliche Auflagen erfüllen, um in Malaysia zugelassen zu werden:
- Gute Herstellungspraxis (GMP): Um sicherzustellen, dass das Produkt den Qualitätsanforderungen entspricht, müssen die Produktionsstätten von den PIC/S akkreditiert sein.
- Klinische Daten: Um ihre Sicherheit und Wirksamkeit nachzuweisen, sind für neue Wirkstoffe Daten aus klinischen Studien erforderlich. Bei Generika muss die Bioäquivalenz nachgewiesen werden.
- Kennzeichnung und Verpackung: Bei der Kennzeichnung von Produkten müssen die örtlichen Vorschriften beachtet werden, insbesondere hinsichtlich der Sprache und der Sicherheitshinweise.
- Produktmonographie: Eine umfassende Beschreibung der Inhaltsstoffe, der Dosierung und der Anwendungshinweise des Produkts ist erforderlich.
- Lokale Vertretung: In der Regel muss ein lokaler Beauftragter oder Vertreter als Ansprechpartner NPRA fungieren. Der Antragsteller für die Produktregistrierung, der sogenannte „Product Registration Holder“ (PRH), muss ein vor Ort eingetragenes Unternehmen, eine Kapitalgesellschaft oder eine juristische Person mit festem Sitz sein, die bei der malaysischen Unternehmenskommission (SSM) registriert ist (mit einem Geschäftsfeld im Bereich Gesundheit/Arzneimittel).
Fallstudie von Freyr: Unterstützung eines in Taiwan ansässigen Pharmaunternehmens beim Markteintritt:
Kundenprofil: Ein führendes taiwanesisches Pharmaunternehmen beauftragte Freyr mit der end-to-end Unterstützung bei der Markteinführung von Generika und NCE auf dem malaysischen Pharmamarkt. Ziel war es, einen zeitnahen Markteintritt zu gewährleisten und gleichzeitig die komplexen regulatorischen Anforderungen zu bewältigen.
Projektdetails: Der Auftrag von Freyr umfasst das gesamte Spektrum an regulatorischen Dienstleistungen:
- Regulatorische Strategie und Vorgehensweise: Für die Produkteinführung in Malaysia wurde eine Strategie entwickelt, die NPRA entspricht und auf die Anforderungen des Kunden zugeschnitten ist.
- Technische Überprüfung und Lückenanalyse: Es wurde eine umfassende Prüfung der Zulassungsunterlagen durchgeführt, um etwaige Lücken aufzudecken und sicherzustellen, dass diese den Anforderungen NPRA entsprechen.
- Zusammenstellung und Einreichung: Es wurde sichergestellt, dass alle erforderlichen Unterlagen vollständig waren und den behördlichen Vorgaben entsprachen, bevor das Zulassungsdossier zusammengestellt und bei NPRA eingereicht wurde.
- Weiterverfolgung mit NPRA: Ich habe den laufenden Schriftverkehr mit NPRA betreut, NPRA etwaige Fragen oder weitere Anliegen zu klären und so das Genehmigungsverfahren zu beschleunigen.
Ergebnis: Mit Unterstützung von Freyr gelang es dem Kunden, das Zulassungsverfahren in Malaysia erfolgreich abzuschließen. Die Produkte wurden zügig genehmigt, was einen reibungslosen Markteintritt ermöglichte, technische Lücken schloss und sicherstellte, dass die richtigen Unterlagen eingereicht wurden. Dieser Fall unterstrich die Stärke von Freyr im Bereich Regulatory Affairs und seine Rolle bei der effektiven Navigation durch den malaysischen Pharmamarkt.
Dank end-to-end durch Freyr, die einen reibungslosen Ablauf des gesamten Zulassungsprozesses – von der Erstellung der Unterlagen bis zur endgültigen Genehmigung – sicherstellte, konnte sich der Kunde auf sein Kerngeschäft konzentrieren.
Sind Sie bereit, in Malaysias florierenden Pharmamarkt einzusteigen?
Der malaysische Pharmamarkt bietet ein immenses Wachstumspotenzial. Die Bewältigung der regulatorischen Rahmenbedingungen erfordert jedoch eine gut durchdachte Strategie, präzise Dokumentation und lokale Kenntnisse.
Durch die Zusammenarbeit mit erfahrenen Anbietern von Regulierungsdienstleistungen wie Freyr können Pharmaunternehmen ihren Markteintritt in Malaysia optimieren, technische Lücken schließen und schneller Zulassungen erhalten – und so neue Chancen in dieser dynamischen Region erschließen.










