Als die COVID-19-Pandemie im Jahr 2020 erstmals als globale Gesundheitskrise erkannt wurde, ergriffen die globalen Gesundheitsbehörden (HAs) innovative Schritte, um bestmöglich damit umzugehen. Ebenso entwickelten Pharmaunternehmen mehrere Impfstoffe/Arzneimittel zum Wohle der Öffentlichkeit. Die Registrierung der Produkte erwies sich jedoch als recht herausfordernd. Um die Registrierung zu vereinfachen und gleichzeitig deren Sicherheit, Qualität und Wirksamkeit zu gewährleisten, erteilten die HAs einigen Impfstoffen und relevanten Produkten Notfallzulassungen (EUAs).
Es stellt sich die Frage, wie die HAs sicherstellen konnten, dass die Vorteile der genannten Produkte die Risiken überwogen. Die Antwort ist die Anwendung der besten Pharmakovigilanz (PV)-Praktiken.
Was ist Pharmakovigilanz?
PV ist definiert als eine Reihe wissenschaftlicher Aktivitäten, die sich auf das Erkennen, Bewerten, Verstehen und Verhindern von unerwünschten Wirkungen und anderen arzneimittelbezogenen Problemen beziehen. Es folgt eine anschauliche Erklärung, wie PV funktioniert und welcher Prozess dahintersteckt.
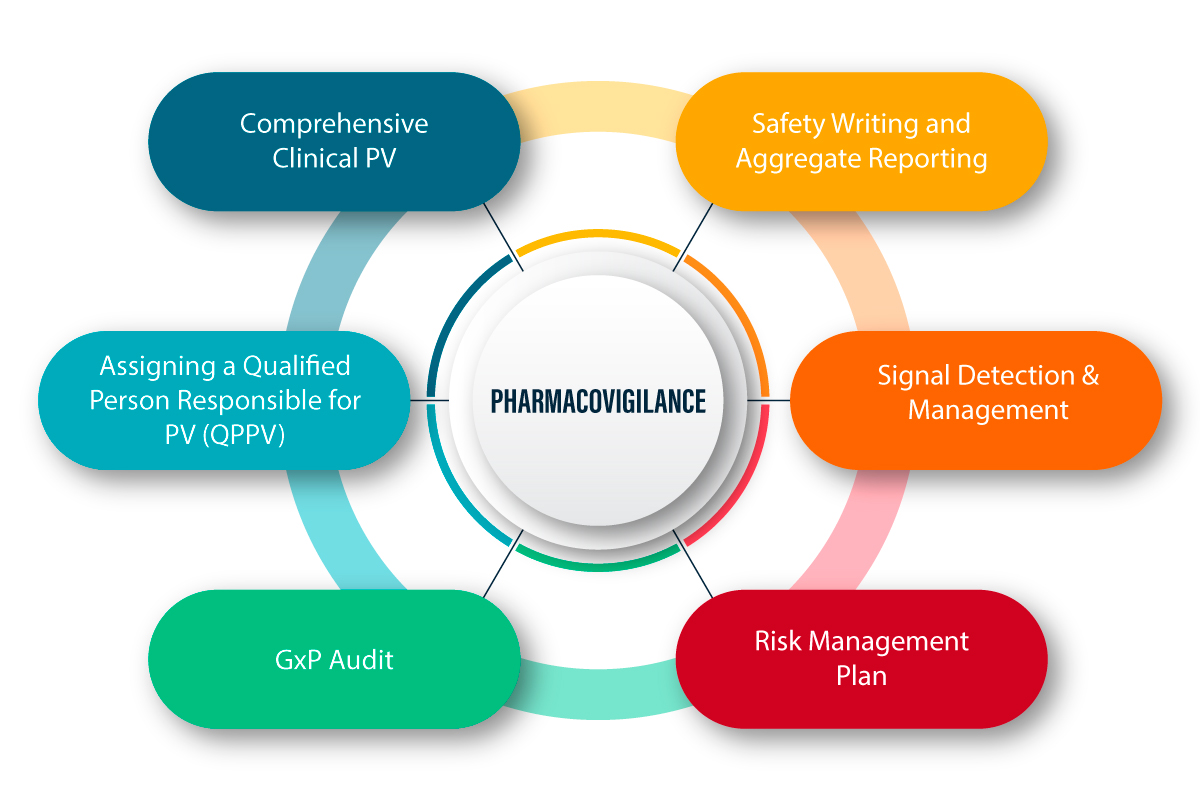
PV in der COVID-19-Pandemie
Als sich die COVID-19-Pandemie weltweit auszubreiten begann, mussten Impfstoffe und relevante Arzneimittel innerhalb eines begrenzten Zeitraums auf den Markt gebracht werden, wobei die erforderlichen Qualitätsstandards einzuhalten waren. In solchen Szenarien standen während der Entwicklungsphase von Arzneimitteln/Impfstoffen weniger Probanden für klinische Studien zur Verfügung, und der Prozess musste schneller als üblich abgeschlossen werden. Dies konnte dazu führen, dass bestimmte unerwünschte Wirkungen in der Phase nach der Zulassung auftraten.
Daher wurde das Nutzen-Risiko-Verhältnis von Impfstoffen/Arzneimitteln als überaus wichtig erachtet. Durch die rechtzeitige Kommunikation von unerwünschten Reaktionen und schädlichen Nebenwirkungen konnte die Wirksamkeit der Produkte in Echtzeit aufrechterhalten werden.
Einige der wichtigsten PV-Aktivitäten, die zur Aufrechterhaltung der Sicherheit, Qualität und Wirksamkeit der genannten Produkte während der Pandemie beigetragen haben, sind die folgenden:
- Anwendung eines guten Risikomanagementplans
- Risikobewertung mithilfe von Periodischen Sicherheitsberichten (PSURs)
- Sammlung der Expositionsdaten
- Post-Authorisation Safety Studies (PASS)
- Spontane Meldung vermuteter unerwünschter Wirkungen
- Effektives Signalmanagement
PV in Regulatory Affairs (RA)
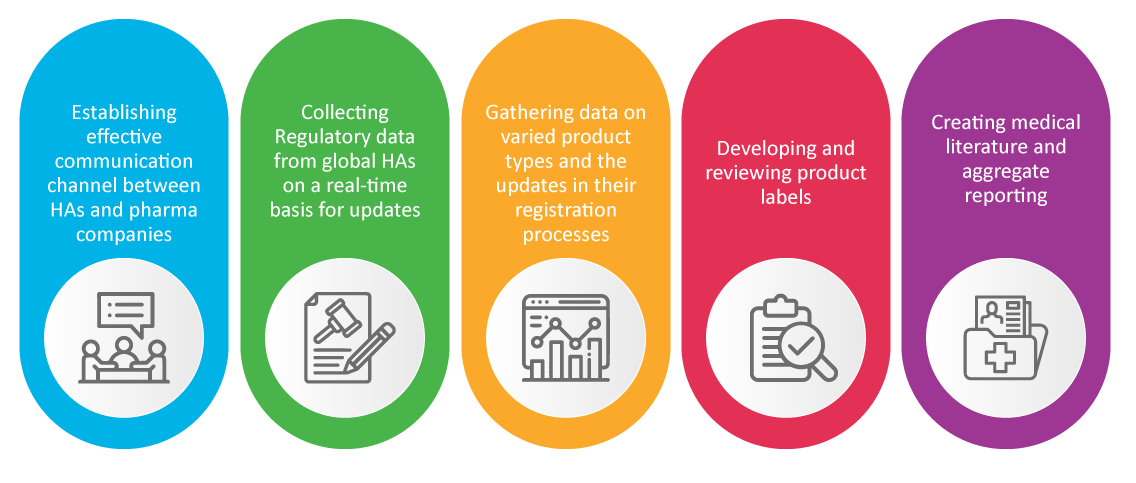
Es ist bekannt, dass das Regulatory Affairs Team eines Pharmaunternehmens für die Sicherheit und Zulassung neuer Produkte verantwortlich ist. RA-Spezialisten kümmern sich um Pharmakovigilanz-Aktivitäten, die sich während der Pandemie als entscheidend erwiesen haben, wie zum Beispiel:
Fazit
Zusammenfassend hilft die Pharmakovigilanz (PV) bei der Überwachung und Meldung der Sicherheit eines Arzneimittelprodukts. Mit maßgeschneiderten Berichten über einzelne Fallstudien (ICSR) wird es für Hersteller/Sponsoren einfacher, die jeweiligen Vorschriften globaler Gesundheitsbehörden (HAs) einzuhalten. Suchen Sie regulatorische Unterstützung für die Erstellung von ICSRs? Konsultieren Sie einen erfahrenen Regulierungsexperten für die Einhaltung der Vorschriften. Kontaktieren Sie Freyr.










