
Direkt an Verbraucher gerichtete (DTC) Arzneimittelwerbung ist in den letzten Jahren zu einem beliebten Diskussionsthema geworden. Diesen Werbeanzeigen, die sich an Verbraucher und nicht an medizinisches Fachpersonal richten, wird zugeschrieben, das Bewusstsein der Patienten und die Nachfrage nach bestimmten Medikamenten erhöht zu haben. Sie wurden jedoch auch dafür kritisiert, dass sie potenziell zu Überdiagnosen und Überbehandlungen führen können.
Im Zuge der aktuellen Trends in Pharmaunternehmen übersteigen die gesamten Marketingausgaben bekanntermaßen deren Forschungsbudgets. Weltweit wurden 1,42 Billionen US-Dollar für Marketing ausgegeben. In den USA wurden 2021 486,62 Milliarden US-Dollar für die Vermarktung von Arzneimitteln an Ärzte ausgegeben; in Kanada waren es 2022 29.305,1 Millionen US-Dollar. Bei der Aufschlüsselung dieser Zahlen entfielen 56 % auf kostenlose Muster, 25 % auf das „Detailing“ (direkte Bewerbung von Arzneimitteln) durch Pharmareferenten bei Ärzten, 12,5 % auf Direktwerbung an Nutzer, 4 % auf das Detailing in Krankenhäusern und 2 % auf Anzeigen in Fachzeitschriften2. Manchmal können negative Marketingpraktiken sowohl Patienten als auch das Gesundheitswesen beeinträchtigen.
Arten von Arzneimittel-Werbemaßnahmen
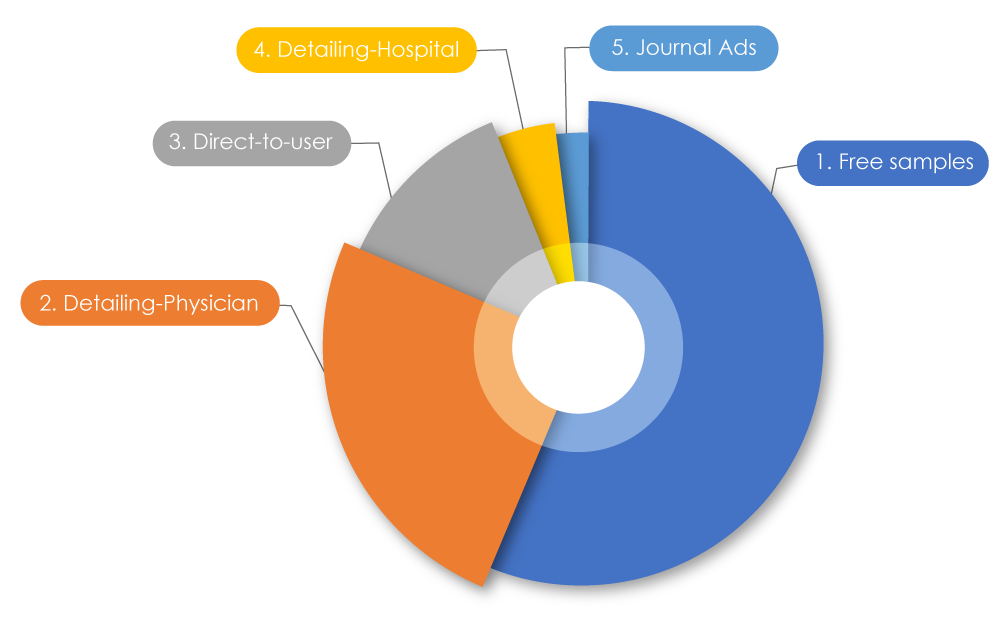
Quelle: Pharmazeutisches Marketing – Wikiwand
Pharmazeutische Werbung für die breite Öffentlichkeit
Für die Werbung für verschreibungspflichtige Medikamente in der breiten Öffentlichkeit, auch bekannt als Direkt-an-Verbraucher-Werbung (DTC-Werbung), gelten Beschränkungen. Um verschreibungspflichtige Medikamente in der Öffentlichkeit zu bewerben, muss die Kommunikation bestimmte grundlegende Anforderungen erfüllen:
- Die On-Label-Konformität von Werbung und Promotion für verschreibungspflichtige Arzneimittel hängt von der bestimmungsgemäßen Verwendung ab, für die das Produkt von der FDA zugelassen ist (der von der FDA zugelassenen Kennzeichnung des Arzneimittels). Die Kennzeichnung enthält Informationen zur sicheren und wirksamen Anwendung des Produkts für die zugelassene Indikation. Werbung und Promotion, die nicht mit der von der FDA zugelassenen Kennzeichnung übereinstimmen, gelten als ungesetzliche „Off-Label“-Promotionen.
- Die Bewerbung und Werbung für verschreibungspflichtige Medikamente erfordert ein ausgewogenes Verhältnis zwischen Produktnutzen und -risiken, wobei sicherzustellen ist, dass diese Informationen in Tiefe, Detail und Kontext vergleichbar dargestellt werden
- Aussagen sollten durch ausreichend aussagekräftige Nachweise oder klinische Erfahrung gestützt werden
- Wahrheitsgemäß und nicht irreführend – Wenn die Werbung und Bewerbung für verschreibungspflichtige Medikamente in irgendeiner Hinsicht falsch oder irreführend ist, wird sie gemäß dem Federal Food, Drug, and Cosmetic Act (FDCA) als falsch gekennzeichnet betrachtet und unterliegt der Durchsetzung.
- Verwendung einer verbraucherfreundlichen Sprache, Vermeidung von Fachsprache, wissenschaftlichen Begriffen und medizinischem Jargon in der an Verbraucher gerichteten Werbung und Bewerbung. Sie muss der genehmigten Kennzeichnung oder Monographie des Produkts entsprechen
Informationen in pharmazeutischer Werbung für die breite Öffentlichkeit
Verbrauchergerichtete Werbung und Promotion für verschreibungspflichtige Arzneimittel müssen die folgenden Kernelemente enthalten, wie es die Vorschriften des FDCA und der Food and Drug Administration (FDA) vorschreiben.
- Proprietäre und etablierte Namen sollten den FDA-Vorschriften entsprechen.
- Sie sollte die quantitative Menge der Inhaltsstoffe des beworbenen Medikaments enthalten
- Sie sollte eine „Kurzfassung“ enthalten, die jede Nebenwirkung, Warnung, Vorsichtsmaßnahme und Kontraindikation offenlegt. Dabei liegt der Schwerpunkt auf wichtigen Risikoinformationen und nicht auf einer vollständigen Liste produktbezogener Risiken. Die meisten Risiken werden so dargestellt, dass sie von Verbrauchern am ehesten verstanden werden
- Die wichtigsten Risiken des Produkts sollten klar, deutlich und neutral als „wichtige Aussage“ dargestellt werden
- Offenlegungserklärungen für die Meldung unerwünschter Ereignisse bei DTC-Werbung müssen die folgende MedWatch-Erklärung in auffälligem Text enthalten: „Sie werden ermutigt, negative Nebenwirkungen verschreibungspflichtiger Arzneimittel der FDA zu melden. Besuchen Sie www.fda.gov/medwatch oder rufen Sie +1–800-FDA-1088 an.“
- Erinnerungskennzeichnung und -werbung sind von den allgemeinen Anforderungen ausgenommen. Wichtig ist, dass Erinnerungskennzeichnung und -werbung für ein verschreibungspflichtiges Arzneimittel mit einem „Boxed Warning“ (Warnhinweis in einem Kasten) in seiner von der FDA zugelassenen Kennzeichnung nicht zulässig sind.
Für DTC-Arzneimittelwerbung, kontaktieren Sie uns.
Für die DTC-Arzneimittelwerbung
Beschränkungen für Interaktionen zwischen Patienten oder Patientenorganisationen und der Industrie
Interaktionen zwischen Pharmaunternehmen und Patienten/Patientenorganisationen sind nur in wenigen Ländern erlaubt, wie den US, jedoch mit Einschränkungen, wie zum Beispiel:
- Muss der Kennzeichnung/CFL entsprechen
- Ausgewogen
- Ausreichend belegt und
- Nicht anderweitig falsch oder irreführend
Darüber hinaus dürfen Interaktionen mit Kunden nicht gegen das Anti-Kickback-Gesetz verstoßen, indem Patientenorganisationen oder Patienten dazu verleitet werden, das beworbene Produkt zu empfehlen oder zu verwenden.
Im Vereinigten Königreich ist die DTC-Werbung für Pharmazeutika in der Öffentlichkeit erlaubt, schließt jedoch Kinder aus. Die Werbung für verschreibungspflichtige Medikamente in der Öffentlichkeit ist verboten. Werbeanzeigen sollten den Namen des Produkts und den Namen des Wirkstoffs enthalten. Produktmuster oder Gutscheine, die es Verbrauchern ermöglichen, das Produkt kostenlos oder zu einem unangemessen niedrigen Preis zu erhalten, sind nicht gestattet.
In Deutschland ist die Werbung an die Öffentlichkeit für Arzneimittel ausschließlich für Kinder unter 14 Jahren erlaubt. Die Werbung für verschreibungspflichtige Arzneimittel an die Öffentlichkeit ist verboten. Es gibt aber auch Sonderregeln für die Werbung für Arzneimittel außerhalb von Fachkreisen. Diese Sonderregeln sind hauptsächlich im Heilmittelwerbegesetz („HWG“) festgelegt und wurden durch das Arzneimittelgesetz („AMG“) geändert, um mit der Richtlinie 2001/83/EG4 in Einklang zu stehen.
Die Möglichkeit der Arzneimittelwerbung im digitalen Zeitalter diskutieren
Befürworter der DTC-Arzneimittelwerbung argumentieren, dass sie Patienten stärkt, indem sie ihnen Informationen über Behandlungsoptionen liefert. Sie weisen auch darauf hin, dass sie zu einer erhöhten Nachfrage nach Medikamenten führen kann, was für Pharmaunternehmen von Vorteil sein kann.
Andererseits argumentieren Kritiker der DTC-Arzneimittelwerbung, dass diese zu Überdiagnosen und Überbehandlungen führen kann. Sie behaupten, dass solche Werbeanzeigen oft die Vorteile von Medikamenten übertreiben und gleichzeitig deren Risiken herunterspielen. Dies veranlasst Patienten, ihre Ärzte nach Medikamenten zu fragen, die sie möglicherweise nicht benötigen. Zudem kann dies zu erhöhten Gesundheitskosten führen, da Patienten möglicherweise teurere Markenmedikamente anstelle von günstigeren Generika verschrieben bekommen.
Trotz der anhaltenden Debatte wird die DTC-Arzneimittelwerbung (Direct-to-Consumer) weiterhin bestehen bleiben. Die FDA hat Richtlinien für diese Art der Werbung herausgegeben, die Anforderungen an die Offenlegung von Risiken und ein ausgewogenes Verhältnis zwischen Nutzen und Risiken umfassen. Zusammenfassend lässt sich sagen, dass die DTC-Arzneimittelwerbung das Potenzial hat, Patienten aufzuklären und die Nachfrage nach bestimmten Medikamenten zu steigern. Es ist jedoch auch wichtig, die potenziellen Nachteile zu berücksichtigen und sich der Grenzen der in diesen Anzeigen bereitgestellten Informationen bewusst zu sein. Wie immer ist es wichtig, vor der Einnahme von Medikamenten Ihren Arzt zu konsultieren. Wenden Sie sich an die Freyr-Experten für End-to-End-Compliance!










