
In der stark regulierten Landschaft der Biowissenschaftsbranche ist die Einhaltung produktspezifischer Leitlinien (PSGs) für eine erfolgreiche Arzneimittelentwicklung und -zulassung von größter Bedeutung. PSGs sind umfassende Dokumente, die von globalen Gesundheitsbehörden (HAs) herausgegeben werden, um Leitlinien für die Zulassung pharmazeutischer Produkte innerhalb spezifischer therapeutischer Kategorien bereitzustellen.
Dieser Blog beleuchtet den Zweck, die Relevanz und die Perspektive der Gesundheitsbehörden (HAs) bei der Herausgabe von PSGs. Das Verständnis der in den PSGs dargelegten Gründe und Erwartungen, die den strategischen Erfolg von Biowissenschaftsunternehmen ermöglichen, wird in diesem Artikel ausführlich beschrieben.
Produktspezifische Leitlinien und ihre Arten verstehen
PSGs spielen eine zentrale Rolle bei der Gestaltung des regulatorischen Weges für pharmazeutische Produkte. Durch gezielte Leitlinien stellen die HAs die Konsistenz und robuste Bewertung von Produktanträgen innerhalb spezifischer therapeutischer Kategorien sicher. Durch die Einhaltung von PSGs können Pharmaunternehmen die komplexe regulatorische Landschaft erfolgreich meistern und sicherstellen, dass ihre Produkte die erforderlichen Sicherheits- und Wirksamkeitsstandards erfüllen.
PSGs sind nicht auf die Entwicklung generischer Arzneimittel beschränkt. Sie decken auch eine breite Palette pharmazeutischer Produkte ab, wie zum Beispiel die folgenden:
- Für innovative Arzneimittel: PSGs bieten spezifische Leitlinien zu präklinischen Studien, zum Design klinischer Studien, zur Sicherheitsbewertung, zur Pharmakokinetik und zu Wirksamkeitsendpunkten. Sie leiten Unternehmen an, welche Art und Menge an Daten erforderlich sind, um die Sicherheit und Wirksamkeit ihrer innovativen Arzneimittel nachzuweisen.
- Für Biosimilars: PSGs legen Datenanforderungen, Analysemethoden und Überlegungen zum Design klinischer Studien für Biosimilar-Produkte fest. Durch deren Befolgung können Biosimilar-Unternehmen die Ähnlichkeit ihrer Produkte mit dem Referenzbiologikum nachweisen und so den Weg für Zulassung und Marktzugang ebnen.
- Für Biologika: Diese Leitlinien behandeln kritische Aspekte wie Herstellung, Charakterisierung und Vergleichbarkeitsstudien, um sicherzustellen, dass die Biologika den genehmigten Standards entsprechen.
Entwicklung produktspezifischer Leitlinien und Prozesse
Die Entwicklung von PSGs ist eine gemeinschaftliche Anstrengung, an der HAs, wissenschaftliche Experten und Branchenakteure beteiligt sind. Die folgenden sind die Entwicklungsstufen der PSGs:
Phase 1 - Umfassende Bewertung des Therapiebereichs: HAs identifizieren Lücken in bestehenden Leitlinien und initiieren die Entwicklung von PSGs, um diese Lücken zu schließen. Wissenschaftliche Experten und Branchenakteure werden dann hinzugezogen, um ihr Fachwissen einzubringen und sicherzustellen, dass die Entwurfsleitlinien evidenzbasiert und praktisch umsetzbar sind.
Phase 2 - Öffentliche Konsultation: Entwürfe von PSGs stehen nun zur öffentlichen Überprüfung und Kommentierung zur Verfügung. Dieser offene und transparente Ansatz ermöglicht es Interessengruppen, einschließlich Angehörigen der Gesundheitsberufe (HCPs), Patientengruppen und Branchenvertretern, wertvollen Input zu geben und die Gesamtqualität und Relevanz der Leitlinien zu verbessern.
Phase 3: Interne Überprüfungsphase: Während sich die Entwürfe der PSGs in der öffentlichen Konsultation befinden, führt das PSG-Entwicklungsteam innerhalb der HAs eine rigorose interne Überprüfung durch, um sicherzustellen, dass die Leitlinien die notwendigen regulatorischen Anforderungen erfüllen und mit dem breiteren regulatorischen Rahmen übereinstimmen.
Phase 4 - Finalisierung: Nach der Finalisierung werden die PSGs veröffentlicht und der Branche zugänglich gemacht, wodurch klare und umsetzbare Leitlinien für die Produktentwicklung und -einreichung bereitgestellt werden.
Bestandteile von PSGs
Biowissenschaftsunternehmen müssen die Bestandteile der PSGs klar verstehen. Das folgende Tortendiagramm veranschaulicht sie im Detail:
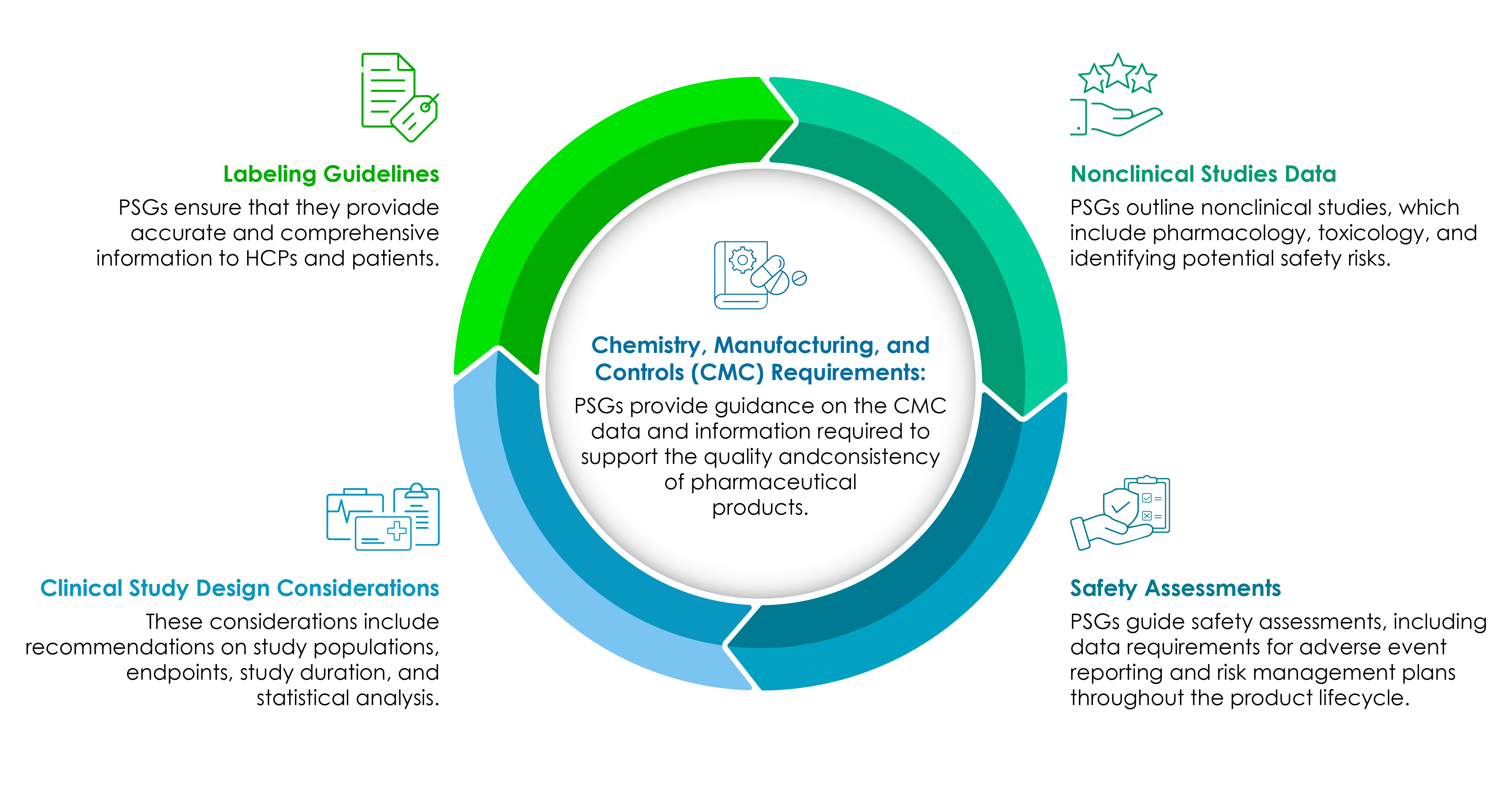
CMC bildet den Kern jeder auf regulatorische Aspekte ausgerichteten pharmazeutischen Produktentwicklung.
Umgang mit PSGs
Der regulatorisch konforme Umgang mit PSGs kann durch die folgenden aufgeführten Punkte/Strategien erreicht werden:
- Frühzeitige Zusammenarbeit mit den Gesundheitsbehörden: Eine solche Zusammenarbeit fördert einen kooperativen Ansatz und hilft, potenzielle Herausforderungen proaktiv anzugehen.
- Wissenschaftliche Expertise: Die Nutzung von Expertenwissen stellt sicher, dass Studiendesigns, Analysemethoden und Sicherheitsbewertungen den höchsten wissenschaftlichen Standards entsprechen.
- Regulierungsberater: Berater bieten fachkundige Beratung und stellen sicher, dass die Entwicklungspläne und regulatorischen Einreichungen erfolgreich sind.
- Umfassende PSG-Überprüfung: Unternehmen sollten spezifische PSG-Abschnitte identifizieren, die für ihr Produkt relevant sind, und ihre Entwicklungspläne entsprechend anpassen.
- Kontinuierliche Überwachung: PSGs sind dynamische Dokumente, die häufig aktualisiert oder überarbeitet werden können. Unternehmen müssen die Änderungen in den PSGs überwachen, um die Einhaltung der neuesten PSG-Anforderungen zu gewährleisten.
Fachkundige regulatorische Beratung erleichtert den Umgang mit PSGs. Jetzt beraten lassen!
Fazit
Produktspezifische Leitlinien (PSGs) bilden das Rückgrat regulatorischer Einreichungen für pharmazeutische Produkte innerhalb spezifischer therapeutischer Kategorien. Das Verständnis der Perspektiven der Gesundheitsbehörden (HA) hinter der Herausgabe von PSGs ist entscheidend für Life-Science-Unternehmen, die Genehmigungen beschleunigen, die Produktqualität sicherstellen und die globale Regulierungslandschaft nahtlos navigieren möchten.
Als führender Anbieter von regulatorischen Dienstleistungen erkennt Freyr die Bedeutung der Einhaltung bewährter Verfahren und der Nutzung von Fachwissen, das Unternehmen der Biowissenschaften dabei unterstützt, ihre Produktentwicklungsstrategien gemäß den PSG-Anforderungen auszurichten. Kontaktieren Sie uns noch heute, um mehr über unsere Dienstleistungen zu erfahren und wie wir Ihnen helfen können, Ihre Ziele zu erreichen.









