
Pharmazeutische Werbung, einschließlich der Direktwerbung an Verbraucher, wird von der US FDA (United States Food and Drug Administration) reguliert, genauer gesagt vom Office of Prescription Drug Promotion (OPDP) und dem Advertising and Promotional Labeling Branch (APLB) im Center for Drug Evaluation and Research (CDER) sowie vom Center for Biologics Evaluation and Research (CBER). Die an das OPDP und das APLB übermittelten Informationen müssen korrekt, ethisch und nicht irreführend sein. Zusätzliche Informationen zu den Vorteilen und Risiken des Produkts müssen in der Einreichung enthalten sein. Die Ämter prüfen auch die der Behörde vorgelegten Werbematerialien.
Im April 2022 veröffentlichte die US FDA eine Leitlinie zu den Einreichungen für Werbekennzeichnungen und Werbematerialien. Die Leitlinie hilft beim Verständnis der elektronischen Einreichung in Modul 1 des eCTD unter Verwendung der Version 3.3 oder höher der US-regionalen Backbone-Datei. Eine Erwähnung der Arten von Werbematerialien, die nicht der obligatorischen elektronischen Einreichung gemäß Abschnitt 745A unterliegen, ist im Dokument aufgeführt. Papierkopien aller Arten von Werbeeinreichungen werden bis vierundzwanzig (24) Monate nach Veröffentlichung der Leitlinie akzeptiert.
Ausnahme
Das Dokument besagt, dass die Einreichungen gemäß Abschnitt 505(b), (i) oder (j) des Federal Food, Drug, and Cosmetic Act (FD&C Act) und die Einreichungen gemäß Abschnitt 47 351(a) oder (k) des Public Health Service (PHS) Act in einem elektronischen Format eingereicht werden müssen, wie von der FDA definiert. Dieses Dokument unterliegt nicht den üblichen Beschränkungen der FDA-Vorschriften für gute Leitlinienpraxis, da es rechtlich keine durchsetzbaren Verantwortlichkeiten festlegt. Daher hat der Teil dieser Leitlinie, der die Anforderung für elektronische Einreichungen gemäß Abschnitt 745A(a) des FD&C Act festlegt, eine bindende Wirkung, wie durch die Verwendung der Wörter „muss“, „soll“ oder „erforderlich“ angezeigt wird.
Die FDA prüft das entworfene Werbematerial innerhalb von fünfundvierzig (45) Tagen nach der freiwilligen Einreichung durch die Sponsoren. Bei Fragen zum Produkt, die von medizinischem Fachpersonal, Verbrauchern, Arzneimittelherstellern oder Anwaltskanzleien aufgeworfen werden, gewährt die OPDP den Sponsoren, diese innerhalb von dreißig (30) Kalendertagen zu bestätigen.
Definition von Werbematerial
Der Ausdruck „Werbematerial“ bezieht sich auf Werbekennzeichnungen und Werbematerialien, unabhängig vom Format, der Art oder dem Medium, über das sie kommuniziert werden. Die FDA überwacht im Allgemeinen zwei (02) Arten der Kennzeichnung für Arzneimittel:
- Von der FDA vorgeschriebene Kennzeichnung
- Werbekennzeichnung
Gemäß Abschnitt 201(m) der FDA wird Kennzeichnung definiert als „alle Etiketten neben schriftlichen, gedruckten oder grafischen Prägungen auf Behältern, Verpackungen oder auf oder begleitend zu einem Artikel.“ Die Formulierung „begleitend zu einem Artikel“ wird als Interpretation oder Erklärung des Werbematerials angesehen, wie vom Obersten Gerichtshof der US festgestellt.
Kriterien für die Einreichung von Werbematerial zur Prüfung
- Angabe geeigneter NDA-, ANDA- oder BLA-Nummern
- In Fällen, in denen die Antragsteller eine sofortige Prüfung benötigen, sind die Einreichungen an den OPDP-Projektmanager zu richten
- Aus dem Formular FDA 2253 weisen Sie die spezifischste Materialart zu, um das Werbematerial darzustellen.
- Verschiedene Arten von Materialien sind separat einzureichen
- Andere Einreichungen dürfen nicht mit Werbematerial gemischt werden
- Werbematerial, das sich an medizinisches Fachpersonal richtet, muss getrennt von dem eingereicht werden, das sich an Verbraucher richtet
Die untenstehenden Kennzahlen verdeutlichen die Anzahl der eingereichten Formulare 2253 und die Materialien, die in diesen Einreichungen enthalten sind.
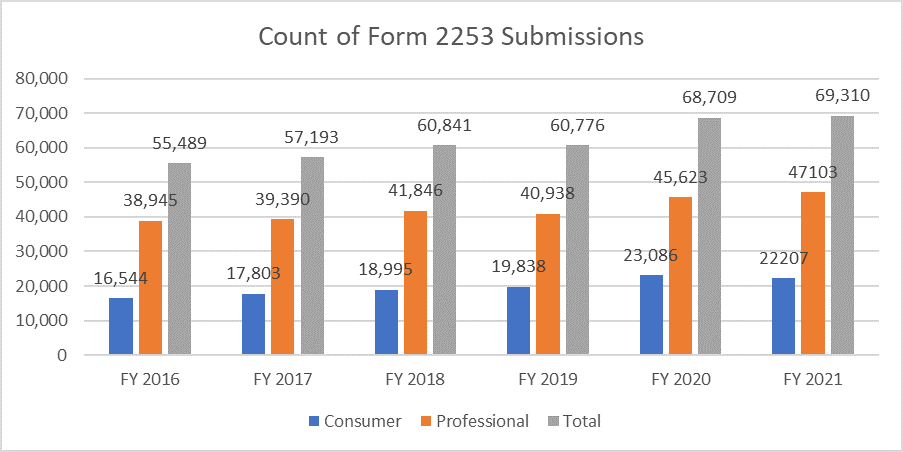
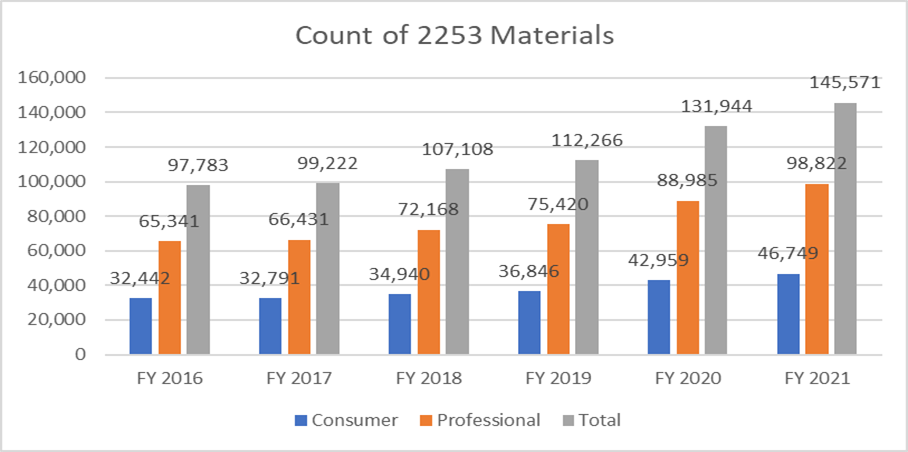
Es ist von größter Bedeutung, dass die Sponsoren ihr Werbematerial gemäß den von der FDA bereitgestellten Leitlinien entwerfen, um angesichts der Kosten des Prozesses mehrfache Prüfzyklen zu vermeiden. Ressourcen, die den Prozess der nahtlosen Einreichung von Werbematerial erleichtern können, ermöglichen es den Sponsoren, ihre Geschäftsziele zu erreichen und die regulatorischen Anforderungen zu erfüllen. Ein bewährter regulatorischer Partner wie Freyr kann eine vollständige Überprüfung von Werbe- und Nicht-Werbematerial vor der Einreichung gewährleisten, sei es in elektronischem oder nicht-elektronischem Format. Kontaktieren Sie Freyr noch heute, um klares, prägnantes und konformes Werbematerial gleich beim ersten Mal zu erstellen.










