
Kombinationsprodukte, die Arzneimittel, Medizinprodukte und/oder biologische Produkte integrieren, haben das Gesundheitswesen durch innovative therapeutische Lösungen revolutioniert. Ihre einzigartige Beschaffenheit stellt jedoch erhebliche regulatorische Herausforderungen dar. Dieser umfassende Leitfaden beleuchtet die komplexe Landschaft der Regulierung von Kombinationsprodukten und bietet Strategien, um diese komplexen Wege erfolgreich zu meistern.
Kombinationsprodukte und ihr regulatorischer Rahmen
Kombinationsprodukte sind Medizinprodukte, die zwei (2) oder mehr regulierte Komponenten – Arzneimittel, Medizinprodukte oder Biologika – zu einer einzigen Einheit vereinen. Diese innovativen Produkte können verschiedene Formen annehmen, wie z. B. medikamentenfreisetzende Stents, vorgefüllte Spritzen oder transdermale Pflaster. Der Regulierungsrahmen für Kombinationsprodukte wird hauptsächlich von der US Food and Drug Administration (FDA) in den US geregelt, wobei ähnliche Ansätze von Regulierungsbehörden weltweit übernommen werden.
Das Office of Combination Products (OCP) der FDA spielt eine entscheidende Rolle bei der Bestimmung des primären Wirkmechanismus (PMOA) eines Kombinationsprodukts, der den Regulierungspfad und das federführende FDA-Zentrum für die Prüfung festlegt. Das Center for Drug Evaluation and Research (CDER), das Center for Devices and Radiological Health (CDRH) und das Center for Biologics Evaluation and Research (CBER) arbeiten im Prüfprozess zusammen und betonen die Notwendigkeit eines integrierten Ansatzes, um die Sicherheit und Wirksamkeit von Kombinationsprodukten zu gewährleisten.
Bestimmung des regulatorischen Weges
Einer der wichtigsten Schritte bei der Entwicklung einer regulatorischen Strategie für Kombinationsprodukte ist die Bestimmung des geeigneten regulatorischen Weges. Diese Entscheidung basiert hauptsächlich auf dem PMOA des Produkts. Hier sind wichtige Überlegungen:
- Primärer Wirkmechanismus (PMOA): Identifizieren Sie den einzelnen Wirkmechanismus, der die wichtigste therapeutische Wirkung des Kombinationsprodukts darstellt.
- Zuweisung des federführenden Zentrums: Basierend auf dem PMOA wird das Produkt CDER, CDRH oder CBER zur primären Prüfung zugewiesen.
- Art der regulatorischen Einreichung: Je nach federführendem Zentrum kann die Einreichung in Form eines New Drug Application (NDA), Biologics License Application (BLA) oder Premarket Approval (PMA) erfolgen.
- Antrag auf Einstufung (RFD): Wenn der PMOA unklar ist, können Sponsoren einen RFD an das OCP zur formellen Bestimmung einreichen.
- Vorab-Antrag auf Einstufung (Pre-RFD): Das OCP kann einen Pre-RFD für informelles, unverbindliches Feedback zu Klassifizierungs- und Zuständigkeitsfragen erhalten.
Das Verständnis dieser Faktoren ist entscheidend für die Entwicklung einer effektiven regulatorischen Strategie, die auf Ihr spezifisches Kombinationsprodukt zugeschnitten ist.
Meistern der Prüfprozesse vor der Markteinführung
Der Prüfprozess vor der Markteinführung für Kombinationsprodukte kann komplex sein und erfordert sorgfältige Planung und Durchführung. Hier sind wichtige Strategien, um diesen Prozess effektiv zu meistern:
- Frühzeitige Zusammenarbeit mit Regulierungsbehörden: Nehmen Sie frühzeitig im Entwicklungsprozess durch Pre-Submission-Meetings Kontakt mit der FDA auf. Diese Interaktionen können wertvolle Hinweise zu regulatorischen Anforderungen, Studiendesigns und potenziellen Herausforderungen geben.
- Umfassender Entwicklungsplan: Entwickeln Sie einen soliden Plan, der die einzigartigen Aspekte Ihres Kombinationsprodukts berücksichtigt, einschließlich der Wechselwirkungen der einzelnen Bestandteile und ihrer kombinierten Auswirkungen auf Sicherheit und Wirksamkeit.
- Integrierter Testansatz: Konzipieren Sie präklinische und klinische Studien, die die einzelnen Komponenten und das gesamte Kombinationsprodukt bewerten. Dieser Ansatz sollte potenzielle Wechselwirkungen und kumulative Effekte bewerten.
- Überlegungen zum Qualitätssystem: Implementieren Sie ein Qualitätssystem, das den Vorschriften für Arzneimittel (21 CFR 210/211) und Medizinprodukte (21 CFR 820) entspricht, je nachdem, was für Ihr Produkt zutreffend ist.
- Berücksichtigung menschlicher Faktoren: Führen Sie Studien zu menschlichen Faktoren durch, um die Benutzerinteraktionen mit dem Kombinationsprodukt zu bewerten und so eine sichere und effektive Anwendung zu gewährleisten.
- Risikomanagement: Entwickeln Sie einen umfassenden Risikomanagementplan, der potenzielle Risiken berücksichtigt, die mit jeder Komponente und deren Kombination verbunden sind.
Durch die Anwendung dieser Strategien können Sponsoren den Prüfprozess vor der Markteinführung optimieren und die Wahrscheinlichkeit eines regulatorischen Erfolgs erhöhen.
Bewältigung der Herausforderungen nach der Markteinführung
Die regulatorischen Verantwortlichkeiten für Kombinationsprodukte reichen über die Marktzulassung hinaus. Eine effektive Überwachung nach dem Inverkehrbringen (Post-Market Surveillance) und die Einhaltung der Vorschriften sind entscheidend für den langfristigen Erfolg. Berücksichtigen Sie die folgenden Strategien:
- Integrierte Pharmakovigilanz: Implementieren Sie ein robustes Pharmakovigilanzsystem, das unerwünschte Ereignisse im Zusammenhang mit den Arzneimittel- und Medizinproduktekomponenten des Kombinationsprodukts erfasst.
- Studien nach der Markteinführung: Planen und führen Sie Studien nach der Markteinführung durch, um zusätzliche Sicherheits- und Wirksamkeitsdaten zu sammeln, insbesondere für neuartige Kombinationsprodukte.
- Pflege des Qualitätssystems: Aktualisieren und pflegen Sie Ihr Qualitätssystem kontinuierlich, um die Einhaltung relevanter Vorschriften für Arzneimittel- und Medizinproduktekomponenten zu gewährleisten.
- Änderungsmanagement: Etablieren Sie einen unkomplizierten Prozess für die Verwaltung von Änderungen nach der Zulassung, unter Berücksichtigung der potenziellen Auswirkungen auf die Arzneimittel- und Medizinprodukteaspekte des Produkts.
- Regulatorische Intelligenz: Bleiben Sie über sich entwickelnde Vorschriften und Leitliniendokumente bezüglich Kombinationsprodukten informiert, um die fortlaufende Einhaltung zu gewährleisten.
Indem Hersteller diese Herausforderungen nach der Markteinführung proaktiv angehen, können sie die Einhaltung regulatorischer Vorschriften und die Produktsicherheit während des gesamten Produktlebenszyklus aufrechterhalten.
Globale regulatorische Überlegungen
Da der Markt für Kombinationsprodukte weltweit wächst, wird das Verständnis internationaler regulatorischer Anforderungen immer wichtiger. Berücksichtigen Sie diese Strategien für einen globalen regulatorischen Erfolg:
- Regulatorische Harmonisierung: Nutzen Sie internationale Harmonisierungsbemühungen, wie die des International Medical Device Regulators Forum (IMDRF), um globale regulatorische Einreichungen zu optimieren.
- Marktspezifische Anforderungen: Recherchieren und verstehen Sie spezifische Anforderungen für Kombinationsprodukte in Zielmärkten, da die Vorschriften zwischen den Ländern erheblich variieren.
- Gleichzeitige Einreichungen: Erwägen Sie gleichzeitige Einreichungen bei mehreren Zulassungsbehörden, um den globalen Marktzugang gegebenenfalls zu beschleunigen.
- Globale klinische Studien: Gestalten Sie klinische Studien, die die Anforderungen mehrerer Zulassungsbehörden erfüllen, um globale Marketinganträge zu unterstützen.
- Internationale Partnerschaften: Arbeiten Sie mit lokalen regulatorischen Experten oder Partnern in Zielmärkten zusammen, um länderspezifische Vorschriften und kulturelle Besonderheiten zu berücksichtigen.
Durch die Übernahme einer globalen Perspektive bei der Entwicklung von Regulierungsstrategien können Hersteller ihre Marktreichweite für Kombinationsprodukte effektiver erweitern.
Fazit
Das Navigieren durch die regulatorischen Wege für Kombinationsprodukte erfordert ein umfassendes Verständnis komplexer regulatorischer Rahmenbedingungen und strategischer Planung.
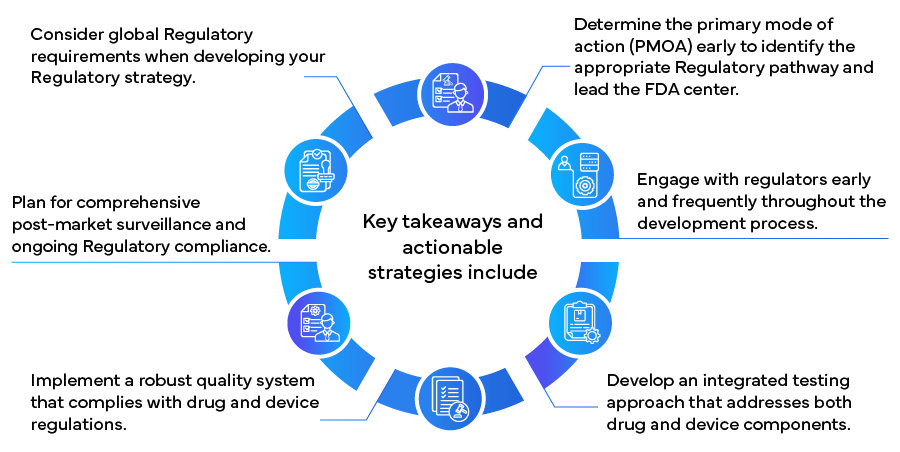
Durch die Umsetzung dieser Strategien können Hersteller die komplexe regulatorische Landschaft für Kombinationsprodukte effektiver navigieren, potenziell die Markteinführungszeit beschleunigen und langfristige Compliance und Erfolg sicherstellen. Da sich der Bereich der Kombinationsprodukte ständig weiterentwickelt, wird es entscheidend sein, über regulatorische Änderungen informiert zu bleiben und Flexibilität in den regulatorischen Ansätzen zu bewahren, um den anhaltenden Erfolg in diesem innovativen und schnell wachsenden Gesundheitssektor zu sichern.









