Während innovative oder Markenarzneimittel zusätzliche Kosten für die Forschung und Entwicklung des Produkts von der Molekülidentifizierung bis zur Marktzulassung verursachen, sind Generika relativ kostengünstig. Diese Therapien senken nicht nur die Gesamtkosten der Behandlung, sondern verbessern auch erheblich den Patientenzugang zu lebensrettenden Arzneimitteln. Da die Abhängigkeit vom Import generischer Antibiotika und Therapien für seltene Krankheiten die weltweite Verfügbarkeit dieser Arzneimittel während der Pandemie beeinträchtigte, führen Gesundheitsbehörden neue Leitlinien ein, um lokale Arzneimittelhersteller zu unterstützen.
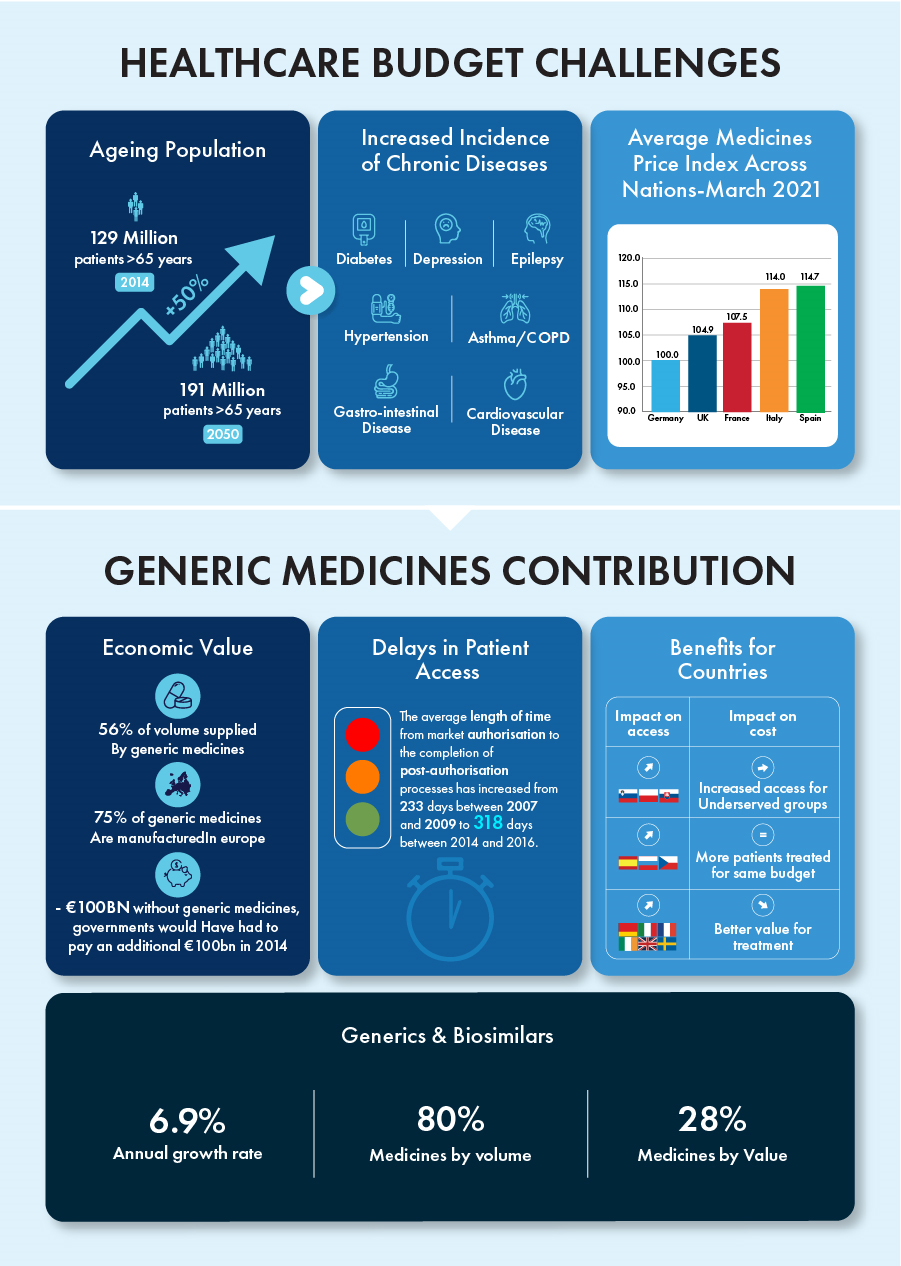
Seit 1993 verfolgt die Handelsorganisation Medicines for Europe, ehemals European Generics Medicine Association (EGA), konsequent ihr Ziel, der europäischen Patientenbevölkerung kostengünstige Therapien zugänglich zu machen. In den letzten zehn Jahren haben sie erfolgreich 67 % aller Arzneimittel nach Europa geliefert und den Patientenzugang in sieben (07) wichtigen Therapiebereichen auf 100 % erhöht. Im Zuständigkeitsbereich der europäischen Gesundheitsbehörden setzte eine „strategische Autonomie“ nach dem Brexit eine sofortige Notwendigkeit in Gang, den Wettbewerbsnachteil, dem europäische Generika- und Biosimilar-Hersteller ausgesetzt sind, wirksam zu beheben. Mit dem Aufkommen der COVID-19-Pandemie brachen die globalen Lieferketten unter dem Druck der Arzneimittelnachfrage zusammen. Lebensrettende Medikamente, die Linderung bei chronischen Krankheiten verschafften, verschwanden aus den Regalen der örtlichen Apotheken. Um Hindernisse bei patentgeschützten Arzneimitteln zu überwinden und die lokale Arzneimittelherstellung zur Verbesserung des Patientenzugangs aufzubauen, hat der EU-Rat eine Verordnung erlassen, die eine Ausnahme für ein Originalmolekül durch die Bereitstellung eines ergänzenden Schutzzertifikats (SPC) vorsieht. Diese Bestimmung erleichtert die Herstellung von Generika und Biosimilars vor Ablauf des Patents zu Lager- oder Exportzwecken. Die Ausnahme ist jedoch nur unter den folgenden Umständen anwendbar.
- Die hergestellten Generika oder Biosimilars sind ausschließlich für den Export in ein anderes Land bestimmt, in dem das Patent für das Arzneimittelmolekül nicht existiert oder abgelaufen ist, oder für Lagerzwecke innerhalb der verbleibenden Patentlaufzeit von sechs (06) Monaten.
- Gemäß der Anforderung hat der Hersteller die Informationen vor Ablauf von drei (03) Monaten an die lokale Gesundheitsbehörde und den Inhaber des SPC übermittelt.
- Der Hersteller hat alle an der Vermarktung des Produkts beteiligten Interessengruppen informiert.
- Der Hersteller hat sichergestellt, dass die Kennzeichnungsvorschriften besagen, dass das Arzneimittelprodukt nur für Exportzwecke bestimmt ist.
Wissenswertes
Seit der Erteilung der bedingten Marktzulassung für COVID-19-Impfstoffe in der EU hat der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur innerhalb eines Jahres vier (04) Standorte für die Impfstoffproduktion zugelassen; zwei (02) in der Schweiz und zwei (02) in den USA. Solche Entscheidungen zugunsten der Erweiterung von Produktionsstandorten werden die Impfstoffherstellungskapazitäten verbessern und die Impfstoffe für die europäische Bevölkerung zugänglicher machen.
Generika und Biosimilars haben maßgeblich zu einer jährlichen Wachstumsrate von 6,9 % beigetragen und machten im letzten Jahrzehnt 80 % des Volumens und 28 % des Wertes aller Arzneimittel aus. Die Patentschutzfrist für bestimmte Biologika im Wert von rund 90 Milliarden Euro läuft bis 2023 aus, was ein wettbewerbsintensives Umfeld für diese Produkte mit enormem Wachstumspotenzial schafft.
Die Einführung eines SPC-Waivers würde der Europäischen Union zugutekommen, indem:
- Jährlich zusätzlich etwa 90,5 Milliarden Euro hinzukommen.
- Schaffung von fünfundzwanzigtausend (25.000) neuen Arbeitsplätzen, davon zweitausend (2.000) direkte Arbeitsplätze für die EU-API-Industrie. Die Initiative wird den EU Member States helfen, 3,1 Mrd. € bei den Gesundheitsausgaben einzusparen.
- Die Bevorratung günstigerer Alternativen zu patentierten Originalarzneimitteln, um deren Markteintritt unmittelbar nach Ablauf des geistigen Eigentums (IP) zu ermöglichen und so den Patientenzugang zu verbessern.
Für einen Arzneimittelhersteller mit Sitz in der Europäischen Union ist die Umsetzung des SPC-Verzichts eine der vorteilhaftesten Initiativen zugunsten von Generika. Da die EU-Gesundheitsbehörde Arzneimittel für den menschlichen und tierärztlichen Gebrauch über ein zentralisiertes oder dezentralisiertes Verfahren reguliert, kann es sehr komplex sein, sich in den spezifischen lokalen Anforderungen zurechtzufinden. Ein Experte, der die lokalen Anforderungen für verschiedene Einreichungen und Lizenzdokumente kennt, kann Ihnen helfen, sich auf wesentliche Produktionsprotokolle zu konzentrieren, anstatt sich mit komplexen regulatorischen Hürden aufzuhalten. Entdecken Sie Ihr Geschäftspotenzial neu, indem Sie Compliance und Qualität erleben. Kontaktieren Sie Freyr.









