
Die meisten Unternehmen der Biowissenschaften finden es schwierig, ihren Prozess für regulatorische Einreichungen zu optimieren, da sich die Einreichungsrichtlinien häufig ändern. Einer aktuellen Analyse der USFDA (United States Food and Drug Administration) zufolge wiesen 32 % der Einreichungen mit Studiendaten kritische Probleme bei der Datenkonformität auf. Der Prozess erfordert ein umfassendes Verständnis der Zusammenarbeit zwischen internen und externen Akteuren. Innerhalb der Organisation müssen die Abteilungen Fertigung, Forschung und Entwicklung, klinische/nicht-klinische Forschung, QA/QC, Marketing und Vertrieb harmonisch zusammenarbeiten, um den Genehmigungsprozess von der ersten Entwicklung bis zur Markteinführung des Medikaments zu beschleunigen. Die Abteilung Regulatory Affairs und die Gesundheitsbehörden (HAs) stehen in ständigem Austausch, um die Sicherheit und Wirksamkeit von Arzneimitteln für den menschlichen Gebrauch zu gewährleisten und zu bewerten. Lassen Sie uns sehen, welche vorbereitenden Maßnahmen pharmazeutische Organisationen ergreifen müssen, um Exzellenz bei regulatorischen Einreichungen zu erreichen:
Ressourcen zuweisen und einsetzen, um unorganisierte Einreichungsarbeiten zu optimieren, zu standardisieren und zu beschleunigen
Ein Einreichungsspezialist arbeitet auf Vertragsbasis und kann mehr als eine (01) Art von Einreichung verstehen, während er über Jahre hinweg mit Entwicklungsprogrammen verbunden ist und dabei hilft, überzeugende Darstellungen für das Dossier zu erstellen. Dies erleichtert es Organisationen,:
- Fehler vermeiden, indem die Zusammenarbeit interner und externer Stakeholder ausgewogen gestaltet wird
- Den Prüfzyklus der Gesundheitsbehörde für den Prozess der Dokumentenerstellung und -genehmigung verkürzen.
- Vollständige und konforme Einreichungen erstellen, um den sich ändernden regulatorischen Anforderungen verschiedener Märkte gerecht zu werden.
- Die von einer Regulierungsbehörde betroffenen Einreichungen bestätigen.
- Den Status der Erstellung, Prüfung und Genehmigung von Einreichungen kennen.
- Verbesserung des aktuellen Einreichungsprotokolls.
Die Methodik für Dossier-Einreichungen vereinfachen.
Die Erstellung eines Dossiers ist bei der Vorbereitung von Einreichungen entscheidend. Es wird festgestellt, dass Biologics License Applications (BLAs) und New Drug Applications (NDAs) unzählige Seiten umfassen, was es für Regulierungsbehörden schwierig macht, die Darstellung des Dossiers zu verstehen. Eine strukturierte Darstellung einer allgemeinen Idee kann die Fähigkeit des Teams, Einreichungen vorzubereiten, und die der prüfenden Behörden erheblich verbessern.
Der Einsatz von Modulen zur Straffung von Einreichungen ermöglicht es den Experten, zu analysieren, was in jedem Abschnitt oder Modul des Dossiers enthalten sein soll. Eine solche Vorgehensweise erleichtert:
- Früher Beginn der Erstellung durch Beschleunigung der Einreichungsvorbereitung der Organisation.
- Verwendung relevanter Daten, die für die Erstellung der Einreichungen erforderlich sind.
- Einsatz geeigneter Ressourcen, ohne die Notwendigkeit, für jede Einreichung umfangreiche Dokumente von Grund auf neu zu erstellen.
In Zusammenarbeit mit den Regulierungsbehörden arbeiten.
Jede Organisation sollte in der frühen Phase der Produktentwicklung routinemäßig regelmäßige Treffen mit den Gesundheitsbehörden (HAs) abhalten. Dies gewährleistet eine zeitnahe Prüfung und Rückmeldung, was zu einer beschleunigten Klärung der Kommentare durch die HA führt und folglich den Genehmigungsprozess beschleunigt. Es baut nicht nur eine gute Beziehung zwischen den Organisationen und der HA auf, sondern hilft auch, frühzeitig Klarheit bei der Einreichungsplanung zu gewinnen.
Inhalte und Daten im Dokumentenmanagementsystem (DMS) optimieren.
Ein robustes Content-Repository soll alle Daten über verschiedene Funktionsbereiche hinweg verwalten, einschließlich der zuvor erstellten Dokumentation und Informationen. Strukturierte Inhalte und Daten-Repositories ermöglichen einen nahtlosen Zugriff auf Dokumente aus verschiedenen Funktionsbereichen ohne zusätzlichen Aufwand oder die Notwendigkeit von Duplikaten. Im DMS gespeicherte Dokumente werden zur einzigen Kontaktquelle für alle internen Akteure (klinische Wissenschaft, CMC, nicht-klinische Studien, Pharmakokinetik, Pharmakodynamik, medizinisches Schreiben und klinische Operationen). Solche Inhalte und Daten können genutzt werden, um lokale Inhalte basierend auf regionalen Anforderungen zu erstellen. Optimierung regulatorischer Einreichungen durch strukturiertes Content- und Datenmanagement
Einsatz von Technologie und Automatisierung zur Reduzierung von Wiederholungsarbeiten und Fehlern.
Organisationen können Technologie nutzen, indem sie die Funktion zur automatischen Aktualisierung und Qualitätskontrolle von Tabellen, Auflistungen und Abbildungen (TLF) im Text anhand der Quelldaten verwenden, um den Dokumentationsprozess zu beschleunigen. Auf diese Weise wird bei Änderungen an den vorhandenen Quelltabellen eine entsprechende Aktualisierung in den TLF im Text vorgenommen. Dies hilft, den gesamten Arbeitsaufwand zu reduzieren, Zeit im kritischen Pfad zu sparen und die Datengenauigkeit zu verbessern.
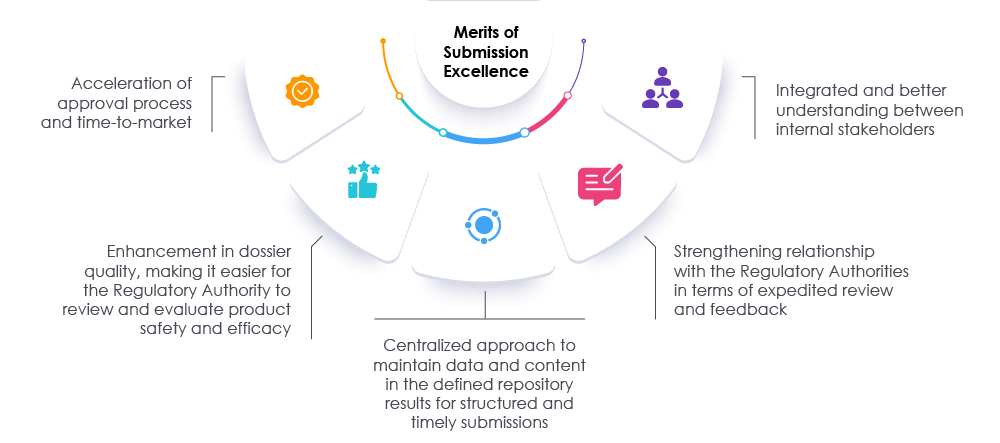
Geeignete Maßnahmen sowie zeitnahe Überprüfungen der Dossiers und Daten können sowohl Regulierungsbehörden als auch Organisationen dabei helfen, den Einreichungsprozess zu beschleunigen. Dieser Ansatz verkürzt die Markteinführungszeit, um sowohl den Bedürfnissen der Patienten als auch der Industrie gerecht zu werden. Ein bewährter regulatorischer Partner kann Organisationen dabei unterstützen, die aktuellen Ansätze zur Vorbereitung von Einreichungen zu überdenken, neu zu bewerten und anzupassen. Unsere Experten bei Freyr können den Weg zur Exzellenz bei regulatorischen Einreichungen ebnen, indem sie die Transparenz innerhalb der Organisation erhöhen und die allgemeine Compliance fördern, wodurch die Organisation auf dem heutigen Markt der Biowissenschaften erfolgreich sein kann. Freyr kontaktieren.










