
Notfallzulassungen (EUAs) sind entscheidend, um lebensrettende Arzneimittel schneller für Patienten verfügbar zu machen. Sie haben sich bei der Bewältigung von Pandemien wie COVID-19 als hilfreich erwiesen. Eine Initiative der USFDA (United States Food and Drug Administration) begann im Jahr 2004, und die EUA trat in Kraft, als Abschnitt 564 des Federal Food, Drug, and Cosmetic Act durch den Project BioShield Act geändert wurde. Dieses Programm ist ein Schritt der FDA zum Schutz der öffentlichen Gesundheit, indem es die Sicherheit, Wirksamkeit und Qualität von Medizinprodukten gewährleistet und gleichzeitig medizinische Notfälle und aufkommende Bedrohungen der öffentlichen Gesundheit angeht.
Lassen Sie es uns in den folgenden Zeilen besser verstehen.
Die EUA entschlüsseln
Das EUA-Verfahren ist ein Mittel, um den Zugang zu medizinischen Gegenmaßnahmen in Zeiten erklärter Notfälle zu erleichtern. Der Kommissar der FDA kann in solchen Situationen Folgendes genehmigen:
- Die genehmigte Verwendung nicht zugelassener Medizinprodukte.
- Die nicht genehmigte Verwendung zugelassener Medizinprodukte.
Die unter die EUA fallenden Produkte umfassen Impfstoffe, Infusionslösungen, Arzneimittel, Medizinprodukte, Tests usw. und können zur Diagnose, Behandlung oder Vorbeugung lebensbedrohlicher Erkrankungen eingesetzt werden. Produkte erhalten eine EUA, wenn die folgenden Kriterien erfüllt sind:
- Nachweis einer lebensbedrohlichen Erkrankung.
- Die wissenschaftlichen Daten liefern ausreichende Beweise dafür, dass das Produkt für seinen vorgesehenen Verwendungszweck wirksam ist.
- Der Nutzen des Produkts überwiegt die Risiken (d.h. Nachweis der Sicherheit).
- Fehlen alternativer Produkte.
Sponsoren wird empfohlen, die Anforderungen der FDA im Voraus zu verstehen, um den besten regulatorischen Prozess zu befolgen und eine fehlerfreie EUA-Einreichung sicherzustellen. Folgende Informationen sind zwingend erforderlich, die vom Sponsor im Antrag mitgeteilt werden müssen.
Vom Sponsor bei der FDA für eine EUA-Zulassung einzureichende Daten
- Produktbeschreibung und sein vorgesehener Verwendungszweck.
- Der Zulassungsstatus des Produkts bei der FDA.
- Informationen zu Sicherheit und Wirksamkeit, wie z.B. klinische und nicht-klinische Daten usw.
- Nutzen-Risiko-Analysebericht.
- Daten zu Chemie, Herstellung und Kontrolle (CMC).
- Informationen zur Dosierung, Gegenanzeigen, Warnhinweisen und unerwünschten Ereignissen für den Vertrieb des betreffenden Medizinprodukts.
Wie werden Notfallzulassungen von der US FDA erteilt?
Nachfolgend finden Sie eine kurze schematische Darstellung des EUA-Lebenszyklus:
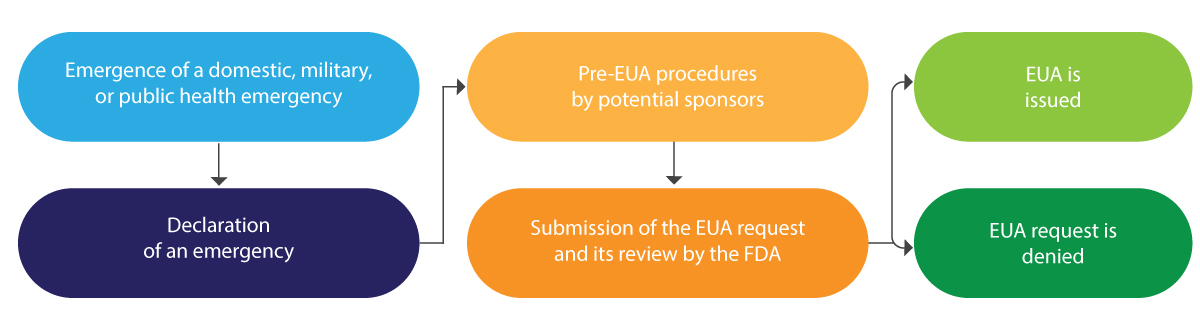
Die EUA wird typischerweise für einen begrenzten Zeitraum ausgestellt, und am Ende des genannten Notfalls wird sie von der FDA beendet.
EUA und COVID-19
Der Gesundheitsminister (HHS) erklärte COVID-19 am 31. Januar 2020 zur Pandemie. Seitdem war die FDA maßgeblich an der Genehmigung einiger Impfstoffe und Heimtestkits im Rahmen des EUA-Verfahrens beteiligt, um den anhaltenden globalen Ausbruch zu bewältigen.
Mit dem Auftauchen neuer Varianten von COVID-19 arbeitet die gesamte Pharmaindustrie hart daran, die Ausbreitung einzudämmen und die Sterblichkeitsraten zu senken. Es besteht ein Bedarf an neuartigen Arzneimitteln und schnelleren Zulassungen durch globale Regulierungsbehörden, damit ihre Markteinführungszeit verkürzt wird. Der EUA-Weg zur Registrierung neuer Arzneimittel/Medikamente ist laut Experten der richtige Weg. Mehrere andere Gesundheitsbehörden wie die European Medicines Agency (EMA), die Central Drugs Standard Control Organization (CDSCO), die Saudi Food and Drug Authority (SFDA) usw. haben ebenfalls den EUA-Weg für schnellere Zulassungen implementiert.
Wenn Sie ein Arzneimittelhersteller sind und eine EUA für Ihr lebensrettendes Produkt suchen, benötigen Sie einen erfahrenen Anbieter von regulatorischen Lösungen. Kontaktieren Sie Freyr für eine schnellere Markteinführung und einen konformen Weg.










