
Das Medical Device Single Audit Program (MDSAP) ermöglicht einer anerkannten Auditorganisation (AO), ein einziges Audit des Qualitätsmanagementsystems (QMS) eines Medizinprodukteherstellers durchzuführen. Es liefert relevante regulatorische Anforderungen für fünf Länder, d.h. Brasilien (ANVISA), die USA (FDA), Japan (PMDA), Kanada (Health Canada) und Australien (TGA). Neben den teilnehmenden Regulierungsbehörden sind mehrere andere internationale Partner (die offiziellen Beobachter und assoziierten Mitglieder) am MDSAP beteiligt.
Die MDSAP-Zertifizierung ist von Health Canada für Produkte der Klassen II, III und IV vorgeschrieben, ist aber für die anderen vier Länder freiwillig. Sie hat die Transparenz und die regulatorische Abstimmung zwischen den teilnehmenden Behörden gefördert und den Bedarf an mehreren Audits minimiert, wodurch Zeit und Ressourcen der Medizinproduktehersteller gespart werden. Um Ihnen eine bessere Perspektive auf das MDSAP-Programm zu geben, haben wir hier versucht, die fünfzehn (15) am häufigsten gestellten Fragen zu beantworten.
- Warum wurde das MDSAP-Programm entwickelt, obwohl eine weltweit anerkannte ISO 13485-Zertifizierung existiert?
MDSAP wurde entwickelt, um den Aufwand für regulatorische Audits bei Medizinprodukteherstellern zu reduzieren und eine stärkere Angleichung der regulatorischen Ansätze und technischen Anforderungen auf der Grundlage internationaler Standards und bewährter Verfahren zu fördern. Es konzentriert sich darauf, Konsistenz, Vorhersehbarkeit und Transparenz in regulatorische Programme zu bringen, indem Verfahren und Praktiken von Regulierungsbehörden und externen Auditorganisationen standardisiert werden.
Das Audit basiert auf den QMS-Anforderungen gemäß ISO 13485 und den regulatorischen Anforderungen des teilnehmenden Landes, in dem die Medizinprodukte vermarktet werden sollen.
- Was sind die Zulassungskriterien für die Durchführung eines MDSAP-Audits?
Jeder Medizinproduktehersteller, der beabsichtigt, sein Produkt in den teilnehmenden Ländern zu vermarkten, kann ein MDSAP-Audit durchlaufen. Jede Regulierungsbehörde kann jedoch bei Bedarf Ausschlusskriterien für bestimmte Bedingungen festlegen.
Zum Beispiel gelten in Japan folgende Ausnahmen für die Berechtigung:
- Eine registrierte Produktionsstätte (RMS), die Medizinprodukte aus menschlichem/tierischem Gewebe herstellt
- Eine RMS, die radioaktive IVDs herstellt, und
- Gründung eines Inhabers der Genehmigung für das Inverkehrbringen (MAH)
- Umfasst das MDSAP-Audit Kombinationsprodukte?
Medizinprodukte, die Arzneimittel (medizinische Substanzen) oder Biologika (z. B. Materialien tierischen Ursprungs, die nicht mehr lebensfähig gemacht wurden, oder Gewebe, Zellen oder Substanzen mikrobiellen oder rekombinanten Ursprungs, menschliches Blut oder Extrakte aus menschlichem Blut oder Blutprodukte usw.) enthalten, gelten als Kombinationsprodukte und können in den Geltungsbereich eines MDSAP-Audits einbezogen werden.
Aufgrund von Unterschieden in der Regulierung dieser Produkte in den Zuständigkeitsbereichen der teilnehmenden Regulierungsbehörden können MDSAP-Auditberichte und Zertifizierungsdokumente jedoch in einigen Jurisdiktionen nicht als Alternative zu den Inspektions- und Bewertungsanforderungen angesehen werden.
Australien- Kombinationsprodukte unterliegen einer externen Prüfung durch die TGA im Rahmen der australischen Konformitätsbewertung. Ein effektives MDSAP-Audit kann jedoch die Inspektionen für diese Produkte reduzieren.
Brasilien, Japan- Kombinationsprodukte, die als Medizinprodukte gelten, sind im MDSAP enthalten, da es keine spezifischen Anforderungen an das QMS gibt.
Kanada- Das MDSAP-Modell deckt die QMS-Anforderungen für Kombinationsprodukte ab, die als Medizinprodukte gelten.
USA- MDSAP-Audits gelten nicht als Alternativen zu FDA-Inspektionen für Kombinationsprodukte.
- Kann ich das Land für das MDSAP-Audit auswählen?
Ja, das Audit wird gemäß dem im Antrag auf Zertifizierungsdienstleistungen deklarierten Umfang durchgeführt. Von Medizinprodukteherstellern wird erwartet, dass sie die Vorschriften nur in den Rechtsgebieten einhalten, in denen ihre Produkte vermarktet werden sollen.
- Ich bin ein Medizinproduktehersteller aus den US, der beabsichtigt, mein Produkt nur in Japan zu vermarkten. Ich stehe kurz vor einem MDSAP-Audit. Muss ich auch die Anforderungen anderer Länder erfüllen?
Nein, Hersteller von Medizinprodukten müssen nur die ISO 13485-Anforderungen und -Vorschriften in den Rechtsgebieten einhalten, in denen ihre Produkte vermarktet werden sollen.
- Meine Auditierende Organisation (AO) und die Europäische Benannte Stelle sind dieselben. Kann ich für beide gleichzeitig auditiert werden?
Wenn Ihre AO und Ihre europäische Benannte Stelle identisch sind, kann die Konformitätsbewertung nach Durchführung des MDSAP-Audits erfolgen, nicht gleichzeitig. Europäische Benannte Stellen sind Beobachter für MDSAP, und die Konformitätsbewertung wird gemäß der EU MDR 2017/745 durchgeführt. Für MDSAP erfolgt die Bewertung gemäß den Anforderungen der ISO 13485 und den regulatorischen Anforderungen der beteiligten Länder im Geltungsbereich.
- Was ist der Unterschied zwischen Bewertungen der Stufe I und II?
Der anfängliche MDSAP-Auditprozess umfasst zwei Phasen. Das anfängliche Audit, auch Erstzertifizierungsaudit genannt, besteht aus Phase-I- und Phase-II-Audits.
Ein Audit der Stufe I umfasst die Dokumentenprüfung und die Bewertung der Bereitschaft des Medizinprodukteherstellers, sich einem Audit der Stufe II zu unterziehen.
Das Phase-II-Audit wird durchgeführt, um zu überprüfen, ob alle anwendbaren Anforderungen der ISO 13485 und andere regulatorische Anforderungen der zuständigen Regulierungsbehörde umgesetzt wurden.
- Wie viele Auditoren können Sie für ein MDSAP-Audit erwarten?
Die Bestimmung der Auditzeit legt fest, wie die Dauer des Vor-Ort-Audits in Personentagen zu bestimmen ist. Die AO entscheidet, wie viele Auditoren das Audit-Team bilden werden. Zum Beispiel kann ein (06) Personentage-Audit von einem Team aus zwei (02) Auditoren in drei (03) Tagen abgeschlossen werden.
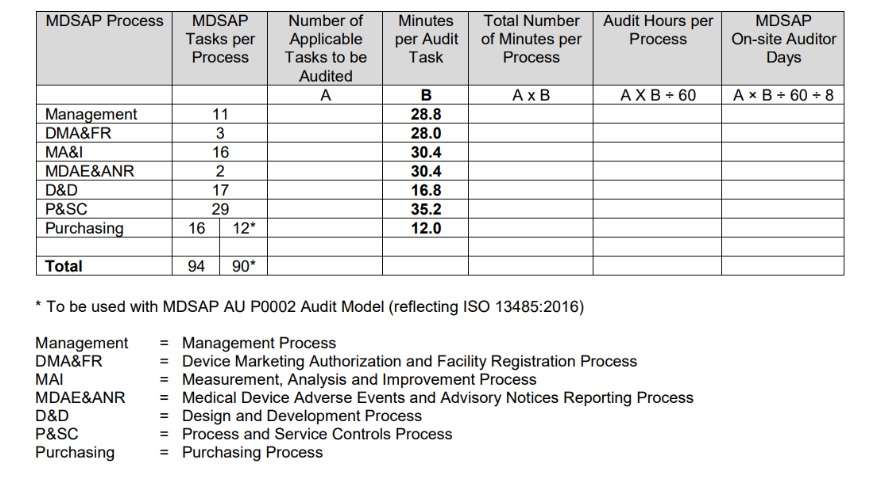
- Wie ist der Zeitplan für das MDSAP-Audit?
Das von der FDA herausgegebene Verfahren zur Bestimmung der Auditdauer fasst den Prozess zur Berechnung der Auditdauer in der folgenden Tabelle zusammen.
Die Berechnung der Auditdauer basiert hauptsächlich auf der Anzahl der relevanten Auditaufgaben, die mit der Art des durchzuführenden Audits und den spezifischen zu auditierenden Aktivitäten der Organisation verbunden sind.
Weitere Informationen dazu finden Sie unter MDSAP P0008007
- Gibt es einen Leitfaden oder eine Checkliste, auf die Sie zugreifen können, um die Einhaltung der Vorschriften bei einem MDSAP-Audit sicherzustellen?
Ja, Sie können auf das Dokument MDSAP Audit Approach zugreifen. Es handelt sich um einen gut strukturierten Leitfaden, der von der USFDA herausgegeben wurde und spezifische Abschnitte der ISO 13485:2016 sowie relevante Vorschriften der australischen TGA, der brasilianischen ANVISA, von Health Canada (Kanada), des japanischen MHLW/PMDA und der US FDA miteinander vergleicht.
- Welche Rolle spielt ein Beobachter bei einem MDSAP-Audit?
Ein MDSAP-Beobachter ist eine Regulierungsbehörde, die an Besprechungen, Bewertungen und anderen Aktivitäten teilnehmen darf, aber die MDSAP-Ergebnisse nicht nutzt. Die Beobachter sind im MDSAP Regulatory Authority Council (RAC) durch einen leitenden Manager vertreten.
- Was sind die nächsten Schritte, wenn ich eine Bewertung von 4 oder höher erhalten habe?
Das Bewertungssystem wird für Nichtkonformitäten vergeben, die während des Audits durch die AO festgestellt wurden. Eine Bewertung von 4 oder 5 weist auf ein hohes Interventionsrisiko hin. Sie müssen für jede festgestellte Nichtkonformität innerhalb von 15 Kalendertagen nach dem Datum der Ausstellung des Nichtkonformitätsberichts einen Sanierungsplan vorlegen. Der Sanierungsplan muss die Ergebnisse der Untersuchung der Nichtkonformität, deren Ursachen und geplante Korrekturmaßnahmen zur Verhinderung eines erneuten Auftretens enthalten. Der Nachweis der Umsetzung des Sanierungsplans/der Maßnahme sollte innerhalb von dreißig (30) Kalendertagen nach dem Enddatum des Audits erbracht werden.
- Gibt es einen Unterschied im Vorgehen beim Audit durch einen internen Auditor im Vergleich zur Benannten Stelle (AO)?
MDSAP verfolgt einen prozessorientierten Ansatz. Die AO wird wahrscheinlich Verknüpfungen und Zusammenhänge betrachten, während ein interner Auditor sich eher auf einen funktionalen Aspekt gleichzeitig konzentrieren könnte. Daher könnte die AO eine Nichtkonformität in einem Funktionsbereich feststellen und Antworten in einem anderen Funktionsbereich suchen. Die Anwendung des prozessorientierten Ansatzes könnte jedoch bei einem internen Audit störend sein.
- Kann ich bei der AO Einspruch erheben, wenn ich beweisen kann, dass eine festgestellte Nichtkonformität nicht gültig ist?
Die AO verfügt über ein Berufungs- oder Streitbeilegungsverfahren, das Sie nutzen können, wenn Sie nachweisen können, dass eine festgestellte Nichtkonformität ungültig ist. Die für Nichtkonformitäten vergebenen Bewertungen können jedoch nicht aufgrund von Korrekturmaßnahmen geändert werden. Sie können nur auf der Grundlage von Nachweisen geändert werden, die belegen, dass sie nicht gültig waren.
- Wie lange ist das MDSAP-Zertifikat gültig?
Medizinproduktehersteller, die unter dem MDSAP-Programm zertifiziert sind, werden jährlich gemäß einem dreijährigen Zertifizierungszyklus auditiert. Das Erstaudit ist ein vollständiges Audit des QMS des Medizinprodukteherstellers. Es folgen Überwachungsaudits, die jährlich für zwei (02) aufeinanderfolgende Jahre durchgeführt werden. Der Zyklus beginnt im dritten Jahr mit einem Rezertifizierungsaudit von Neuem.
Um mehr über unsere MDSAP-Dienstleistungen zu erfahren, kontaktieren Sie Freyr noch heute, um einen Termin für ein Gespräch mit unseren Experten zu vereinbaren.









