Überblick und Definition
Fusionen und Übernahmen (M&A) in der Medizinproduktebranche sind mit komplexen regulatorischen Herausforderungen in verschiedenen Rechtsräumen verbunden. Die Integration zweier Unternehmen erfordert die Harmonisierung der Qualitätsmanagementsysteme (QMS), die Abwicklung behördlicher Einreichungen sowie die Abstimmung klinischer und nachmarktbezogener Prozesse.
Die auf Medizinprodukte spezialisierten Dienstleistungen von Freyr in den Bereichen Fusionen und Übernahmen sowie regulatorische Angelegenheiten bieten end-to-end , damit Ihr Unternehmen diese Herausforderungen nahtlos meistern kann, und gewährleisten die kontinuierliche Einhaltung der ISO 13485, der MDR, FDA und anderer globaler Standards.
Compliance-Prozess bei Fusionen und Übernahmen im Bereich Medizinprodukte
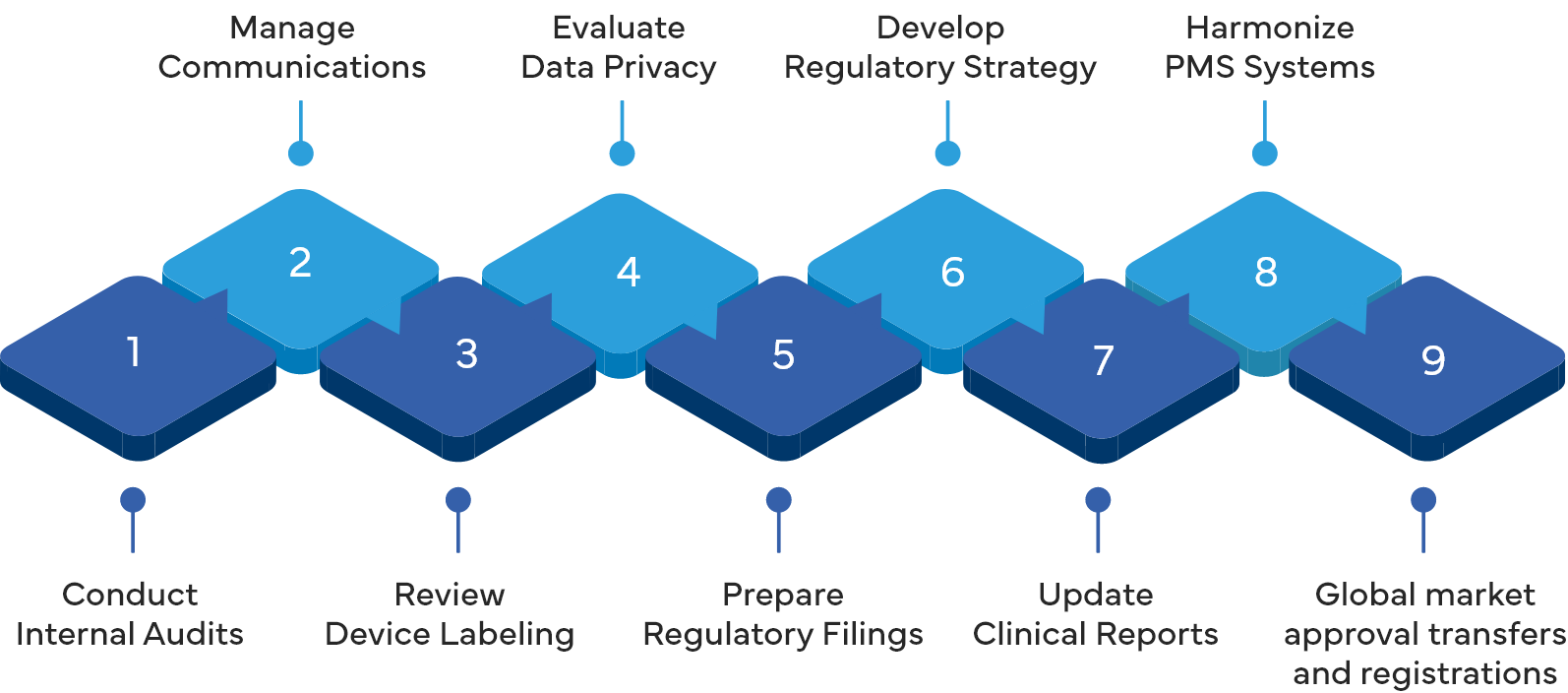
Freyrs Dienstleistungen
PMS-Integration
- Zusammenführung der PMS-Systeme beider Unternehmen.
- Harmonisierung der Prozesse zur Meldung unerwünschter Ereignisse und zur Trendanalyse.
REGULATORISCHE DUE-DILIGENCE-PRÜFUNG
- Umfassende Bewertung der Einhaltung gesetzlicher Vorschriften durch das Zielunternehmen, einschließlich des Qualitätsmanagementsystems, der Produktzulassungen, der klinischen Daten und der Kennzeichnung.
- Ermittlung potenzieller regulatorischer Risiken und Haftungsrisiken.
- Lückenanalyse und Sanierungsplanung.
REGULIERUNGSSTRATEGIE UND -PLANUNG
- Entwicklung einer umfassenden Zulassungsstrategie zur Integration der Produktportfolios beider Unternehmen.
- Planung der Übertragung und Aktualisierung von behördlichen Registrierungen und Lizenzen in allen relevanten Märkten.
- Erstellung eines Zeitplans für regulatorische Maßnahmen.
Integration von QMS und CAPA
- Harmonisierung der Qualitätsmanagementsysteme beider Unternehmen, um die Einhaltung der Norm ISO 13485 anderer einschlägiger Normen sicherzustellen.
- Entwicklung und Einführung eines einheitlichen Dokumentationssystems für das Qualitätsmanagementsystem.
- Durchführung interner Audits und Lückenanalysen.
- Behördliche Einreichungen und Registrierungen:
- Erstellung und Einreichung aller erforderlichen behördlichen Unterlagen für die Übertragung und Aktualisierung von Produktzulassungen.
- Kommunikation mit den Aufsichtsbehörden
INTEGRATION VON DATENSCHUTZ UND CYBERSICHERHEIT
- Durchführung einer umfassenden Bewertung der Risiken im Bereich Datenschutz und Cybersicherheit.
- Entwicklung und Umsetzung eines Plans zur Integration von Datenschutz- und Cybersicherheitssystemen.
- Gewährleistung der Einhaltung der DSGVO und anderer einschlägiger Vorschriften.
- Datenabgleich aller übertragenen Daten.
AKTUALISIERUNGEN DER TECHNISCHEN DATEN
- Verwaltung klinischer Daten und Bewertungen:
- Bewertung der Validität und Übertragbarkeit klinischer Daten.
- Aktualisierung der klinischen Bewertungsberichte (CERs) nach Bedarf.
- Durchführung von klinischen Nachbeobachtungsmaßnahmen nach der Markteinführung (PMCF).
Einhaltung der Kennzeichnungsvorschriften
- Überprüfung und Aktualisierung der Etikettierungsunterlagen, um den Eigentümerwechsel widerzuspiegeln und die Einhaltung der örtlichen Vorschriften sicherzustellen.
- Entwicklung einer einheitlichen Kennzeichnungsstrategie.
Herausforderung
Freyrs Service und wie wir Sie unterstützen
Schwankungen hinsichtlich des Reifegrades und des Konformitätsstatus von Qualitätsmanagementsystemen
Dienstleistungen zur Harmonisierung von Qualitätsmanagementsystemen: Unser Beraterteam für Fusionen und Übernahmen führt Lückenanalysen und interne Audits durch, um Qualitätsmanagementsysteme (QMS) mit ISO 13485 den behördlichen Vorschriften in Einklang zu bringen und so eine nahtlose Integration zu gewährleisten.
Komplexe Zulassungsanträge und Registrierungsübertragungen
Regulatory Affairs SoMAD (Spin-off, Fusionen und Übernahmen im Bereich Medizinprodukte, Veräußerungen) Dienstleistungen: Abwicklung von Zulassungsanträgen, Lizenzübertragungen und Kommunikation mit Behörden weltweit, um eine zeitnahe Zulassung und die fortlaufende Einhaltung der Vorschriften sicherzustellen.
Sicherstellung der Kennzeichnungskonformität unter Berücksichtigung des neuen Eigentümers
Aktualisierung der Kennzeichnung und Compliance-Dienstleistungen: Entwicklung und Umsetzung einheitlicher, konformer Kennzeichnungsstrategien, die den Eigentümerwechsel widerspiegeln und alle regionalen regulatorischen Anforderungen erfüllen.
Verwaltung klinischer Bewertungsdaten und PMCF )
Verwaltung klinischer Daten und Bewertungen: Bewertung der Übertragbarkeit klinischer Daten, Aktualisierung klinischer Bewertungsberichte (CERs) und Verwaltung von Aktivitäten im Rahmen der klinischen Nachbeobachtung nach der Markteinführung (PMCF).
Einhaltung der Vorschriften zum Datenschutz und zur Cybersicherheit
Bewertungen zum Datenschutz und zur Cybersicherheit: Bewertung und Integration von Datenschutz- und Cybersicherheitssystemen zur Gewährleistung der Einhaltung der DSGVO und anderer globaler Vorschriften.
Kombination von Systemen zur Marktüberwachung und Meldesystemen
Pharmakovigilanz und Medical Affairs – SoMAD-Dienstleistungen: Harmonisierung von Systemen zur Überwachung nach dem Inverkehrbringen, Meldung unerwünschter Ereignisse und Trendanalysen für eine einheitliche und vorschriftsmäßige Sicherheitsüberwachung.
Wir bieten NICHT an
Rechtliche Beratung bei Fusionen und Übernahmen im Bereich Medizinprodukte
Finanz- oder Transaktionsberatung
Dienstleistungen zur Integration in die Fertigung oder den Betrieb
Hinweis: Als Ihr Berater für regulatorische Fragen im Bereich Fusionen und Übernahmen konzentrieren wir uns ausschließlich auf die Einhaltung regulatorischer Vorschriften und bieten keine rechtlichen, finanziellen oder operativen M&A-Dienstleistungen an.
Warum mit Freyr zusammenarbeiten?

Erfolgsgeschichte
Optimierter globaler Markteintritt für ein KI-gestütztes Unternehmen für zahnmedizinische Diagnostik.
Ein junges KI-gestütztes Unternehmen für Zahndiagnostik arbeitete mit Freyr zusammen, um sich in der komplexen globalen Regulierungslandschaft zurechtzufinden.