Die SmPC oder Zusammenfassung der Merkmale des Arzneimittels ist ein rechtliches Dokument, das Teil der Zulassung jedes Arzneimittels ist. Das Dokument dient medizinischen Fachkräften als Informationsgrundlage für die Anwendung von Arzneimitteln. Die in der SmPC enthaltenen Informationen werden regelmäßig aktualisiert, sobald neue Informationen vorliegen. Die SmPC enthält mehr Informationen als eine Packungsbeilage. Die SmPC-Informationen sind über die folgenden Quellen zugänglich:
- Websites von Gesundheitsbehörden; wie der Europäischen Arzneimittel-Agentur (EMA)
- Arzneimittelwörterbücher
Woraus besteht ein SmPC?
- Informationen zur Arzneimittelanwendung
- Qualitative und quantitative Informationen zu Nutzen und Risiken von Arzneimitteln
- Dosierungsinformationen
- Verabreichungsmethode
- Pharmakologische Informationen
- Informationen zur individuellen Versorgung
Struktur einer SmPC
Die Struktur der SmPC ist durch die europäische Arzneimittelgesetzgebung festgelegt. Die in der SmPC enthaltenen Informationen sollten produktspezifisch sein und können querverwiesen werden, um Redundanzen zu vermeiden. Sie sollte in klarer Sprache dokumentiert sein und keine Unklarheiten aufweisen. Die SmPC ist in 6 Hauptabschnitte unterteilt:
- Name des Produkts
- Zusammensetzung
- Darreichungsform
- Klinische Angaben – Umfasst therapeutische Indikationen, Dosierungsempfehlungen und Sicherheitsinformationen
- Pharmakologische Eigenschaften – Berücksichtigt die therapeutischen Indikationen der klinischen Elemente und deren mögliche unerwünschte Arzneimittelwirkungen
- Pharmazeutische Angaben – Umfasst regulatorische Informationen zum Arzneimittel
Gemäß der EMA-Struktur kann ein SmPC wie folgt dargestellt werden:
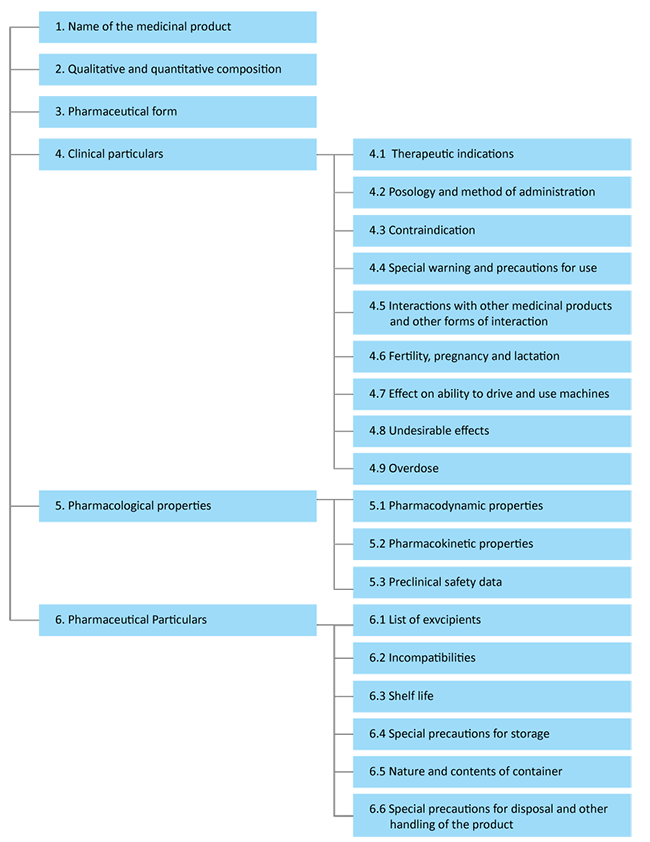
Quelle: EMA
Welche Informationen werden aus einem SmPC ausgeschlossen?
- Informationen, die in den öffentlichen Bewertungsberichten verfügbar sind (Details zur wissenschaftlichen Entwicklung)
- Informationen zu nicht zugelassenen Indikationen
- Aspekte, bei denen Daten fehlen
- Allgemeine Ratschläge zu pharmakologischen Zuständen
Die Pflege einer SmPC ist wichtig für den Lebenszyklus jedes Arzneimittels, da sie Teil seiner Zulassung ist. Daher wird die Erstellung einer konformen SmPC dringend empfohlen. Suchen Sie fachkundige regulatorische Unterstützung bei der Entwicklung einer SmPC? Kontaktieren Sie Freyr unter sales@freyrsolutions.com.