Das Medical Device Reporting (MDR) ist ein Instrument zur Überwachung nach dem Inverkehrbringen, das die Food and Drug Administration (FDA) nutzt, um die Geräteleistung zu überwachen, potenzielle gerätebezogene Sicherheitsprobleme zu erkennen und zu Nutzen-Risiko-Bewertungen von Geräten beizutragen. Der Zweck des MDR ist es, gerätebezogene unerwünschte Ereignisse rechtzeitig zu erkennen und zu beheben. Es ermöglicht Ärzten, Gesundheitseinrichtungen, Herstellern und Verbrauchern die freiwillige Meldung, um die Sicherheit und Wirksamkeit des Geräts nach dem Inverkehrbringen zu verstehen.
MDR gilt für alle Klassen von Medizinprodukten, die entweder in den Vereinigten Staaten von Amerika (US) hergestellt oder in die US importiert werden. Hersteller von Medizinprodukten, die ihre Produkte in den US vermarkten möchten, müssen die MDR einhalten, da dies sonst zu finanziellen Strafen führen kann. Sie gilt in den US, einschließlich eines ausländischen Ereignisses, d. h. sie gilt für legal in den Vereinigten Staaten vermarktete Medizinprodukte, die sowohl in den US als auch in anderen Ländern hergestellt wurden. Zusätzlich gibt es verschiedene Anwendungsfälle für eine MDR, wie zum Beispiel:
- wenn ein Produkt in den US hergestellt und lokal sowie in andere Märkte vertrieben wird
- wenn ein Produkt in den US hergestellt, aber in andere Märkte vertrieben wird
- wenn ein Produkt im Ausland hergestellt und in den US sowie in andere Märkte geliefert wird
- wenn ein Produkt im Ausland hergestellt und lokal vertrieben wird und
- wenn ein Produkt in den US untersucht wird
MDR und der Meldeprozessablauf
Die MDR-Verordnung enthält viele verbindliche Anforderungen für Hersteller, Importeure und Anwender von Medizinprodukten, bestimmte produktbezogene unerwünschte Ereignisse und Produktprobleme der FDA zu melden. Das unten dargestellte Prozessflussdiagramm beschreibt den Meldeprozess Schritt für Schritt.
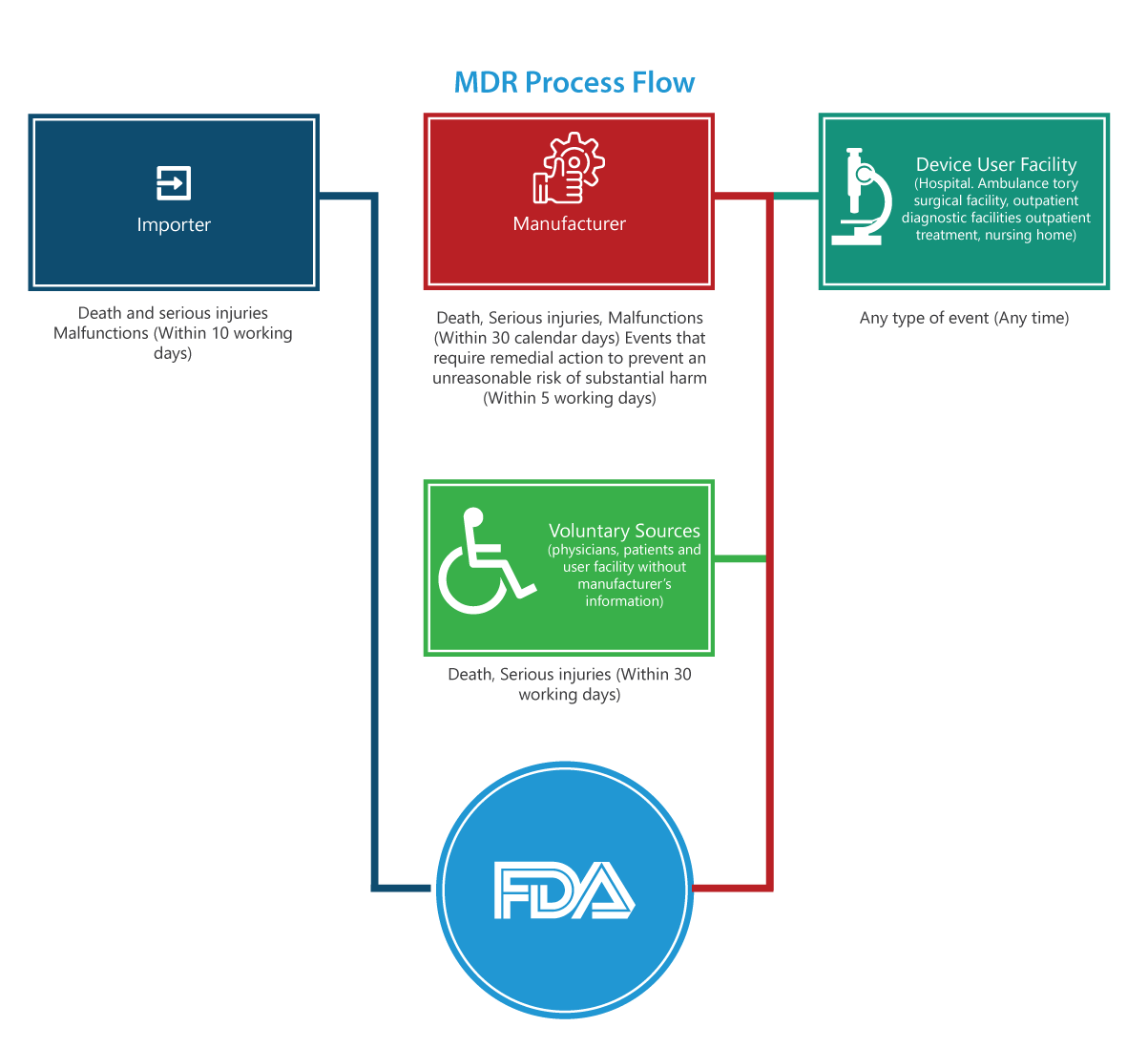
Für wen gilt es?
Importeure
Berichte über Todesfälle, schwere Verletzungen und Fehlfunktionen müssen der FDA und dem Hersteller innerhalb von 30 Arbeitstagen übermittelt werden. Kann die Fehlfunktion an anderer Stelle Verletzungen oder Todesfälle verursachen, müssen die Importeure die Fehlfunktion dem Hersteller melden.
Hersteller
Berichte über ein von der FDA festgelegtes Ereignis (Todesfälle, schwere Verletzungen und Fehlfunktionen) oder ein Ereignis, das Abhilfemaßnahmen erfordert, um ein unangemessenes Risiko erheblichen Schadens für die öffentliche Gesundheit zu verhindern, müssen der FDA innerhalb von 5 Arbeitstagen durch Ausfüllen des Formulars 3500A übermittelt werden.
Anwendereinrichtung für Medizinprodukte (Krankenhaus, ambulante chirurgische Einrichtung, Pflegeheim, ambulante Diagnostikeinrichtung oder ambulante Behandlungseinrichtung)
Berichte müssen dem Hersteller des Geräts spätestens 10 Arbeitstage, nachdem er Kenntnis davon erlangt hat, dass ein Gerät eine schwere Verletzung eines Patienten der Einrichtung verursacht oder dazu beigetragen hat oder haben könnte, übermittelt werden. Ist der Hersteller unbekannt, muss die Einrichtung den Bericht der FDA vorlegen.
Freiwillige Gruppen
Patienten, medizinisches Fachpersonal und Verbraucher, die ein Problem im Zusammenhang mit einem Medizinprodukt feststellen, können dies der FDA über MedWatch melden.
eMDR
Die FDA hat 2015 die elektronische Meldung von Medizinproduktevorfällen (eMDR) vorgeschrieben, um kritische Probleme der Datenqualität und -integrität im Zusammenhang mit der Meldung schwerwiegender Verletzungen bei allen Klassen von Medizinprodukten zu identifizieren. eMDR ist die bevorzugte Meldeform.
Hersteller können ihre eMDR über ein Electronic Submissions Gateway (ESG) einreichen. Ab dem Zeitpunkt der Einreichung dauert es bis zu 48 Stunden, bis das elektronische Gateway eine Bestätigung sendet. Sollte beim Einreichen des Berichts ein Fehler auftreten, wird eine Meldung zur Vornahme der Korrektur(en) angezeigt.
eMDR – Welche Vorteile bietet es?
eMDR bietet mehrere Vorteile gegenüber dem manuellen Meldemechanismus (d. h. MDR). Einige bemerkenswerte Vorteile, auf die Hersteller / Behörden / Patienten zählen können, sind unten aufgeführt:
- Das eMDR-Einreichungstool verbessert die Zusammenarbeit zwischen einer Organisation, der Gesundheitsbehörde (FDA) und Patienten.
- eMDR spart Kosten. Die Automatisierung reduziert den Bedarf an administrativem Aufwand und traditioneller Kommunikation; sie hilft, den Prozess zu beschleunigen und fördert eine effektive Ereignisberichterstattung, was zu einer sofortigen Interaktion mit der FDA führt.
- Manuelle Prozesse erfordern einen erheblichen Papieraufwand, können langwierig und schwer zu verfolgen und zu bearbeiten sein. Die eMDR-Einreichung ist automatisiert und zentralisiert. Datensätze können leicht abgerufen werden, was viel Zeit bei der Überprüfung spart.
- eMDR ermöglicht es den Beteiligten, Einreichungsfehler schnell zu kennzeichnen, im Gegensatz zu manuellen und zeitaufwändigen Korrespondenzen mit der FDA.
- eMDR fungiert als zentrale Anlaufstelle, um alle elektronischen Einreichungen in einer hochsicheren Umgebung zu verarbeiten, und ist vorteilhaft, da Beschwerden bei der Organisation direkt mit dem MedWatch-Formular verknüpft und in das Gateway der FDA integriert werden können.
eMDR und der Meldeprozessablauf
Die eMDR-Verordnung enthält verbindliche Anforderungen für Hersteller, Importeure und Anwendereinrichtungen von Medizinprodukten, bestimmte gerätebezogene unerwünschte Ereignisse und Produktprobleme an die FDA zu melden. Das untenstehende Flussdiagramm beschreibt den Meldeprozess Schritt für Schritt.
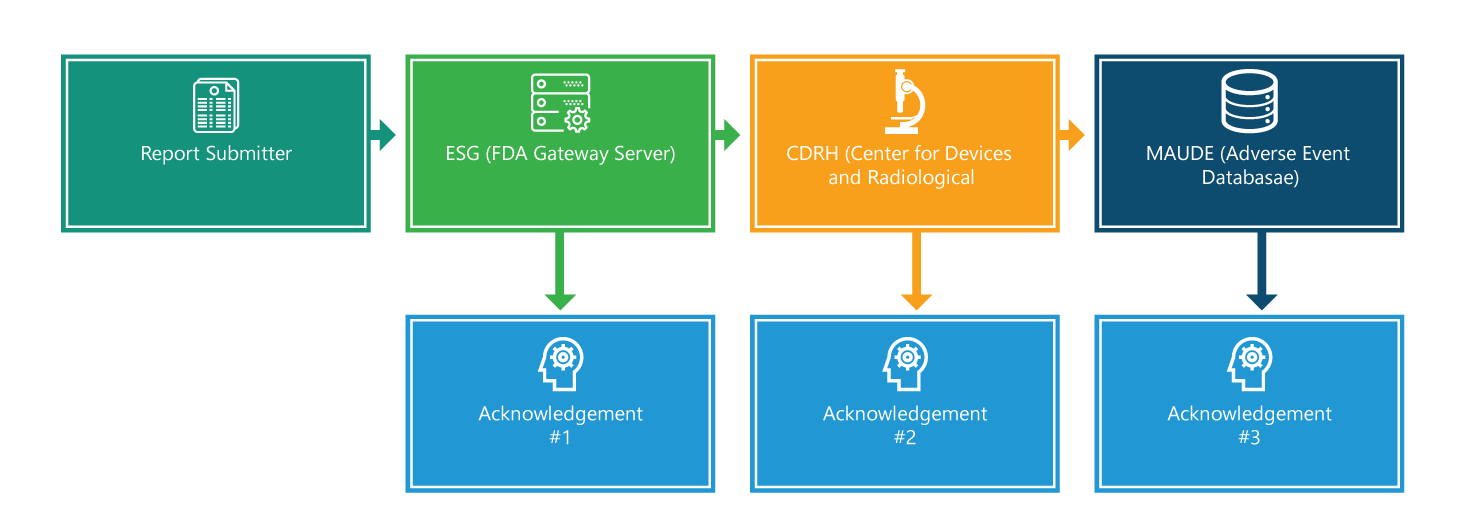
Der Meldeprozess besteht aus vier Schritten. Mit Ausnahme des ersten Schritts wird jeder Schritt bestätigt. Zusätzlich wird jeder Schritt mit weiteren Informationen versehen, die den Prozess erleichtern.
Schritt 1: Berichtseinreicher
Einreichung eines eMDR. Zunächst sollte man für eine Einreichung eine elektronische Signatur besitzen und sicherstellen, dass die Dateinamen der Einreichung nur einen Punkt enthalten, der zur Angabe der Dateityperweiterung verwendet wird (zum Beispiel 555.xml oder 555.pdf). Die Liefer- und Bearbeitungszeit des Antrags hängt jedoch von der Gesamtgröße Ihrer Einreichung ab; größere Einreichungen benötigen mehr Zeit für die Lieferung und Bearbeitung.
Schritt 2: Electronic Submissions Gateway (ESG)
Wenn Ihre Einreichung die ESG erreicht, sollten Sie schnell eine Bestätigung #1 erhalten, es sei denn, die ESG ist wegen Wartungsarbeiten nicht verfügbar. Sie müssen den Status Ihrer MDR auf der ESG-Website überprüfen.
Schritt 3: CRDH
eMDR wird automatisch vom ESG an das Center for Devices and Radiological Health (CDRH) weitergeleitet. Sobald es weitergeleitet wurde, wie in Schritt 2, sollten Sie eine Bestätigung erhalten, d.h. #2.
Schritt 4: Hersteller- und Anwendererfahrungen mit Medizinprodukten (MAUDE)
Wenn das CDRH die Einreichung in der Datenbank für unerwünschte Ereignisse (MAUDE) validiert und aktualisiert, wird erwartet, dass der Einreicher eine Bestätigung Nr. 3 erhält. Es ist zu beachten, dass alle Fehler, die während der Validierung und des Ladens auftreten, aufgezeichnet werden.
Das Meldewesen für Medizinprodukte (MDR) ist ein entscheidender Prozess, der dazu beiträgt, Leben zu retten und Patienten vor unnötigen Risiken zu schützen. Es stellt sicher, dass alle an der Patientenversorgung beteiligten Parteien verantwortungsbewusst und aufmerksam im Umgang mit Geräten sind.
eMDR erleichtert die Berichterstattung, aber die Dokumentation und Nachverfolgung können ressourcenintensiv sein. Machen Sie es gleich beim ersten Mal richtig; kontaktieren Sie uns unter sales@freyrsolutions.com.